
科目: 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法不正确的是( ) 
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到D点,可采用:温度不变在水中加入少量的酸
C.若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体
D.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。(已知:Na2SO3+H2SO4(浓) Na2SO4+SO2↑+H2O)

请回答下列问题:
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是________、________。
(2)反应后,装置B中发生的现象是______________,反应的离子方程式为__________;装置C中的现象是__________,表现了SO2的__________________;装置D中的现象是__________,发生反应的化学方程式为__________________。
(3)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象________________________________________________________________
(4)F装置的作用是_________________________,倒扣漏斗的作用是__________
查看答案和解析>>
科目: 来源: 题型:
【题目】I下面是几种实验中常用的仪器:
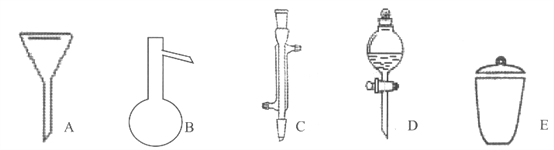
写出序号所代表的仪器的名称:
A__________;B__________;C__________;D__________;E__________
II实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题:
(1)配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、天平、量筒和__________________。
(2)用托盘天平称取氯化钠固体,其质量为__________g。
(3)下列主要操作步骤的正确顺序是____________________(填序号)。
①称取一定质量的氯化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度__________ (填“偏高”或“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】雾霾是对空气中各种悬浮颗粒物含量超标的笼统表述,而氮氧化物是造成酸雨和光化学烟雾的罪魁祸首之一,工业上在一定温度和催化剂条件下,NH3可用于消除NO的污染,生成一种无害气体。
(1)悬浮颗粒物可用高压电除去,利用了________________现象。
(2)实验室制备氨气的原理:_________________________(用化学方程式表示)。反应发生、气体收集和尾气处理的装置依次为_______(填序号)。
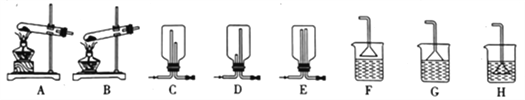
(3)实验室也可采用下图所示装置制取氨气。烧瓶内可选用______________(填序号)。

A.NaOH固体 B.无水氯化钙 C.二氧化硅 D.碱石灰
(4)按下图装置进行NH3性质实验。
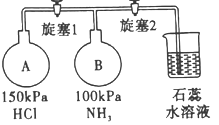
①先打开旋塞1,B瓶中的现象是_____________________,原因是______________________,稳定后,关闭旋塞1。
②再打开旋寒2,B瓶中的现象是_____________________________。
(5)请写出NH3与NO2反应的化学方程式:_______________________。该反应中每生成1nolN2转移的电子数____________________(结果保留1位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于电解质溶液的正确判断是( )
A.在pH=12的溶液中,K+、Cl﹣、HCO3﹣、Na+可以共存
B.水电离的c(H+)=1×10﹣3mol/L的溶液中:Na+、Fe3+、SO42﹣、Cl﹣
C.由0.l moI/L BOH溶液的pH=10,可推知BOH溶液存在BOH=B++OH﹣
D.![]() =1×10﹣13mol/L 的溶液中:Ba2+、ClO﹣、Cl﹣、NO3﹣
=1×10﹣13mol/L 的溶液中:Ba2+、ClO﹣、Cl﹣、NO3﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学一选修3:物质结构与性质]
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对立的辐射波长为_____________nm(填序号)。
A.589.2 B.500.3 C.650.2 D.434.4
(2)K和Fe属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Fe低,原因是________________________。
(3)基态I原子中,核外电子占据最高能层的符号为_____________________。
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长a=0.446am,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示,K与O间的最短距离为________nm,与K紧邻的O个数为_____________________。
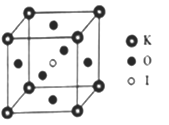
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于________位置,O处于__________位置。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列变化不能通过一步化学反应实现的是( )
A.BaCl2→BaSO4B.CuO→Cu(OH)2
C.NaOH→Na2CO3D.MgSO4→Mg(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com