
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 1.0mol·L-1的CH3COONa溶液中所含CH3COO-的数目一定小于NA
B. 46g二氧化氮(NO2)所含的电子数为23NA
C. 标准状况下,2.24 LCCl4中所含C-Cl键的数目为0.2NA
D. 将0.1mol H2和0.2molI2充入密闭容器中充分反应后,生成HI的分子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A. NH3、O2、NO、H2O(g)同时存在时,则反应达到化学平衡状态
B. 单位时间内生成x mol NO,同时消耗x mol NH3时,说明反应达到化学平衡状态
C. 达到化学平衡状态时,若增大容器体积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系是3v正(NH3)=2v正(H2O)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.通过石油的裂解可以获得更多的汽油
B.蛋白质、纤维素、油脂、聚乙烯、淀粉都是高分子化合物
C.研制乙醇汽油(汽油中添加一定比例的乙醇)技术,可以降低机动车辆尾气中有害气体排放
D.石油、煤、天然气、植物油都属于化石燃料
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组是
A.Mg2+、Ba2+、Br-B.Al3+、CH3COO-、Cl-
C.Mg2+、Cl-、Fe2+D.Na+、NH4+、Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题.
(1)写出下列有机物的名称
① ![]() ; ②
; ② ![]() .
.
(2)写出下列物质的化学式:
① ![]() ; ②
; ② ![]() .
.
(3)写出下列有机物的结构简式
①2﹣甲基﹣2﹣戊醇②甲基丙烯酸甲酯 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于“物质的量”“摩尔”和“摩尔质量”的叙述正确的是
A. “物质的量”是国际单位制中的个基本单位
B. 1mol任何物质均约含有6.02×1023个分子
C. 物质的摩尔质量等于其相对分子质量或相对原子质量
D. 0.012kg12C中所含的碱原子数为NA(NA代表阿伏加德罗常数的数值)
查看答案和解析>>
科目: 来源: 题型:
【题目】在一密闭容器中通入A、B、C三种气体,保持一定温度,在t1~t4 s时测得各物质的浓度如表,则下列判断正确的是
测定时刻/s 浓度 | t1 | t2 | t3 | t4 |
c(A)/(mol·L1) | 6 | 3 | 2 | 2 |
c(B)/(mol·L1) | 5 | 3.5 | 3 | 3 |
c(C)/(mol·L1) | 1 | 2.5 | 3 | 3 |
A.在t3 s时反应已经停止
B.t3~t4 s内正、逆反应速率不相等
C.在容器中发生的反应为A(g)+B(g)![]() C(g)
C(g)
D.在t2~t3 s内A的平均反应速率为![]() mol·L1·s1
mol·L1·s1
查看答案和解析>>
科目: 来源: 题型:
【题目】在使用分液漏斗进行分液时,正确的操作是( )
A.上层液体经漏斗下口放出
B.分离液体时,将漏斗拿在手上进行分离
C.分离液体时,使分液漏斗玻璃塞上的凹槽(或小孔)对准漏斗上的小孔,再将分液漏斗下面的活塞拧开
D.分液漏斗中盛装的是液体,振荡后不必打开活塞把气体放出
查看答案和解析>>
科目: 来源: 题型:
【题目】钢铁分析中常用高氯酸(HClO4)溶解矿样,某研究性学习小组欲制取少量高氯酸。该学习小组查阅到:
a.HClO4浓度高于60%时遇含碳化合物易爆炸,浓度低于60%时比较稳定;
b.NaClO4与浓硫酸反应可制得高氯酸,若采用真空蒸馏可得纯高氯酸;
c.NaClO3在673K(400℃) 分解产生NaClO4、NaCl和一种气体。
该小组同学设计实验分三步制备高氯酸:
(一)制氯气并使制得的氯气与氢氧化纳溶液反应制氯酸纳;
(二)氯酸钠分解制高氯酸钠;
(三)高氯酸纳与浓硫酸反应制高氯酸[2NaClO4+H2SO4(浓)![]() Na2SO4+2HClO4]。
Na2SO4+2HClO4]。
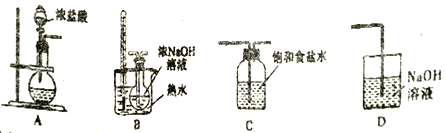
(1)制取氯酸钠的装置连接顺序为A,___________
(2)B 装置中发生反应的离子方程式为__________________________。
(3)为了制备高氯酸钠并推出氯酸钠分解制高氯酸钠的化学方程式,该小组设计了两组装置(甲,乙)如下:
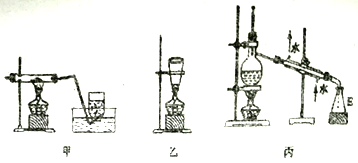
该小组经过分析决定选用甲装置制备高氯酸钠,取NaClO3样品2.13 g,加热充分反应后集气瓶中收集到224 mL (标准状况下)气体,则该反应的化学方程式为_________________________;不选用乙装置的原因可能为______________________。
(4)用丙裝置制备高氯酸,向烧瓶中加入高氯酸钠,然后加入浓硫酸后,加热可制取高氯酸。实验开始前,胶塞及导管接口需要包锡箔纸,其原因是___________,仪器E的名称为___________。该组同学发现操作中少加入一种物质,该物质的名称为___________。发现后的正确操作为_________________。
(5)工业上大量制备NaClO4常用高电流密度电解NaClO3的方法,试写出以惰性电极电解时的阳极反应式:_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com