
科目: 来源: 题型:
【题目】纳米碳酸钙是一种广泛应用于塑料、食品、医药、饲料等行业的重要无机填料。以磷石膏钙渣为原料制取高品质纳米碳酸钙的工艺流程如下:
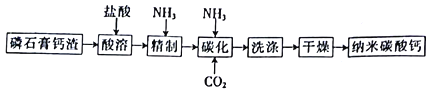
已知某磷石膏钙渣的主要成分及其含量如下表所示。
CaO | P2O5 | SO3 | Fe2O3 | Al2O3 | SiO2 | 烧失量 |
47.70% | 1.60% | 1.77% | 0.041% | 0.0027% | 9.85% | 37.69% |
请回答下列问题:
(1)对磷石膏钙渣进行酸溶的目的是获得机制CaCl2溶液,为了提高溶出率,可以采取的措施有___________(填字母)。
A.粉碎磷石膏钙渣 B.增大盐酸浓度 C.适当降低温度 D.缩短酸溶时间
(2)为了探究酸溶的工艺条件,称取6 份各50g磷石膏钙渣,分别用不同浓度盐酸进行溶解,反应时间为30 min,测得滤液中钙溶出率的结果如图所示,最适宜的盐酸浓度为___________。
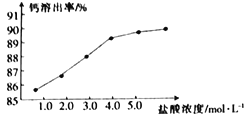
(3)精制是向粗制CaCl2溶液中通入氨气,控制溶液的pH,主要除去___________(填金属阳离子)。
(4)碳化时,先将精制CaCl2溶液稀释至一定体积,控制反应温度以及NH3和CO2 的通入量,此过程中,通入气体有先后顺序,应先通入气体的化学式___________(填化学式);碳化时发生反应的化学方程式为___________________________________________。
(5)把CaCO3浊液滴入1.0mol·L-1 的Na2SO3溶液中,能否产生CaSO3沉淀?___________。若不能,说明原因;若能,请从定量的角度简述判断依据:___________________________________。[已知:Ksp(CaSO3)=1.4×10-7,Ksp(CaCO3)=2.8×10-9
(6)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级:___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制备三氯乙醛(CCl3CHO)的反应原理为C2H5OH+4Cl2→CCl3CHO+5HCl可能发生的副反应是C2H5OH+HCl→C2H5Cl+H2O。某探兖小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。回答下列问题:

(1)仪器a的名称是______________。
(2)装置A中发生反应的离子方程式为____________________________________。
(3)仪器b中冷凝水从______(填“p”或“q”,下同)口进,___________口出。
(4)若撤去装置B,对实验的影响是__________________________________________________。
(5)实验时发现D中导管口处气泡速率过快,合理的解决方法是______________________。
(6)已知:CCl3CHO+OH-→CHCl3+HCOO-;HCOO-+I2-=H++2I-+CO2↑;I2+2S2O32-=2I-+S4O62-。称取0.40g产品,配成待测溶液,加入20.00mL0.100mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00mL。滴定时所用指示剂是__________________________,达到滴定终点的现象是_____________________________________________________,测得产品的纯度为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对下列各图描述不正确的是( ) 
A.在NaCI晶体中,距Na+最近的Cl﹣有6个
B.在BaO2晶胞中,每个晶胞平均占有4个Ba2+和4个O ![]()
C.在金刚石晶体中,碳原子与碳碳键的个数比为1:2
D.该气态分子的分子式为EF或FE
查看答案和解析>>
科目: 来源: 题型:
【题目】在高温高压下碳氧化物具有极高的化学活性,能与多种单质或化合物反应。
(1)一定条件下,CO与H2 可合成甲烷,反应方程式为:CO(g)+3H2(g) ![]() CH4(g)+ H2O(g)
CH4(g)+ H2O(g)
①一定条件下,该反应能够自发进行的原因是_________
②已知H2(g)、CO(g)和CH4(g)的燃烧热分别为285.8kJ/mol 283.0kJ/mol和890.0kJ/mol。
写出CO 与H2 反应生成CH4 和CO2 的热化学方程式:_____________。
(2)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO (g) +2H2 (g) ![]() CH3OH (g)
CH3OH (g)
反应Ⅱ: CO2 (g) +3H2 (g) ![]() CH3OH (g) +H2O (g)
CH3OH (g) +H2O (g)
①在以上制备甲醇的两个反应中:反应Ⅰ优于反应Ⅱ,原因为______________。
②一定温度下,在体积可变的密闭容器中加入4molH2和一定量的CO发生反应Ⅰ,开始时容器体积为2L,CO 和CH3OH (g) 的浓度随时可变化如图。10min 达到平衡,则反应1的化学平衡常数为____________。
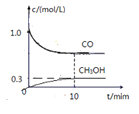
③恒温恒容条件下,在密闭容器中等物质的量的通入CO2 和H2, 下列描述能说明反应Ⅱ已经达到平衡状态的是___。(填标号)
A.容器内CO2的体积分数不再变化
B.当CO2和H2转化率的比值不再变化
C.单位时间CH3OH分子断裂5NA个共价键,同时断裂3NA个H-H键
D.容器内混合气体的平均相对分子质量为34.5,且保持不变
(3)甲烷碱性燃料电池装置如图所示(开始时两边溶液质量相等),用电器为惰性电极电解装置,其原理是:通电后,将Co2+氧化成Co3+,进而彻底氧化CN-为无害气体使废水得以净化。
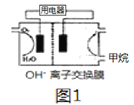
①当除去1molCN-时,图1两边质量差为__________g.
②负极电极反应式为__________.
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,反应方程式为:CH3OH(g)+CO(g) ![]() HCOOCH3(g) ΔH=-29.1KJ/mol,科研人员对该反应进行了研究.部分研究结果如下:
HCOOCH3(g) ΔH=-29.1KJ/mol,科研人员对该反应进行了研究.部分研究结果如下:
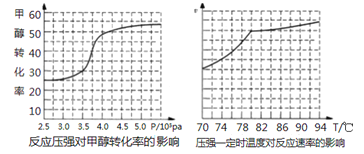
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是_____。
②实际工业生产中采用的温度是80℃,其理由是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式中,属于水解反应的是( )
A.HCOOH+H2OHCOO﹣+H3O+
B.CO32﹣+H2OHCO3﹣+OH﹣
C.CO2+H2OHCO3﹣+H+
D.HS﹣+H2OS2﹣+H3O+
查看答案和解析>>
科目: 来源: 题型:
【题目】在2 L密闭容器内,充入一定量的NO和O2,800 ℃时发生反应2NO(g)+O2(g) ![]() 2NO2(g),n(NO)随时间的变化如表:
2NO2(g),n(NO)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)反应在1 s~2 s内,O2的物质的量减少________mol。
(2)如图所示,表示NO2变化曲线的是________。用O2表示从0~2s内该反应的平均速率v=________。
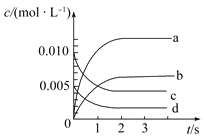
(3)能说明该反应已达到平衡状态的是________(填序号)。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________;K、F、Zn的电负性从大到小的顺序为___________。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________。
(3)OF2分子的几何构型为___________,中心原子的杂化类型为___________。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在___________;与O3-互为等电子体的分子为___________ (任 写一种 )。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为___________个。
②晶胞中紧邻的两个F-间的距离为_______________________(列出算式即可)nm。
③该晶体的密度为___________(列出算式即可,用NA表示阿伏加德罗常数的数值)g·cm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入 1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
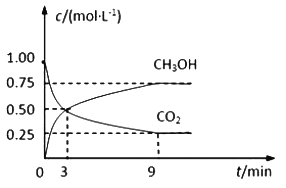
(1)从3 min到9 min,υ(H2)=________mol·L-1·min-1。
(2)能说明上述反应达到平衡状态的是____________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为______________。
(4)平衡时混合气体中CH3OH(g)的体积分数是__________________。
(5)一定温度下,第9分钟时υ逆(CH3OH) _______(填“大于”、“小于”或“等于”)第3分钟时υ正(CH3OH)。
查看答案和解析>>
科目: 来源: 题型:
【题目】镁、硫、氮的化合物在工业上用途非常广泛。
(1)硝酸厂尾气中含有大量的NO,可用氢气催化还原法除去NO,发生的主要反应如下:
2NO(g)+4H2(g)+O2(g)=N2(g)+4H2O(g) △H=-1143 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-484 kJ·mol-1
则2NO(g)+2H2(g)=N2(g)+2H2O(g) △H=___________kJ·mol-1。
(2)一种镁一锂双离子二次电池的装置如图1所示。
①放电时, Mg 电 极 为___________ (填“ 正极”或“负极” ), Li +迁 移 至___________ (填“正极区”或“负极区”)。
②充电时,阳极的电极反应式为_______________________________。
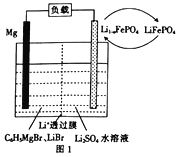
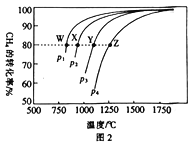
(3)在一定条件下,反应:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)平衡时CH4的转化率与温度和压强的关系如图2所示。
2CO(g)+2H2(g)平衡时CH4的转化率与温度和压强的关系如图2所示。
①图中p1、p2、p3、p4 代表不同压强,压强最大的是___________。该反应的△H___________(填“>"“<”或“=”下同)0。
②压强为p4时,在Y点:v(正)___________v(逆)。
③图中W、X、Y、Z四点对应的反应的平衡常数K1、K2、k3、K4由大到小的顾序为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com