
科目: 来源: 题型:
【题目】化学学习中要注重对过程的分析,按要求回答下列问题:
(1)向石蕊试液中通入氯气,观察到的现象是________________________,用化学方程式进行分析________________________________;若将氯水久置,将会有气泡冒出,用化学方程式进行分析_______________________________
(2)将一小块钠投入到盛FeCl3的溶液中,观察到的现象是__________________,用化学方程式进行分析________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】由硫和亚硫酸钠共热可制备硫代硫酸钠(Na2S2O3),Na2S2O3是重要的化工料,易溶于水,在酸性溶液中发生如下反应:S2O32-+2H+=S↓+SO2↑+H2O。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O),并测定产品的纯度。装置如下(已略去加热装置):
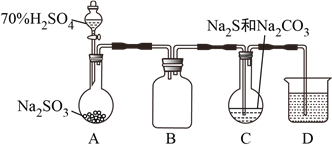
(1)D是尾气处理装置,盛放的溶液可以是__________。
a.酸性高锰酸钾溶液 b.NaOH溶液 c.饱和NaHSO3溶液
(2)C中发生的化学反应有:__________、2Na2S+3SO2=2Na2SO3+3S↓、__________。
(3)经过系列操作,该小组同学从C中制得了Na2S2O3·5H2O,此晶体中可能混有Na2SO3和Na2SO4杂质。接下来,他们做实验证明了则两种杂质的存在,请完成操作:取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,__________,沉淀未完全溶解,并有刺激性气味的气体产生(已知Ba2+与S2O32-不生成沉淀)。
(4)该组同学经讨论认为:先向A中滴加70%的H2SO4,产生的气体将装置中的空气排尽后,再向C加入Na2S和Na2CO3混合溶液,可减少装置C中生成的Na2SO4的量,画出改进后的C装置。___________

(5)测定Na2S2O3·5H2O的纯度:称取Wg产品,用适量蒸馏水溶解,滴加少量淀粉溶液,用0.1000mol·L-1碘的标准溶液滴定,反应原理为2S2O32-+I2=S4O62-+2I-。
①判断反应达到滴定至终点的标志是:______________________________。
②滴定起始和终点的液面位置如图,则产品的纯度为(Na2S2O·5H2O的摩尔质量为Mg·mol-1)____________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】已知某温度下CH3COOH的电离常数K=1.6×10﹣5 . 该温度下,向20mL 0.01molL﹣1 CH3COOH溶液中逐滴加入0.01molL﹣1 KOH溶液,回答下列有关问题:
(1)醋酸溶液中c(H+)为 , pH约为 .
(2)用滴定管取CH3COOH溶液20.00mL放在锥形瓶中,滴加几滴酚酞,待测.滴定管在使用前除洗涤外,还应 .
(3)判断到达滴定终点的实验现象是;
(4)下列操作中,可能使所测CH3COOH溶液的浓度偏低的是
A.碱式滴定管未用标准碱液润洗就直接注入标准液
B.读取碱液体积时,开始仰视读数,滴定结束时俯视读数
C.碱式滴定管在滴定前有气泡,滴定后气泡消失
D.滴定前盛放CH3COOH溶液的锥形瓶用蒸馏水洗净后没有干燥.
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学为了检验浓硫酸与木炭粉在加热条件下反应:![]() ,产生的所有气体产物,选用了下图所示实验装置。
,产生的所有气体产物,选用了下图所示实验装置。
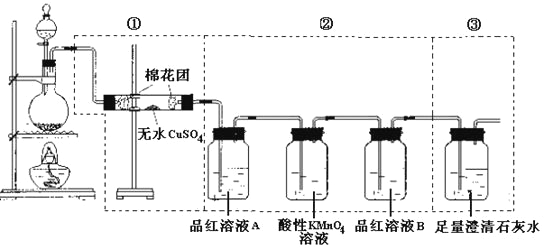
(1)①中无水硫酸铜的作用是___________。
(2)②中酸性KMnO4溶液的作用是______________________。
(3)②中两次用到品红溶液,它们的作用分别是A________、B________。
(4)③中发生反应的离子方程式是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】R2O82-离子在一定条件下可以把Mn2+离子氧化,若反应后R2O82-离子变为RO42-离子,又知反应中氧化剂和还原剂的物质的量之比为5︰2,Mn2+离子被氧化后的化合价为
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
科目: 来源: 题型:
【题目】明代《本草纲目》中与“烧酒”有关的条目:用浓酒和糟入甑,蒸令气上…其清如水,味极浓烈,盖酒露也”。下列说法正确的是( )
A.“烧酒”为纯净物
B.“酒露”为有刺激性气味的气体
C.“烧酒”的制作过程中没有物理变化
D.这里制作“烧酒”的方法是指蒸馏
查看答案和解析>>
科目: 来源: 题型:
【题目】已知下列热化学方程式: Zn(s)+ ![]() O2(g)═ZnO(s)△H=﹣351.1kJmol﹣1
O2(g)═ZnO(s)△H=﹣351.1kJmol﹣1
Hg(l)+ ![]() O2(g)═HgO(s)△H=﹣90.7kJmol﹣1
O2(g)═HgO(s)△H=﹣90.7kJmol﹣1
由此可知反应Zn(s)+HgO(s)═ZnO(s)+Hg(l)的焓变△H为( )
A.﹣260.4 kJmol﹣1
B.﹣441.8 kJmol﹣1
C.+260.4 kJmol﹣1
D.+441.8 kJmol﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | Q | R |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(1)Z在元素中期表中的位置是______________________________。
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是__________(填离子符号)。
(3)周期表中有些处于对角线(左上→右下)位置的元素,它们的单质及其化合物的性质相似,则M的氧化物与强碱溶液反应的离子方程式______________________________。
(4)Q和R按原子个数比1:1组成的化合物甲是一种“绿色”氧化剂。
①甲中所含共价键类型是____________________。
②空气阴极法电解制备甲的装置如图所示。在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液。图中a是__________极,阴极的电极反应式是____________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示:
(1)则25℃时水的电离平衡曲线应为(填“A”或“B”),请说明理由
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 .
(3)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 .
(4)曲线B对应温度下,pH=2的HCl溶液和pH=10的某BOH溶液等体积混合后,混合溶液的pH=8.请分析其原因: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com