
科目: 来源: 题型:
【题目】纯水能微弱地电离出H+和OH﹣ , 在25℃时,水电离出的H+和OH﹣浓度为 . 水的电离过程是一个吸热过程,升高温度,水的离子积(填“增大”“减小”或“不变”)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存的是
A. Na+、Mg2+、Cl-、OH- B. H+、Ca2+、CO32-、NO3-
C. Cu2+、K+、SO42-、NO3- D. Na+、H+、OH-、Ca2+
查看答案和解析>>
科目: 来源: 题型:
【题目】已知Na2SO3固体与硫酸可发生反应:Na2SO3+ H2SO4=Na2SO4+H2O+SO2↑,下图是实验室制取SO2并验证SO2的某些性质的装置图。回答正确的是( )

A. ①中的实验现象为紫色石蕊试液褪色此实验证明SO2具有漂白性
B. ③中溶液变浑浊是因为SO2和H2S发生了氧化还原反应,氧化产物和还原产物质量比为1∶1
C. ④和②中溶液均褪色,但褪色的原理不同
D. 实验室中可以用澄清石灰水代替氢氧化钠溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
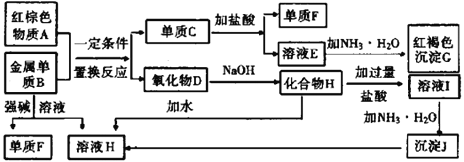
(1)如果把红棕色物质A换成黑色磁性晶体,推测出来的物质是完全一致的,请写出黑色磁性晶体与过量盐酸反应的化学方程式_______________________________。
(2)写出单质B与强碱溶液反应的离子方程式:_______________________________。把溶液Ⅰ中的阳离子完全转化为沉淀J为什么加氨水而不加氢氧化钠_______________。
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:_________________________。白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式_________________________。
(4)保存E溶液时候为什么要加入单质C,用离子方程式解释_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】依据图1中氮元素及其化合物的转化关系,回答问题:
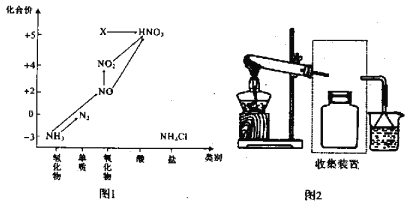
(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为____________________。
(2)若要收集一瓶氨气,请将下列装置补充完整,在图2虚框内画出连接图。____________
(3)下列试剂可用于干燥NH3的是________________________________。
A.浓硫酸 B.碱石灰 C.CuSO4固体 D.P2O5
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO化学方程式为________________________________;
②NO→NO2实验现象是________________________________;
③将32.64g铜与l40mL一定浓度的HNO3反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。则其中NO、NO2的物质的量比为____________________。
(5)图1中在标准状况下将NO2、NO、O2混合并充满容器,将该容器倒置于水中,气体完全溶解,无气体剩余,若产物也不扩散,则所得溶液的物质的量浓度M,其数值大小范围为___________
A.0<M<l/22.4 B. 1/39.2<M<1/22.4 C.1/39.2<M<1/28 D.1/28<M<1/22.4
(6)图1中X转化为HNO3的化学方程式为:________________________________。
(7)若要将NH3→N2,从原理上看,下列试剂可行的是_______________。
A.O2 B.Na C.NH4Cl D. NO2
查看答案和解析>>
科目: 来源: 题型:
【题目】在配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释到所需的浓度,这样操作的目的是( )
A.提高硫酸铁的溶解度
B.防止硫酸铁分解
C.降低溶液的pH
D.抑制硫酸铁水解
查看答案和解析>>
科目: 来源: 题型:
【题目】氯气在工业上有着重要的用途,某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝(无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾)。可用下列装置制备。

(1)装置B中盛放____溶液,C和F中装的是同一种试剂,该试剂为________________。
(2)装置A的圆底烧瓶中发生反应的化学方程式为_______________________________。
(3)实验步骤:如图连接装置后,先检验装置气密性,再装药品,然后点燃___________(填“A”或“C”)处酒精灯,当____(填实验现象)时,再点燃___________(填“A”或“C”)处酒精灯。
(4)装置G的作用是__________________,写出G中反应的离子方程式_____________________。
(5)甲同学认为装置D和E中间的细玻璃导管换成粗的玻璃导管为什么?___________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】请回答下列问题:
(1)下列所给出的几组物质中:含有分子数最少的是________________;标准状况下体积最小的是_____________________。
①1gH2 ②2.408×1023个CH4分子 ③10.8gH2O ④标准状况下6.72LCO2
(2)请配平方程式:___KClO3+____HCl(浓)=___KC1+____ ClO2↑+___Cl2↑+__H2O,__________
(3)溶液导电能力取决于自由移动离子的浓度和所带电荷数,离子浓度越大,所带电荷数越多,溶液导电能力越强。现有浓度均为lmol/L的以下电解质溶液:①K2CO3 ②AgNO3 ③NaHSO4 ④Al2(SO4)3⑤H2SO4 ⑥Ba(OH)2。这些溶液中导电能力最强的是__________(填序号),导电能力最弱的是____________。
(4)有12.4gNa2R含Na+为0.4mol,则Na2R的摩尔质量为____________。
(5)在0.2L由NaCl溶液、MgCl2溶液、CuCl2溶液组成的混合溶液中,部分离子的浓度如图所示。该混合溶液中CuCl2的物质的量浓度为____________ molL-1。

(6)下图所示的警示标志,是一种____________(填选项序号)。

A.易燃品 B.剧毒品 C.腐蚀品 D.爆炸品
查看答案和解析>>
科目: 来源: 题型:
【题目】能源是人类生存和发展的重要支柱,碳元素的单质及化合物是人类生产生活的主要能源物质.
(1)有机物M经过太阳光光照可转化为N,转化过程如下: 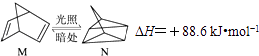
则M、N相比,较稳定的是 .
(2)CO可用于合成燃料甲醇.在有催化剂存在的10L恒容密闭容器中充入2mol CO和4mol H2 , 发生如下反应:CO(g)+2H2(g)CH3OH(g). 测得CO的平衡转化率与温度、压强的关系如图所示:
①判断上述反应达到平衡状态的依据是(填字母编号).
A.CH3OH的生成速率与CO的消耗速率相等
B.CH3OH、CO、H2的浓度都不再发生变化
C.混合气体的密度不变
D.混合气体的相对平均分子质量不变
②下列措施中,能使上述平衡体系中 ![]() 的值增大的是(填字母编号).
的值增大的是(填字母编号).
A.降低温度 B.充入He(g),使体系压强增大 C.再充入1mol CO和2mol H2
③100℃时反应在5min末达到平衡,则从反应开始至达平衡,v(H2)=mol/(Lmin);该温度下反应的平衡常数K= . 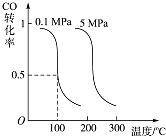
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com