
科目: 来源: 题型:
【题目】将1.76g铜镁合金完全溶解于一定浓度的硝酸中,得到NO和NO2标准状况下896mL的混合气体,向反应后的溶液中加入lmol/L的NaOH溶液,当金属离子全部沉淀时,得到3.12g沉淀。下列说法不正确的是
A. 合金中铜镁物质的最之比为1:1
B. 产生的NO和NO2的体积之比为1:1
C. 得到3.12g沉淀时,加入NnOH溶液体积一定是80mL
D. 1.76g该合金与足量盐酸反应,可生成标准状况下448mL气体
查看答案和解析>>
科目: 来源: 题型:
【题目】向物质的量浓度均为1mol/L的HCl、AlCl3、MgC12、NH4Cl混合溶液中逐滴加入1mol/L的NaOH溶液,得到如图图像。下列有关说法正确的是

A. 沉淀的最大物质的量为2mol
B. c-d段会产生标况下22.4LNH3
C. d-e段发生的反应为Al3++40H-=AlO2-+2H2O
D. 滴加NaOH溶液过程中,微粒反应的先后顺序是H+、Mg2+、NH4+、Al(OH)3
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25%的酒精密度为0.96 g·cm-3,5%的酒精密度为0.99 g·cm-3。若将上述两溶液等体积混合,所得酒精溶液的质量分数是 ( )
A. 等于15% B. 大于15%
C. 小于15% D. 无法估算
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.乙醇在水中能电离出少量的H+,所以乙醇是电解质
B.乙醇与O2发生不完全燃烧生成乙醛
C.乙醇分子中所有的氢原子都可被钠置换出来
D.乙醇是一种很好的溶剂,能溶解多种物质
查看答案和解析>>
科目: 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义.
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等.已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g)△H1=+489.0kJmol﹣1
C(石墨)+CO2(g)═2CO(g)△H2=+172.5kJmol﹣1
则CO还原Fe2O3的热化学方程式为
(2)某实验将CO2和H2充入一定体积的密闭容器中,在两种不同温度条件下反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49.0kJmol﹣1
测得CH3OH的物质的量随时间变化如下图所示,回答问题: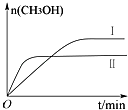
①该反应的平衡常数表达式K=;
②曲线Ⅰ、Ⅱ对应的平衡常数大小关系为:KⅠKⅡ(填“>”、“=”或“<”).
③下列措施中能增大CO2转化率的是 . (填序号)
A.升高温度B.充入He(g)使体系压强增大
C.将H2O(g)从体系中分离 D.再充入一定量CO2
④下列图象正确且能表明在t时刻反应一定处于平衡状态的是 . (填序号)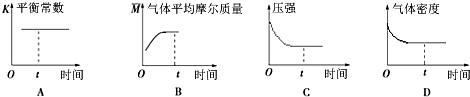
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A.凡是含有羟基的化合物都是醇
B.可以通过加成反应制得乙醇
C.钠与乙醇反应比与水反应更剧烈
D.乙醇与钠反应生成氢气,此现象说明乙醇具有酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铜矿(主要成分为CuFeS2)是海洋矿物中的一种,它是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。请回答下列问题:
(1) 利用黄铜矿冶炼铜的反应为8CuFeS2+21O2![]() 8Cu+4FeO+2Fe2O3+16SO2。已知CuFeS2中Fe的化合价为+2,Cu的化合价为+2,
8Cu+4FeO+2Fe2O3+16SO2。已知CuFeS2中Fe的化合价为+2,Cu的化合价为+2,
① 反应中被还原的元素是________(填元素符号),
② 生成1 mol Fe2O3时转移电子的物质的量为________mol。
(2)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3,方法为:①用过量稀盐酸浸取炉渣,过滤。②先将滤液氧化,再向其中加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。据以上信息回答下列问题:
A.①中过滤的目的是____________________,
B.②中将滤液氧化常常选用H2O2,其反应的离子方程式为____________________。
C.只能选用提供的试剂,设计实验验证炉渣中含有FeO。提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水,
① 所选试剂为___________________
② 证明炉渣中含有FeO的实验现象为_____________________
查看答案和解析>>
科目: 来源: 题型:
【题目】滴定法是化学上常用的定量分析的方法.滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等.
(1)甲化学兴趣小组取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用0.2000molL﹣1的标准NaOH溶液进行滴定.重复上述滴定操作3次,并记录数据.
a.滴定时边滴边摇动锥形瓶,眼睛应观察 . (填序号)
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
b.判断滴定终点的现象是: .
c.根据下列数据:请计算待测盐酸溶液的浓度为 mol/L.
滴定次数 | 待测液体积(mL) | 标准NaOH溶液读数记录(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 4.00 | 24.00 |
第三次 | 20.00 | 2.00 | 24.10 |
(2)乙化学兴趣小组利用氧化还原反应滴定,测定了某工厂废水中游离态氯的含量.实验如下:
①取水样10.0ml于锥形瓶中,加入10.0ml的KI溶液(足量),滴入指示剂2~3滴.
②将自己配制的0.01molL﹣1标准Na2S2O3溶液装入滴定管中,调整液面,记下读数.
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+2Na2S4O6 . 试回答下列问答:
a.步骤①发生的化学反应方程式为:;加入的指示剂是 .
b.步骤②应使用式滴定管.
c.氯的所测浓度比实际浓度会偏大,造成误差的原因可能是(填序号)
A 配制标准Na2S2O3溶液定容时,加水超过刻度线
B 锥形瓶水洗后直接装待测水样
C 装标准Na2S2O3溶液的滴定管水洗后没有润洗
D 滴定到达终点时,俯视读出滴定管读数;
E 滴定前尖嘴部分有气泡,滴定后消失
(3)沉淀滴定所用的指示剂本身就是一种沉淀剂.已知一些银盐的颜色和Ksp(20℃)如下表,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定.
化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
Ksp | 2.0×10﹣10 | 5.4×10﹣13 | 8.3×10﹣17 | 2.0×10﹣48 | 2.0×10﹣12 |
a.滴定时,你认为该滴定适宜选用的指示剂是下列中的 . (填序号)
A.KBrB.KIC.K2S D.K2CrO4
b.向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, ![]() = .
= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com