
科目: 来源: 题型:
【题目】下列反应中,浓硫酸既表现强氧化性,又表现酸性的是
①2NaC1(固)+ H2SO4(浓) ![]() Na2SO4+2HC1↑
Na2SO4+2HC1↑
②C +2H2SO4(浓) ![]() CO2↑+ 2SO2↑+2H2O
CO2↑+ 2SO2↑+2H2O
③Cu+2H2SO4(浓) ![]() CuSO4+ SO2↑+2H2O
CuSO4+ SO2↑+2H2O
④2FeO+4H2SO4(浓)=Fe2(SO4)3+SO2↑+4H2O
A. ①② B. ③④ C. ①③ D. ②④
查看答案和解析>>
科目: 来源: 题型:
【题目】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A. 60 mL B. 45 mL C. 30 mL D. 15 mL
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化合物能用相应元素的单质直接化合生成的是
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S ⑥FeCl2 ⑦H2S ⑧FeCl3
A. ②③⑤⑦⑧ B. ①④⑥⑦ C. ①②③⑦⑧ D. ②③⑤⑥⑦⑧
查看答案和解析>>
科目: 来源: 题型:
【题目】有一镁铝合金,用适量稀硫酸完全溶解,再加入氢氧化钠溶液,析出沉淀的质量与加入氢氧化钠的体积关系如图所示,原合金中镁铝的质量比为

A. 4:9 B. 4:3 C. 8:9 D. 20:27
查看答案和解析>>
科目: 来源: 题型:
【题目】空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.右图为RFC工作原理示意图,有关说法正确的是( ) 
A.转移0.1mol电子时,a电极产生1.12LH2
B.b电极上发生还原反应
C.酸性电解质溶液中H+移向c电极
D.d电极上发生的电极反应是:O2+4H++4e﹣=2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.在由水电离产生的氢离子浓度为10﹣13 mol?L﹣1的溶液中:Ca2+、K+、Cl﹣、HCO ![]() 四种离子能大量共存
四种离子能大量共存
B.已知MgCO3的Ksp=6.82×10﹣6 , 则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO ![]() ),且c(Mg2+)?c(CO
),且c(Mg2+)?c(CO ![]() )=6.82×10﹣6
)=6.82×10﹣6
C.对于反应2N2H4(l)=N2(g)+2H2(g),△H=﹣50.6 kJ?mol﹣1 , 它只在高温下自发进行
D.常温下,将0.2 mol?L﹣1某一元碱(ROH)溶液和0.1 mol?L﹣1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+)
查看答案和解析>>
科目: 来源: 题型:
【题目】ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2,还含少量Fe2O3、Al2O3、SiO2等杂质)通过如下方法制取:
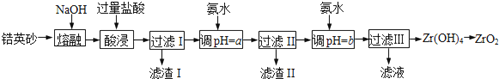
已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表。
金属离子 | Fe3+ | Al3+ | ZrO2+ |
开始沉淀时pH | 1.9 | 3.3 | 6.2 |
沉淀完全时pH | 3.2 | 5.2 | 8.0 |
(1)熔融时ZrSiO4发生反应的化学方程式为 ,滤渣I的化学式为 。
(2)为使滤液I的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是 ;继续加氨水至pH=b时,所发生反应的离子方程式为 。
(3)向过滤III所得滤液中加入CaCO3粉末并加热,得到两种气体。该反应的离子方程式为 。
(4)为得到纯净的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式正确的是
A. 硫酸氢钠溶液与小苏打溶液的反应:H+ + HCO3- = CO2↑ + H2O
B. 用苛性钠溶液吸收过量SO2:SO2 +2OH-= SO32- + H2O
C. 二氧化锰和浓盐酸反应:MnO2+4HCl![]() Mn2++2Cl2↑+2H2O
Mn2++2Cl2↑+2H2O
D. 工业上氯气和石灰乳反应制漂白粉:Cl2 + 2OH-= ClO-+ Cl- + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com