
科目: 来源: 题型:
【题目】常温下用惰性电极电解200mLNaCl、CuSO4的混合溶液,所得气体的体积随时间变化如下图所示,根据图中信息回答下列问题:( 注:气体体积已换算成标准状况下的体积,且忽略气体在水中的溶解和溶液体积的变化.)
(1)曲线(选填“Ⅰ”或“Ⅱ”) 表示阳极产生气体的变化情况.
(2)NaCl的物质的量浓度为;CuSO4 的物质的量浓度 .
(3)t2时所得溶液的pH为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为: 2KClO3 +4HCl(浓)===2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况:(单线桥法表示)________________________。
(2)氧化剂与还原剂的物质的量之比是 ___________________
(3)若产生标况下22.4 L Cl2,则转移的电子的物质的量为________mol。
(4)实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸中HCl的物质的量浓度 mol·L-1。
(5)ClO2对污水中Fe2+、Mn2+、S2-和CN- 等有明显的去除效果。某工厂污水中含CN- a mg/L,现用ClO2将CN - 氧化,只生成两种气体,其离子反应方程式为为 ,处理100 m3这种污水,至少需要ClO2 _______mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】化工原料红矾钠(重铬酸钠:Na2Cr2O72H2O)主要是以铬铁矿(主要成分为FeOCr2O3 , 还含有Al2O3、SiO2等杂质)为主要原料生产,其主要工艺流程如下: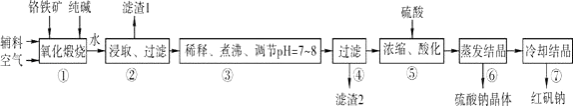
步骤①中主要反应的化学方程式如下:
4FeOCr2O3+8Na2CO3+7O2═8Na2CrO4+2Fe2O3+8CO2
(1)①中反应是在回转窑中进行的,反应时需不断搅拌,其作用是 .
(2)杂质Al2O3在①中转化的化学反应方程式为 .
(3)用化学平衡移动原理说明③中煮沸的作用是(用离子方程式结合文字说明),若调节pH过低产生的影响是 .
(4)⑤中酸化是使CrO42﹣转化为Cr2O72﹣写出该反应的离子方程式: . 
(5)工业上还可用电解法制备重铬酸钠,其装置示意图如上.阴极的电极反应式为;
阳极的电极反应式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组在实验室制取CO2气体的过程中,不慎用到了浓盐酸,导致制得的CO2气体中混有HCl气体,他们设计了如下除去HCl气体并探究CO2与过氧化钠(Na2O2)反应的实验。请回答下列问题:
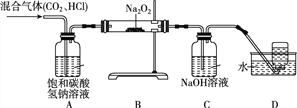
(1)装置A的作用是___________________________。
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含________,该小组同学继续进行探究。
【提出问题】反应后硬质玻璃管中固体的成分是什么?
(3)【做出猜想】猜想一:Na2CO3;猜想二:NaOH;猜想三:Na2CO3和NaOH
经过讨论,大家一致认为猜想二不合理,理由是_____________________________(用化学反应方程式表示)。
(4)【实验验证】小组同学取上述形成的溶液M于试管中,向其中加入过量的____________________溶液,若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想三成立。
(5)【交流反思】小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,你认为该同学的观点_____________(填“正确”或“错误”),理由是:____________________________________________(用化学反应方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学兴趣小组的同学为了探究原电池工作的原理,进行了如下系列实验,请你一起参与实验并分析实验结果后回答有关问题: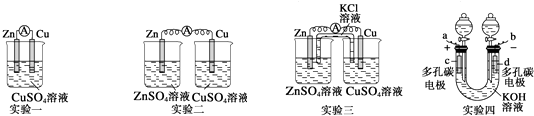
(1)实验一中铜片、锌片表面均有红色物质析出,电流计指针偏转,但较短时间内电流即明显减小.实验结束时测得锌片减少了3.94g,铜片增重了3.84g,则该原电池的工作效率是(指参加原电池反应的锌占反应总量的百分数).
(2)实验二中刚将铜、锌片插入溶液中时电流计指针有偏转,但立即就归零了.解释锌失去的电子能不能持续通过导线流向铜极给Cu2+ .
(3)实验三中盐桥中的K+流向溶液(填ZnSO4或CuSO4),如果Zn的消耗速率为1×10﹣3 mol/s,则K+的迁移速率为mol/s.
(4)实验四中,调节低压电源的电压到6V,并把其正、负极分别与上图装置中的两个碳电极相连接;接通电源,图示中的“+”连接到电源的正极上,“﹣”连接到电源的负极上,电解氢氧化钾溶液制取氢气、氧气,且制得的氢气与氧气的体积比为2:1,去掉电源,该装置就成为一只氢氧燃料电池,用带有一小灯泡的导线连接a、b,灯泡即可发亮.则下列说法错误的是 .
A.在电解KOH溶液制备H2和O2时,KOH的作用是增强溶液的导电性,一段时间后其浓度增大
B.当作为氢氧燃料电池时,c极发生氧化反应,d极发生还原反应
C.当作为氢氧燃料电池时,电解质溶液中的OH﹣向着d极移动
D.如将KOH溶液换成稀H2SO4 , 且作为氢氧燃料电池时,c极的电极反应为:O2+2H2O+4e﹣═4OH﹣ .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法正确的是( )
A.容量瓶使用前必须干燥,否则将引起误差
B.蒸馏实验结束后,先停止通冷凝水,再停止加热
C.含硫酸的废液倒入水槽,用水冲入下水道
D.不慎将酒精灯打翻在桌上失火时,立即用湿抹布盖灭
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式的书写正确的是
A. 漂白粉溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO
B. 碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
C. 向Fe2(SO4)3溶液中加入过量铁粉:2Fe3++Fe===3Fe2+
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,部分元素在周期表中的位置关系如右图所示.其中X是周期表中原子半径最小的元素,Q与X同主族;Z的最外层电子数是次外层的3倍.
Y | Z | ||
R |
请回答下列问题:
(1)写出Y元素的名称:________,Q的原子结构示意图________;R在周期表中的位置为________.
(2)Q2Z电子式为:________,Q2Z2含的化学键类型为:________.
(3)R、Z分别形成简单离子的半径大小:________________(离子符号表示)
(4)Y的氢化物与其最高价氧化物对应的水化物反应的化学方程式为:__________________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各物质的转化关系如下图所示.B、D是气体,其中B是空气的主要成分之一;C是淡黄色固体,常用于供氧剂;E是红棕色固体;F是最常见的无色液体.

回答下列问题:
(1)C的化学式是_______________.
(2)气体D通入紫色石蕊溶液的现象是_____________________.
(3)写出反应①的离子方程式______________________________________.
(4)写出反应②的化学方程式_____________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com