
科目: 来源: 题型:
【题目】某元素位于第三周期第ⅥA族.下列叙述不正确的是( )
A.该元素是非金属元素
B.该元素原子的核电荷数为16
C.该元素原子核外有3个电子层
D.该元素原子容易失去最外层电子
查看答案和解析>>
科目: 来源: 题型:
【题目】利用下列实验装置不能完成相应实验的是( )

A. 用装置①测量生成氧气的化学反应速率
B. 用装置②比较NaHCO3和Na2CO3的热稳定性
C. 装置③中分液漏斗内的液体可顺利加入蒸馏烧瓶
D. 装置④可实现制取CO2实验中的“即关即止,即开即用”的作用
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式书写正确的( )
A.钠与水的反应:2Na+2H2O═2Na++2OH﹣+H2↑
B.硅酸钠溶液中通入过量CO2:SiO ![]() +2CO2+2H2O═H2SiO3↓+2HCO3﹣
+2CO2+2H2O═H2SiO3↓+2HCO3﹣
C.氯气与水反应:Cl2+H2O═2H++Cl﹣+ClO﹣
D.明矾溶液中加入过量的Ba(OH)2溶液:Al3++4OH﹣═AlO2﹣+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关离子检验的操作和实验结论正确的是( )
A.向某溶液加入NaOH并微热,产生能够使湿润的红色石蕊试纸变蓝的无色气体,该溶液中一定含有NH ![]()
B.向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有SO ![]()
C.向某溶液中加入氨水,产生白色沉淀,则该溶液中一定含有Mg2+
D.用铂丝蘸取某溶液在酒精灯火焰上灼烧,若火焰呈黄色,则证明该溶液中无K+离子
查看答案和解析>>
科目: 来源: 题型:
【题目】“绿水青山就是金山银山”,研究NO2、NO、CO、NO2- 等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)已知:①NO2 + CO ![]() CO2 + NO 该反应的平衡常数为K1(下同)
CO2 + NO 该反应的平衡常数为K1(下同)
每1mol下列物质分解为气态基态原子消耗能量分别为
NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
②N2(g)+O2(g) ![]() 2NO(g) ΔH=+179.5 kJ/mol K2
2NO(g) ΔH=+179.5 kJ/mol K2
③2NO(g) +O2(g)![]() 2NO2(g) ΔH=-112.3 kJ/mol K3
2NO2(g) ΔH=-112.3 kJ/mol K3
试写出NO与CO反应生成无污染物气体的热化学方程式____________________________以及此热化学方程式的平衡常数K=____________(用K1、K2、K3表示)
(2)污染性气体NO2与CO在一定条件下的反应为:2NO2+4CO![]() 4CO2+N2,某温度下,在1L密闭容器中充入0.1mol NO2和0.2mol CO,此时容器的压强为1个大气压,5秒时反应达到平衡时,容器的压强变为原来的
4CO2+N2,某温度下,在1L密闭容器中充入0.1mol NO2和0.2mol CO,此时容器的压强为1个大气压,5秒时反应达到平衡时,容器的压强变为原来的![]() ,则反应开始到平衡时CO的平均反应速率v(CO)=________。
,则反应开始到平衡时CO的平均反应速率v(CO)=________。
若此温度下,某时刻测得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,a的取值范围________________。
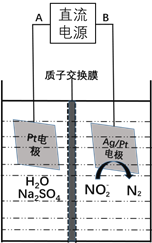
(3)电化学降解NO2-的原理如下图:
①电源的负极是____________(填A或B)阴极反应式为________________。
②若电解过程中转移了6mol电子,则膜两侧电解液的质量变化差![]() 为_____g。
为_____g。
查看答案和解析>>
科目: 来源: 题型:
【题目】小闵同学拥有下列实验仪器:
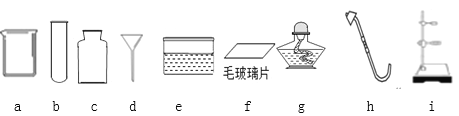
(1)写出仪器名称:c______。
(2)实验室用氯酸钾和二氧化锰制取氧气:
①上述仪器中不需要用到的是(填序号)_____。
②在用排水法收集氧气的过程中,判断集气瓶中氧气已集满的现象是______。
A.集气瓶中水位下降了;
B.在水槽中出现气泡;
C.将带火星的木条放在集气瓶口,木条复燃。
③要从反应后的剩余固体中回收二氧化锰,需要以下操作步骤:______、______、洗涤、烘干。
④小闵是否可以用向上排空气法收集氧气______(填写是或否)。
⑤小闵若在实验室利用12.25g氯酸钾与3gMnO2混合加热,列式计算最多可以得到多少物质的量的氧气____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“空气中氧气体积分数的测定”有多种方法,请按要求回答下列问题:在燃烧匙内盛过量红磷,红磷必须过量的原因是______,点燃红磷后立即插入集气瓶内,塞紧橡皮塞红磷燃烧的现象是____________,其反应的化学方程式为____________________。待红磷火焰熄灭,集气瓶冷却至室温,打开止水夹,观察到的现象是______,该实验除了得出氧气在空气中的体积分数之外,还能得出氮气具有的性质是______(任写一点);若测得空气中氧气的体积分数约为1/7,则可能的原因是______。

查看答案和解析>>
科目: 来源: 题型:
【题目】质量守恒定律的定量研究对化学科学发展具有重大意义。
(1)下图为某化学反应的微观模拟图,“○”和“![]() ”分别表示两种不同的原子:
”分别表示两种不同的原子:
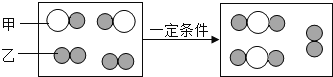
由微粒甲“![]() ”聚集成的物质______(填“可能”或“不可能”)是氧化物,参加反应的甲、乙两种反应物分子的个数比为______,此反应的基本反应类型为______,任举一例符合此反应类型的化学方程式______。
”聚集成的物质______(填“可能”或“不可能”)是氧化物,参加反应的甲、乙两种反应物分子的个数比为______,此反应的基本反应类型为______,任举一例符合此反应类型的化学方程式______。
(2)把m1g镁带放在空气中完全燃烧,通过计算可知,生成氧化镁m2g(只考虑与氧气的反应,下同),则m1______m2(填大于或小于或等于)。小嘉同学在做该实验时,观察到耀眼的白光,冒出大量白烟,称量无误时,发现m1>m2,其原因可能是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com