
科目: 来源: 题型:
【题目】25℃时,pH=3的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如下图所示。下列说法不正确的是

A. 曲线I代表盐酸的稀释过程
B. a溶液的导电性比b溶液的导电性强
C. b溶液中和氢氧化钠的能力强于a溶液
D. 将a、b两溶液加热至30℃, 变小
变小
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4s内A的平均反应速率v(A)=0.005 mol/(L·s)。下列说法正确的是
A. 4s时c(B)为0.78 mol/L
B. 该反应AH>0
C. 830℃达平衡时,A的转化率为20%
D. 1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数为2.5
A(g)+B(g)的平衡常数为2.5
查看答案和解析>>
科目: 来源: 题型:
【题目】下列烃①C4H8 ②C4H10 ③C6H12 ④C7H8分别完全燃烧,耗氧量分析正确的是
A. 等质量时耗氧量最多的是④
B. 等物质的量时耗氧量最少的是②
C. 等物质的量时③和④耗氧量相等
D. 某气态烃CxHy与足量O2恰好完全反应,如果反应前后气体体积不变(温度>100℃),则y=4;若体积减小,则y>4;反之,则y<4
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂的废液经测定其主要含有乙醇,此外还有丙酮、乙酸和乙酸乙酯.以上各物质的沸点如下:
物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
沸点/℃ | 56.2 | 77.06 | 78 | 117.9 |
现拟通过下列步骤回收乙醇和乙酸:
①向废液中加入甲溶液;②将混合液放入蒸馏器中缓缓加热;③收集温度在70℃~85℃之间的馏出物;④排出蒸馏器中的残液,冷却后向其中加入乙溶液(过量),然后再放入蒸馏器中进行蒸馏,收集馏出物.
可选用试剂:A.烧碱溶液 B.浓硫酸 C.饱和食盐水 D.浓盐酸
请回答下列问题:
(1)乙醇的沸点比丙酮沸点高的主要原因是 .
(2)加入甲溶液是 , (填A B C D序号),涉及到的反应方程式: .
(3)在70℃~85℃时馏出物的主要成分为 .
(4)在步骤④中加入过量的乙溶液是 . (填A B C D序号),
(5)最后蒸馏的温度控制在 .
(6)在蒸馏操作中,仪器选择及安装都正确的是:(填标号)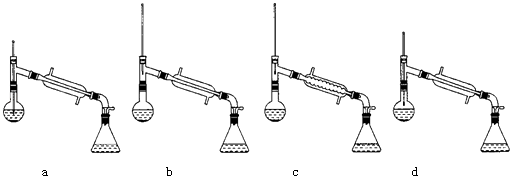
如果蒸馏前忘记加沸石,液体温度已接近沸点时,应该如何处理? .
查看答案和解析>>
科目: 来源: 题型:
【题目】LiOH是制取锂和锂的化合物的原料,用电解法制备LiOH的工作原理如下图所示:

下列叙述不正确的是
A. b极附近溶液的pH减小
B. a极发生的反应为2H2O-4e-===O2↑+4H+
C. 该法制备LiOH还可得到硫酸和氢气等产品
D. 当电路中通过1mol电子时,可得到1mol LiOH
查看答案和解析>>
科目: 来源: 题型:
【题目】已知1mol链烃CxHy可以发生如上系列转化:(无机试剂是足量的)下列说法错误的是
![]()
A. x=5、n=10
B. 用酸性高锰酸钾溶液可以区分CxHy和Q
C. 上述转化过程中依次发生了加成反应和取代反应
D. Q的同分异构体数目少于CxH12
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某碱性硼化矾(VB2)﹣空气电池工作时发生反应为:11O2+4VB2═2V2O5+4B2O3 . 以该电池作为电源,使用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( ) 
A.VB2电极发生的电极反应为:2VB2+11H2O﹣22e﹣═V2O5+2B2O3+22H+
B.若B装置内的液体体积为400mL,则CuSO4溶液的物质的量浓度为0.025mol/L
C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生
D.外电路中电子由a电极流向b电极
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7.下列关于滤液中的离子浓度关系不正确的是( )
A.![]() <1.0×10﹣7mol/L
<1.0×10﹣7mol/L
B.c(Na+)=c(HCO ![]() )+c(CO
)+c(CO ![]() )+c(H2CO3)
)+c(H2CO3)
C.c(H+)+c(NH4+)>c(OH﹣)+c(HCO ![]() )+2 c(CO
)+2 c(CO ![]() )
)
D.c(Cl﹣)>c(HCO ![]() )>c(NH4+)>c(CO
)>c(NH4+)>c(CO ![]() )
)
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究外界条件对反应:mA(g)+nB(g)cZ(g)△H的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( ) 
A.在恒温恒压条件下,向已达到平衡的体系中加入少量Z,达新平衡时,Z的物质的量分数增大
B.升高温度,正、逆反应速率都增大,平衡常数增大
C.△H>0,m+n>c
D.温度不变,减小压强,平衡逆向移动,达新平衡时,A的浓度比原平衡减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com