
科目: 来源: 题型:
【题目】某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、CaMg(CO3)2、A12O3和Fe2O3等,回收其中镁的工艺流程如下:

沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
pH | 4.7 | 3.2 | 9.7 | 10.4 | 11.2 |
部分阳离子以氢氧化物形式完全深沉时溶液的pH 由见上表
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有_____________________(要求写出两条)
(2)滤渣I的主要成分有_________________________。
(3)从滤液II中可回收利用的主要物质有________________________。
(4)若最终得到的氯化镁溶液中,c(Mg2+)=0.02 mol·L-1,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1.0×10-5 mol·L-1 ,此时是否有Mg3(PO4)2沉淀生成?_______(列式计算)。FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24。
(5) Mg (C1O3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备: MgCl2+2NaC1O3=Mg (C1O3)2+2NaCl已知四种化合物的溶解度(S) 随温度(T) 变化曲线如下图所示: ①将反应物按化学反应方程式计量数比混合制备Mg (ClO3)2。简述可制备Mg (ClO3)2的原因:_______________________。
②按①中条件进行制备实验。在冷却降温析出Mg (ClO3)2过程中,常伴有NaCl 析出,原因是:__________。除去产品中该杂质的方法是:___________________________________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】最新研究表明,有毒气体H2S具有参与调节神经信号传递、舒张血管减轻高血压的功能。
(1)下列事实中,可以用来比较H2S与H2SO3的酸性强弱的是______(填标号)。
A.H2S 的还原性强于H2SO3
B.0.10 mol·L-1的H2S和H2SO3的pH分别为4.5和2.1
C.H2S 不能与NaHCO3溶液反应,而H2SO3可以
D.等浓度的两种溶液pH 值: NaHS > NaHSO3
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知(1)式和(5)式的热化学方程式分别为___________、________________,制得等量H2所需能量系统I是系统II的_______倍。
(3)H2S与CO2在高温下发生反应: H2S(g)+CO2(g) ![]() COS(g) +H2O(g) △H >0;保持T1温度,将0.20mol CO2与0.80mol H2S充入2.5L的空钢瓶中,反应平衡后COS的物质的量分数为0.02
COS(g) +H2O(g) △H >0;保持T1温度,将0.20mol CO2与0.80mol H2S充入2.5L的空钢瓶中,反应平衡后COS的物质的量分数为0.02
①H2S的平衡转化率a1=_______%,反应平衡常数K=______________。
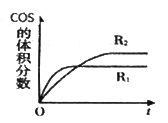
②在不同条件下发生上述反应,COS 的体积分数随时间(t)的变化如图所示,根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是____________(填字母序号)CO2的转化率a2__a1,(填”>”或“<”)
A.压强 B.温度 C.催化剂
(4)反应开始,保持T1温度,2L 钢瓶中充入0.08molCO2、0.40mo1H2S、0.02molCOS和0.02molH2O,则此时V正___V逆(填”>”或“<”)判断依据是___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)请你将反应Cu+2FeCl3==CuCl2+2FeCl2设计成原电池并回答下列问题:
①写出电极反应式:正极_____________________;负极_________________________。
②画出你所设计的原电池简易装置图_________。
(2)该电池向外提供0.2mol 电子,负极材料的质量变化为________________________。
(3)利用反应2Cu+O2+2H2SO4==2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极的反应式为____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为了探究碳酸钙与稀盐酸反应过程中的速率变化,在VmL稀盐酸中加入足量的碳酸钙,收集反应放出的CO2(气体体积已换算为标准状况下的数值),实验记录如下(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
CO2体积(mL) | 50 | 120 | 232 | 290 | 310 |
(1)0~1 min、1~2 min、2~3 min、3~4 min、4~5 min五个时间段中,_________反应速率最快。
(2)假设溶液体积不变,4~5min时间段以盐酸的浓度变化来表示的该反应速率为____________________________。
(3)为了降低上述化学反应的反应速率,向溶液中加入下列物质,你认为可行的是
_______________(填编号)。
a.蒸馏水 b.浓盐酸 c.NaCl固体 d.NaCl溶液
(4)除了上述方法外,你认为还可以采取哪些措施来降低化学反应速率?(试写两条)_______________________________________________________________________,
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在Mg(NO3)2和Al(NO3)3的混合溶液中,NO3﹣的物质的量为0.7mol.向该溶液中加入100mL 8molL﹣1的KOH溶液,使之充分反应,反应前,若Al3+的物质的量与混合溶液中离子总物质的量的比值为x. (不考虑Mg2+和Al3+的水解及水的电离所引起的离子总数的变化)
(1)x的取值范围是 .
(2)当KOH刚好完全消耗,且Al3+全部转化为AlO2﹣时,x的取值范围 .
(3)将(2)中的x值记为x1 , 则: 当0<x<x1时,反应生成的沉淀物的化学式为 .
当x>x1时反应生成的沉淀物的化学式为
(4)若反应前Al3+的物质的量为a mol,则a=(用含x的代数式表示).
查看答案和解析>>
科目: 来源: 题型:
【题目】根据题意解答
(1)相同条件下,体积之比为a:b和质量之比为a:b的H2和O2的混合气体,其平均相对分子质量为和 .
(2)已知各物质参加反应的物质的量之比等于其在化学方程式中的计量数之比,气体化合物A的分子式可表示为OxFy , 同温同压下,10mLA受热分解生成15mLO2和10mLF2 , 则A的化学式为 , 推断的依据为 .
查看答案和解析>>
科目: 来源: 题型:
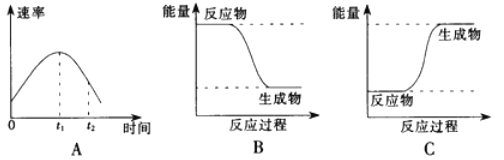
【题目】(1)某小组同学在烧杯中加入5mL1.0mol/L盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,如图A所示,该反应是_________________________。(填“吸热”或“放热”)反应,其能量变化可用图中的____________(填“B”或“C”)表示。
(2)已知拆开1mo1H-H键、1molN![]() N、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。当1mo1 NH3_______________(填“放出”或“吸收”)________kJ 的热量。
N、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。当1mo1 NH3_______________(填“放出”或“吸收”)________kJ 的热量。
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钙(CaO2)是一种白色晶体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。通常利用CaCl2在碱性条件下与H2O2反应制得。
某化学兴趣小组在实验室制备CaO2的实验方案和装置示意图(图一)如下:


请回答下列问题:
(1)三颈烧瓶中发生的主要反应的化学方程式为___________________________________;
(2)支管B的作用是_________________________;
(3)步骤③中洗涤CaO2·8H2O的液体X的最佳选择是____________;
A.无水乙醇 B.浓盐酸 C.水 D.CaCl2溶液
(4)过氧化钙可用于长途运输鱼苗,这体现了过氧化钙___________的性质;
A.可缓慢供氧 B.能吸收鱼苗呼出的CO2气体 C.能潮解 D.可抑菌
(5)已知CaO2在350℃时能迅速分解,生成CaO和O2。该小组采用如图二所示的装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体)
①检查该装置气密性的方法是:_________________________________;
②使用________(填仪器名称)准确称取0.5000g样品,置于试管中加热使其完全分解,收集到33.60mL(已换算为标准状况)气体,则产品中过氧化钙的质量分数为________(保留4位有效数字);
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com