
科目: 来源: 题型:
【题目】短周期元素X、Y、Z组成的化合物Y2X和ZX2。Y2X溶于水形成的溶液能与ZX2反应生成一种化合物Y2ZX3.已知三种元素原子的质子总数为25,且Z和Y的原子序数之和比X的原子序数2倍还多1,Z原子有2个电子层,最外层电子数是核外电子数的2/3倍,试回答:
(1)Y元素在元素周期表中的位置___________________________
(2)Y2X对应水化物的电子式_______________________________
(3)X的氢化物比同主族的氢化物的熔沸点明显偏高的原因_________________________
(4)Z元素的最简单氢化物与X单质可形成一种原电池,如果以氢氧化钠溶液为电解质,则该原电池负极电极反应方程式为:________________________________________
(5)X、Y两种元素还可以形成另外一种化合物,试用电子式表示该物质的形成过程:_______________,该化合物与1mol ZX2完全反应,则反应中电子转移的数目为___________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5.X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物.请回答:
(1)X元素的名称是;Y元素的名称是;Z元素的名称是: .
(2)XZ3化合物的分子式是 , 电子式是 .
(3)分别写出X、Y的含氧酸的分子式、 .
查看答案和解析>>
科目: 来源: 题型:
【题目】I:已知:反应aA(g)+bB(g) ![]() cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
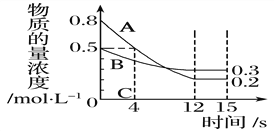
(1)经测定前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为_______________________
(2)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1; 乙:v(B)=0.12 mol·L-1·s-1; 丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为__________________(用甲、乙、丙表示)。
Ⅱ: 某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
氢气体积/mL | 50 | 120 | 224 | 392 | 472 | 502 |
(3)哪一时间段反应速率最大__(填0~1、1~2、2~3、3~4、4~5、5~6 min,下同),原因是_______________________________________________________
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是__________(填字母)
A.CH3COONa B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
Ⅲ:(5)下列说法可以证明H2(g)+I2(g)![]() 2HI(g)已达平衡状态的是______________________
2HI(g)已达平衡状态的是______________________
A.单位时间内生成n mol H2的同时,生成n mol HI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=![]() v(HI)
v(HI)
E.温度和体积一定时,容器内压强不再变化
F.温度和体积一定时,混合气体的密度不再变化
查看答案和解析>>
科目: 来源: 题型:
【题目】1.92g Cu片与一定量的浓HNO3作用,当收集到NO2和NO气体共1.12L时(标准状况),金属铜恰好全部作用.则:
(1)反应中消耗HNO3mol,转移电子mol.
(2)用排水法收集生成的气体,最后气体的体积为L(标准状况).
(3)向收集到的气体中通入mL O2(标准状况)才能使水刚好充满整个集气容器.
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ:用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥MgCl2
⑦NH3H2O ⑧Na2O2 ⑨HClO ⑩CaO
(1)只存在离子键的是:_______________
(2)既存在离子键又存在共价键的是:__________________
(3)试写出⑨的电子式:_________________________________________________________
Ⅱ: (4)氢氧燃料电池,是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)燃料电池。如果是酸性燃料电池则正极反应方程式是:_____________
(5)科研人员设想用如图原电池装置生产硫酸:则负极的电极反应式为:______________________________________________________

查看答案和解析>>
科目: 来源: 题型:
【题目】Fe和Fe2O3的混合物15g,加入150mL稀硫酸中,标准状况下放出H21.68L,同时固体全部溶解.向溶液中滴加硫氰化钾溶液后,未见颜色变化.若向溶液中加入3molL﹣1 NaOH溶液200mL,恰好使铁元素全部沉淀.则该稀硫酸的物质的量浓度为( )
A.2.25molL﹣1
B.2molL﹣1
C.0.6molL﹣1
D.0.3molL﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】氮及其化合物与生产生活关系密切。请完成下列填空:
(1)肼由N、H 两种元素组成,它常用作火箭推进剂。肼的相对分子质量为32,分子中N、H原子的个数比为1∶2,肼的分子式为_____________。16g 肼分子中所含的氮原子数与标准状况下_______L N2中所含的氮原子数相等。
(2)实验室常用下图所示装置制取并收集氨气。

①实验室制取氨气反应的化学方程式为____________________________________;
②图中方框内收集氨气的装置可选用_________________(填字母序号);
③尾气处理装置中使用倒扣漏斗的作用是_________________________________。
(3)在盛有一定量浓硝酸的试管中加入6.4g的铜片发生反应。请回答下列问题:
①开始阶段,反应的化学方程式为____________________________________,若该反应共产生标准状况下气体2.24L,则反应过程中被还原的HNO3的物质的量为_______。
②反应结束后铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式为____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com