
科目: 来源: 题型:
【题目】A、B、C、D、E和F表示含有10个电子的微粒,请回答:
(1)A离子为单核离子且A原子在所在周期中原子半径最大,A离子是______;(填离子符号)
(2)D是由两种元素组成的分子,其水溶液呈碱性,D的结构式是_______________;
(3)向含B微粒溶液中加入含F微粒溶液,先出现白色沉淀,继续加入含F微粒溶液沉淀溶解,写出该过程的离子方程式__________________________________
(4)向含E微粒溶液中加入含F微粒溶液,并加热生成 C和D,写出该离子方程式____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法不正确的是
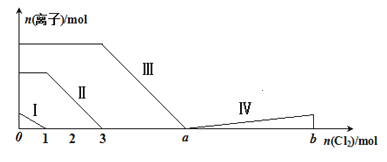
A. 线段Ⅱ表示Fe2+的变化情况
B. 线段Ⅳ发生反应的离子方程式为:I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O
C. 根据图象可计算a=6
D. 原溶液中c(Fe2+)∶c(I-)∶c(Br-)=2∶1∶3
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为长式周期表的一部分,其中的编号代表对应的元素。请回答下列问题:
① | ② | ③ | |||||||||||||||
④ | ⑤ | ⑥ | ⑦ | ||||||||||||||
⑧ | ⑨ | ⑩ |
(1)⑥元素在周期表中的位置是第______周期______族;
(2)上表①~⑩十种元素中金属性最强的是______,非金属性最强的是______;(填元素符号)
(3)用电子式写出表中元素④原子与元素⑦原子形成化合物的过程________________;
(4)写出③元素的氢化物与⑩元素的氢化物反应生成盐的电子式__________;
(5)写出③元素的最高价氧化物对应的水化物的稀溶液与过量的元素⑨单质反应的离子方程式_________________________________;
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与元素⑧的最高价氧化物对应的水化物的溶液反应的化学方程式:______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用太阳能分解水制氢,若光解0.02mol水,下列说法正确的是( )
A.可生成H2的质量为0.02g
B.可生成氢的原子数为2.408×1023个
C.可生成H2的体积为0.224L(标准情况)
D.生成H2的量理论上等于0.04mol Na与水反应产生H2的量
查看答案和解析>>
科目: 来源: 题型:
【题目】已知24mL浓度为0.05mol/L 的Na2SO3溶液恰好与V mL浓度为0.04mol/L的K2X2O7溶液完全反应。得到X元素在产物中的化合价为+3。则V为
A. 40 B. 30 C. 20 D. 10
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将pH=3 的硫酸与pH=9的NaOH 溶液混合,若要得到pH=7 的溶液,混合时硫酸酸与NaOH溶液的体积比为( )
A.1:200
B.200:1
C.100:1
D.1:100
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下表中的信息分析回答问题:
元素 | 元素或由元素组成的物质性质 |
A | 单质在自然界中硬度最大,燃烧产生的气体能使澄清石灰水变浑浊。 |
B | 原子最外层电子数是次外层电子数三倍 |
C | 金属焰色反应为黄色,与氧气燃烧生成淡黄色固体 |
D | 单质在空气中体积分数最大 |
E | 固体为淡黄色,燃烧产生气体有漂白性。 |
F | 相同条件下气体密度最小 |
(1)用电子式写出形成F2E的过程__________________;
(2)写出CBF物质的电子式______________;
(3)C2B2物质中存在化学键的类型是___________ ,1 molC2B2与足量AB2反应转移的电子数为_______;
(4)由B、C、E形成的简单离子半径由大到小的关系是______________(用离子符号表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于铁及其化合物的说法正确的是( )
A.将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红,可以检验Fe(NO3)2晶体是否已氧化变质
B.浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
C.1 mol FeI2与足量氯气反应时转移的电子数为2NA
D.水溶液中Fe2+、H+、SO ![]() 、ClO﹣不能大量共存
、ClO﹣不能大量共存
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸盐(如Na2FeO4)已经被广泛应用在水处理方面,以铁基材料为阳极,在高浓度强碱溶液中利用电解的方式可以制备高铁酸盐,装置如图。下列说法不正确的是

A. a为阳极,电极反应式为Fe—6e- +8OH- =FeO42- +4H2O
B. 为防止高铁酸根扩散被还原,则离子交换膜为阳离子交换膜
C. 在电解过程中溶液中的阳离子向a 极移动
D. 铁电极上有少量气体产生原因可能是4OH--4e-=O2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com