
科目: 来源: 题型:
【题目】乙醇分子中不同化学键如图所示,关于乙醇在各种反应中断裂的键不正确的是( ) 
A.在Cu催化作用下和O2反应时键①⑤断裂
B.和氢溴酸共热时键②断裂
C.和金属钠反应时键①断裂
D.和浓硫酸加热到170℃,键②⑤断裂
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生利用以下装置探究氯气与氨气之间的反应,其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。请回答下列问题:

(1)装置F 为实验室制备氯气的装置,请写出实验室制备氯气的化学方程式________;
(2)装置A 中烧瓶内的固体可选用_____;装置B 中试剂可选用_____;
a.碱石灰 b.无水CuSO4 c.无水CaCl2 d.浓硫酸
(3)E 装置选用试剂的名称_____;
(4)装置C 内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。
①请写出反应的化学方程式______________;
②并用单线桥表示电子转移的方向和数目。
③当有amol氯气参加反应时,转移的电子总数为b 个,则阿伏加德罗数常数表示为______________;(用含a、b 的代数式表示,结果注明单位)
(5)通入C 装置的两根导管左边较长、右边较短,目的是______________;从装置C 的G 处逸出的尾气中可能含有黄绿色的有毒气体,请在上图右边方框中画图,表示处理该气体的方法,并标出气流方向和所用试剂的名称。_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4和H2SO4的工艺流程如下所示:

焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,氧化剂是________,氧化剂与还原剂的物质的量之比为_________
(2)从水浸后的滤液中得到K2SO4晶体的方法是____;产物K2SO4中K元素的鉴定操作过程是____。
(3)向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全的离子反应方程式为____。
(4)焙烧产生的SO2可用于制硫酸。已知25℃、l0lkPa时:
①2SO2(g)+O2(g) ![]() 2SO3(g) △H1=-197kJ·mol-1
2SO3(g) △H1=-197kJ·mol-1
②H2O(g)=H2O(l) △H2=-44kJ·mol-1
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3=-545kJ·mol-1
则SO3(g)与H2O(1)反应的热化学方程式是__________________________。
(5)假设整个过程中没有物质损失,理论上三种最终产物K2SO4,Al和H2SO4的物质的量之比为___________.
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、X、Y、Z是原子序数依次增大的短周期元素,其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子的化合物;B与Z的最外层电子数之比为2∶3;常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞溶液变红。请回答下列问题:
(1)Z 元素在元素周期表中的位置是______________ ,化合物A2X2的电子式为______________
(2)化合物A2X和A2Z中,沸点较高的是__________(填化学式),其主要原因是_____________
(3)A与X、A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为:_______
(4)将Z与X 形成的气态化合物ZX2通入Ba(NO3)2 溶液中,有白色沉淀和NO气体生成,发生反应的离子方程式为___________________
(5)两种均含A、X、Y、Z四种元素的化合物相互反应放出气体的反应离子方程式为:_________
查看答案和解析>>
科目: 来源: 题型:
【题目】绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染.下列做法不符合绿色化学理念的是( )
A.研制水溶剂涂料替代有机溶剂涂料
B.用可降解塑料生产包装盒或快餐盒
C.用反应:Cu+2H2SO4(浓) ![]() ?CuSO4+SO2↑+2H2O? 制备硫酸铜
?CuSO4+SO2↑+2H2O? 制备硫酸铜
D.用反应:2CH2=CH2+O2 ![]()
![]() 制备环氧乙烷
制备环氧乙烷
查看答案和解析>>
科目: 来源: 题型:
【题目】汉黄芩素(其结构如下图所示)是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是
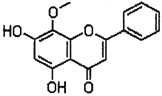
A. 汉黄芩素的分子式为C16H13O3
B. 汉黄芩素遇FeCl3溶液显色
C. lmol汉黄芩素与溴水反应,最多消耗2molBr2
D. 汉黄芩素与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.(1)按要求写出下列反应的化学方程式:
①由饱和FeCl3溶液制备Fe(OH)3胶体_______________________________。
②氢氟酸腐蚀玻璃____________________________________。
(2)按要求写出下列反应的离子方程式:
①制漂白粉(有效成分为次氯酸钙)____________________________________。
②用硫氰化钾溶液检验溶液中含有Fe3+____________________________________。
③向Ba(OH)2溶液中逐滴加入NaHSO4溶液至溶液恰呈中性____________________________________;
Ⅱ.已知还原性是I->Fe2+>Br-,1L某溶液中含有FeI2和FeBr2两种溶质,分析知其中Fe2+、I-、Br-的物质的量比为1:1:1。取出1/10体积该混合溶液向其中通入氯气,发现吸收3.36L(标况下)的氯气后溶液中的溶质离子刚好完全被氧化得到I2、Br2、Fe3+。请回答:
①试写出此反应过程中第二步反应的离子方程式__________。
②求原混合溶液中各溶质的物质的量浓度______________。
③当溶液中Br-有一半被氧化时,通入的氯气在标况下所占体积是________升,此时溶液中溶质的物质的量浓度约为(不考虑溴和碘单质的溶解)________
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组用如图装置进行乙醇催化氧化的实验. 
(1)实验过程中铜网出现黑色和红色交替的现象,请写出此过程总的化学反应方程式 .
(2)甲和乙两个水浴作用不相同,其中甲的作用是 .
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们有水和 . 集气瓶中收集到的气体的主要成分是 .
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有乙酸,要除去该物质,可先在混合液中加入(填字母序号),然后,再通过(填实验操作名称)操作即可除去.
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)的△H>0,△S>0
B. 常温下,NH4Cl溶液加水稀释 增大
增大
C. 电解饱和食盐水产生了11.2LH2,则反应中转移的电子数为6.02×1023
D. 在NaCl和KI均为0.1 mo1·L-1的混合溶液中滴加AgNO3溶液,则先产生黄色沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】将ag铁和氧化铁的混合物加入800mL0.1mol/L 的盐酸中充分反应后,盐酸全部消耗,放出标准状兄下气体0.224L。则下列判断中正确的是 ( )
A. 原混合物中n (Fe) :n (Fe2O3) =2: 1 B. 向溶液中滴入KSCN 溶液,显血红色
C. 无法计算出原混合物的质量 D. 此混合物中铁元素的质量分数为68.6%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com