
科目: 来源: 题型:
【题目】用括号内试剂除去下列各物质中的少量杂质,不正确的是
A.乙烷中的乙烯(Br2水)B.溴苯中的溴(KI溶液)
C.乙醇中的水(CaO)D.乙酸乙酯中的乙酸(饱和Na2CO3溶液)
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上用废镍催化剂(成分主要为Ni ,含有一定量的Al2O3、Fe、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
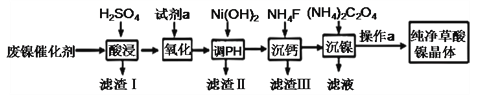
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(NiC2O4)= 4.05×1010
(1)“酸浸”前将废镍催化剂粉碎的目的是:____。“滤渣Ⅰ”的主要成分为:____。
(2)若试剂a为H2O2 ,写出氧化时反应的离子方程式:____。
(3)调节pH的范围为:____。
(4)写出“沉钙”操作中加入NH4F时发生反应的离子方程式:____,NH4F的电子式为:____。
(5)如果“沉镍”操作后测得滤液中C2O42 的浓度为0.18 mol·L1,则溶液中c(Ni2+)= ____ mol·L1。
(6)将得到的草酸镍晶体在真空中加热至320℃分解,可重新制得单质镍催化剂。该制备过程的化学方程式为:____。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于糖类、脂肪和蛋白质的叙述正确的是
A.植物油不能使溴的四氯化碳溶液褪色
B.脂肪、纤维素和蛋白质都是天然高分子化合物
C.葡萄糖能发生氧化反应和水解反应
D.淀粉溶液与稀硫酸共热后,滴加碘水不变蓝,说明淀粉已完全水解
查看答案和解析>>
科目: 来源: 题型:
【题目】鸦片最早用于药物(有止痛、止泻、止咳的作用),长期服用会成瘾,使人体质衰弱,精神颓废,寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如下:  已知该物质的燃烧产物为CO2、H2O和N2 , 1mol该化和物完全燃烧消耗的O2的物质的量及在一定条件下与Br2发生苯环取代反应生成的一溴代物的同分异构体的种数分别为( )
已知该物质的燃烧产物为CO2、H2O和N2 , 1mol该化和物完全燃烧消耗的O2的物质的量及在一定条件下与Br2发生苯环取代反应生成的一溴代物的同分异构体的种数分别为( )
A.23.25mol 5
B.24.5mol 7
C.24.5mol 8
D.23.25mol 6
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是环保部门监测有害气体常用的一种药品,它易溶于水,遇酸易分解。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图。
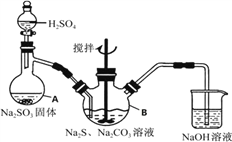
实验具体操作步骤为:
①打开分液漏斗使硫酸慢慢滴下,适当调节分液漏斗的滴速,使反应产生的SO2气体较均匀的通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体。
(1)写出仪器A的名称____。
(2)写出A中发生反应的化学方程式____。
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是____。
(4)Na2S2O3常用作脱氯剂,在溶液中易被Cl2氧化成SO42离子,该反应的离子方程式为____。
(5) 为了验证固体硫代硫酸钠工业产品中含有碳酸钠,选用下图装置进行实验。
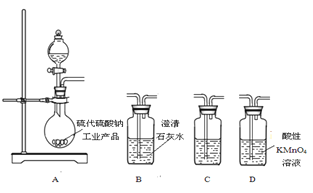
①实验装置的连接顺序依次是____(填装置的字母代号),装置C中的试剂为____。
②能证明固体中含有碳酸钠的实验现象是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质与条件己略去)。已知A、C由两种相同元素組成的物质,其A摩尓质量为65g/mol,C是白色粉末且焰色反应呈黄色,I是最常见的液体,E是一种红棕色气体,B、F都是无色气体单质。
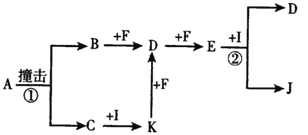
(1)E的化学式为________。
(2)C的电子式为_________。
(3)用电子式表示I的形成辻程________。
(4)写出反应①的化学方程式________。
(5)写出反应②的离子方程式________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用海水可以提取溴和镁,提取过程如下:

(1)提取溴的过程中,经过2次Br-→Br2转化的目的是________,吸收塔中发生反应的离子方程式是________________。
(2)据上述流程,将10m3海水中溴元素(海水中Br-离子含量为64mg/L)转化为工业溴,整个流程中至少需要标准状况下Cl2的体枳为______L(忽略Cl2溶解)。
(3)从理论上考虑,下列物质也能吸收Br2的是_____。
A.H2O B.FeCl2 C.Na2SO3
(4)由无水氯化镁得到镁的化学方程式是_______。
(5)有同学认为:可以加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,以简化实验步骤,体现实验的简约性原则,你是否同意该同学的观点,理由为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=l.1×10-12以及Ksp[Cu(OH)2] =2×10-20。下列说法错误的是
A. 常温下AgCl饱和溶液和Ag2CrO4饱和溶液的物质的量浓度比较:c(AgCl)<c(Ag2CrO4)
B. 常温下,在0.010molL-1的AgNO3溶液中,AgCl与Ag2CrO4分别能达到的最大物质的量浓度比较:c(AgCl)<c(Ag2CrO4)
C. 某CuSO4溶液里c(Cu2+)=0.02 molL-1,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于5
D. 要使0.2molL-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液PH为6
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)硫酸被人们誉为“化学工业之母”,在国民生产中发挥着重要作用。硫酸的性质有:A.高沸点;B.强酸性;C.吸水性;D.脱水性;E.强氧化性。在下列硫酸的用途或化学反应中,硫酸可能表现上述的一个或者多个性质,试用字母填空:
①硫酸可用作气体干燥剂___________;
②往晶体硫酸铜中加液硫酸,晶体变白___________;
③浓硫酸使湿润蓝色石蕊试纸先变红后又变黑___________;
④浓硫酸使蔗糖变黑,且有刺激性气味的气体产生___________;
⑤浓硫酸与FeO反应____________;
⑥运用铁制槽车和铝制槽车送输浓硫酸___________。
(2)“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。煤燃烧排放的烟气含有SO2和NOx,形成酸雨,汚染大气,采用NaClO2溶液在碱性条件下可对烟气迸行脱硫、脱硝,效果非常好。
①完成下列对烟气脱硝过程的离子方程式
___C1O2-+__NO+____=Cl-+____NO3-+______。
②SO2有多种处理方式,写出用过量氨水吸收尾气的离子方程式:_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定质量的铜片加入到20 mL某浓度的浓硝酸中,充分反应后,铜片全部溶解,并收集到标准状况下的混合气体共896mL(假设[体中只有NO和NO2)。向反应后所得溶液中逐滴滴加lmol/L的NaOH溶液,产生沉淀质量与加入NaOH溶液体积(单位: mL)的关系如图所示。回答下列问题:
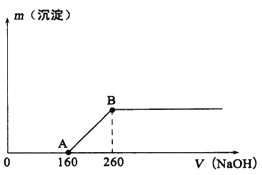
(1)B点所表示溶液中只含一种溶质,该物质是______(填化学式)。
(2)收集的气体中,NO2的物质的量为_______mol。
(3)原浓硝酸的浓度为_______mol/L。
(4)欲使铜与硝酸产生的混合气体在氢氧化钠溶液中全部转化为硝酸钠,至少需要30%的双氧水______g(保留两位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com