
科目: 来源: 题型:
【题目】同周期的X、Y、Z三种元素,已知最高价氧化物的水化物的酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断错误的是
A. 非金属性: X>Y>Z
B. 气态氢化物的稳定性: HX>H2Y>ZH3
C. 原子半径: X>Y>Z
D. 阴离子的还原性: ![]() > X-
> X-
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是
A. ![]() 、
、![]() 、
、![]() 、H+和H2是氢元素的五种不同粒子
、H+和H2是氢元素的五种不同粒子
B. 石墨和金刚石互为同位素,化学性质相似
C. ![]() 和
和![]() 是不同的核素
是不同的核素
D. 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
查看答案和解析>>
科目: 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)NaClO2中氯元素的化合价为______________。
(2)在鼓泡反应器中通入含有SO2和NOx的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol/L,溶液呈碱性。反应一段时间后溶液中离子浓度的分析结果如下表
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol/L) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①以NO转化为NO3-为例,写出NaClO2溶液脱硝过程中主要反应的离子方程式__________。增加压强,NO的转化率__________(填“提高”“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐___________(填“提高”“不变”或“降低”)。
③由实验结果可知,脱硫反应速率脱硝反应速率__________(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是________________________________。
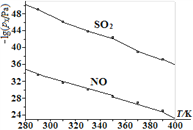
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压px如图所示。已知图中: ![]() 其中(nx代表各成分的物质的量,na代表气体总物质的量)
其中(nx代表各成分的物质的量,na代表气体总物质的量)
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均____(填“增大”“不变”或“减小”)。
②反应ClO2+2SO32==2SO42+Cl的平衡常数K表达式为______________。
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为200 mL,回答下列问题:

(1)电源F是__________极;
(2)A池的第②极上的电极反应式_________
(3)通电前A池中原混合溶液Cu2+的浓度________
查看答案和解析>>
科目: 来源: 题型:
【题目】温度会影响微生物的生存和繁殖.下表为大肠杆菌在不同温度下繁殖l代所用的时间(min).根据表格可直接得出哪项结论( )
温度 | 10℃ | 15℃ | 20℃ | 25℃ | 30℃ | 35℃ | 40℃ | 45℃ | 50℃ | ||
时间 | 860 | 120 | 90 | 40 | 29 | 22 | 1 | 5 | 2 | 0 | 80 |
A.10℃时细菌繁殖最快 B.温度越高酶活性越强
C.低温可抑制细菌繁殖 D.酶的活性受时间控制
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2:1和1:1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是______________
(2)C、B可按原子个数比1:1形成离子化合物乙的电子式___________
(3)C、D、E三种元素的离子半径由小到大的顺序是____________(用元素符号填写)。
(4)E单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是:____________________
(5)简述比较D与E金属性强弱的实验方法:_______________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量,则下列热化学方程式中正确的是( )
A.2CH4(g)+4O2(g)═2CO2(g)+4H2O(l);△H═+890KJ/mol
B.CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H═+890KJ/mol
C.CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H═﹣890KJ/mol
D.2CH4(g)+4O2(g)═2CO2(g)+4H2O(l);△H═﹣890KJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)CH3OH(g)
(1)判断反应达到平衡状态的依据是(填字母序号,下同) .
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)下表所列数据是反应在不同温度下的化学平衡常数(K).
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断该反应的△H0(填“>”、“=”或“<”);
②某温度下,将2molCO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为 , 此时的温度为 .
(3)要提高CO的转化率,可以采取的措施是 . a.升温b.加入催化剂c.增加CO的浓度
d.加入H2加压e.加入惰性气体加压f.分离出甲醇
(4)一定条件下,CO与H2在催化剂的作用下生成5molCH3OH的能量变化为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 | |
反应物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
平 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | a kJ | b kJ | c kJ | |
体系压强(Pa) | p1 | p2 | p3 | |
反应物转化率 | α1 | α2 | α3 | |
下列说法正确的是 .
A.2c1>c3
B.a+b<90.8
C.2p2<p3
D.α1+α3<1.
查看答案和解析>>
科目: 来源: 题型:
【题目】控制变量是科学研究的重要方法。相同质量的铁粉与足量稀硫酸分别在下列条件下发生反应,其中反应速率最快的是
A | B | C | D | |
t/℃ | 10 | 10 | 40 | 40 |
c(H2SO4 )/(mol/L) | 1 | 3 | 1 | 3 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com