
科目: 来源: 题型:
【题目】I.被誉为改变未来世界的十大新科技之一的燃料电池。 右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.

试回答下列问题:
(1)燃料电池的优点是________;电解质溶液中的OH-移向______极(填“负”或“正”).
(2)写出氢氧燃料电池工作时正极反应式:_______________________。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________.
(4)利用该装置可以处理氮的氧化物和NH3 尾气,总反应为:6NO2 +8NH3=7N2+12H2O,负极反应式为__________。
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为________________;
(2)通过导线的电子数为__________(用NA表示).
查看答案和解析>>
科目: 来源: 题型:
【题目】已知正四面体形分子E和直线型分子G反应,生成四面体形分子L和直线型分子M.(组成E分子的元素的原子序数小于10,组成G分子的元素为第三周期的元素.)如图,则下列判断中正确的是( ) 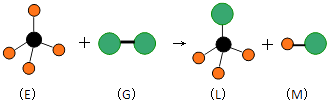
A.常温常压下,L是一种液态有机物
B.E是一种含有非极性键的分子
C.干燥的G 能漂白有色物质
D.上述反应的类型是取代反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在生物体内含量很少,但必不可少的微量元素有( )
A. Fe Mn Zn Mg
B. Zn Cu Mn Ca
C. H O Na Mg
D. Zn Cu B
查看答案和解析>>
科目: 来源: 题型:
【题目】
A. 组成生物的最基本元素是C
B. 占人体细胞干重百分比最多的元素是O
C. H7N9病毒和桃树共有的元素是C、H、O、N、P
D. Cu、Mn、Mo、B都是组成生物体的微量元素
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示(乙装置中X为阳离子交换膜,甲醚的结构简式为CH3OCH3) 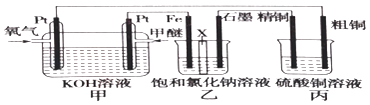
根据要求回答下列相关问题:
(1)写出负极的电极反应: .
(2)氢氧化钠主要在(填“铁极”或“石墨极”)区生成.
(3)如果粗铜中含有锌、银等杂质,则粗铜的电极反应为:、 .
(4)反应一段时间,硫酸铜溶液的浓度将(填“增大”、“减小”或“不变”).
(5)若在标准状况下有2.24L氧气参加反应,丙装置中阴极析出铜的质量为 .
(6)若将丙装置改成在标准状况下,用石墨作电极电解体积为2L的CuSO4溶液,写出电解CuSO4溶液时的离子反应方程式;当电解适当时间后断开电源,发现只需补充22.2g固体Cu2(OH)2CO3即可使电解液恢复到原浓度与体积,则原CuSO4溶液的浓度是mol/L;若将丙设计成在镀件上镀铜的装置,该如何改动,请用简要的语言叙述: .
(7)若将乙中的交换膜去掉,发现只有H2逸出,则试写出乙池中发生的总反应: .
查看答案和解析>>
科目: 来源: 题型:
【题目】以天然气为原料合成甲醇,有关热化学方程式如下:
①2CH4(g)+O2(g)==2CO(g)+4H2(g) △H1=-70.8kJmol-1
②CO(g)+2H2(g)![]() CH3OH(g) △H2
CH3OH(g) △H2
③2CH4(g)+O2(g)![]() 2CH3OH(g) △H3=-251.0 kJmol-1
2CH3OH(g) △H3=-251.0 kJmol-1
(1)反应②的△H2=________kJmol-1;
(2)在体积可变的密闭在器中投入1 mol CO和2 mol H2,在不同条件下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。实验测得平衡时CH3OH的物质的量随温度、压强变化如图1所示。
CH3OH(g)。实验测得平衡时CH3OH的物质的量随温度、压强变化如图1所示。

①M 点时,H2 的转化率为_________;压强: p1_______(填“>”“<”或“=”)p2;
②反应速率:N 点v正(CO) _______(填“>”“<”或“=”)M 点v 逆(CO)
③若压强为p1、在1L恒容密闭容器中进行上述反应(起始投料不变),在不同温度下上述反应的平衡常数的对数(IgK)如图2所示。则温度为506K时,平衡常数K=____________, B、C、D、E四点中能正确表示该反应的1gK 与T的关系的点为________________。
④若在2L恒容密闭容器中充入x (x>0)mol H2、2 mol CO、和8 mol CH3OH(g),在 506 K下进行上述反应。为了使该反应逆向进行,x的范围为________________。
(3)某甲醇-空气燃料电池以KOH溶液为电解质溶液。当KOH全部转化成KHCO3时停止放电,写出此时负极的电极反应式______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物G(1,6-己二酸)是合成尼龙的主要原料之一,可由烃A制备,合成路线如图1,烃A的质谱图如图2,回答下列问题:


(1)A的化学名称为________,D的官能团名称为__________________。
(2)A→B的反应类型是______________,F→G的反应类型是_______________。
(3)F的结构简式为___________________________。
(4)若H2NRNH2为已二胺,则由G合成尼龙的反应方程式为_____________________________。与G含有相同官能团的同分异构体共有__________种,其中核磁共振氢谱为4组峰,且峰面积比为1∶1∶2∶6的结构简式是______________(写出一种即可)。
(5)由A通过两步反应制备1,3-环己二烯的合成路线为______________________。(其它试剂任选)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com