
科目: 来源: 题型:
【题目】下图为生锈了的家用铁锅,下列有关解释事实的方程式不正确的是

A. 铁锅生锈过程中有原电池反应,负极反应式是:Fe—2e—= Fe2+
B. 铁锅生锈过程中有 Fe(OH)3生成:Fe3+ + 3H2O![]() Fe(OH)3 + 3H+
Fe(OH)3 + 3H+
C. 摄入体内的铁锈会在胃内产生不利于健康的Fe3+:Fe2O3 + 6H+=2Fe3++3H2O
D. 用醋可除去铁锈:6CH3COOH + Fe2O3 =6CH3COO—+ 2Fe3+ + 3H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】H2在Cl2中燃烧的方程式为:H2 + Cl2 ![]() 2HCl,已知在相同条件下,有下图所示的能量变化,下列说法中正确的是
2HCl,已知在相同条件下,有下图所示的能量变化,下列说法中正确的是
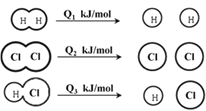
A. H2、Cl2和HCl分子中的化学键都是非极性共价键
B. 1 mol H2与1 mol Cl2的总能量小于2 mol HCl的总能量
C. 1molH2与1molCl2反应生成2 mol HCl时,反应放出的能量为:2Q3-Q1 -Q2
D. 1molH2与1molCl2反应生成2 mol HCl的过程中:Q1+ Q2 >2Q3
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W、M 为原子序数依次增大的短周期主族元素。已知:①元素对应的原子半径大小为:X<Z<Y<M<W;② Y 是组成有机物的必要元素 ③ Z 与 X 可形成两种常见的共价化合物,与 W 可形成两种常见的离子化台物;④ M 的电子层数与最外层电子数相等。下列说法不正确的是
A. W、M 的原子半径为 M<W
B. YZ2为直线形的共价化合物,W2Z2既含有离子键又含有共价键
C. Z 与 X 形成的化合物的熔沸点偏高是因其分子内存在氢键
D. Z 与 M 形成的化合物可作为耐高温材料
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,可逆反应X(g)+ 3Y(g)![]() 2Z(g)达到平衡的标志是
2Z(g)达到平衡的标志是
A. Z生成的速率与X消耗的速率相等
B. 单位时间生成a mol X,同时生成3a mol Y
C. X、Y、Z的浓度不再变化
D. X、Y、Z的分子数比为1∶3∶2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列措施能明显增大原反应的化学反应速率的是
A. C(s)+ CO2 ![]() 2CO反应中,增大C的量
2CO反应中,增大C的量
B. 将稀H2SO4改为98%的浓H2SO4与Zn反应制取H2
C. 在H2SO4与NaOH两溶液反应时,增大压强
D. 恒温恒容条件下,在工业合成氨反应中,增加氮气的量
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.2,2﹣二甲基﹣1﹣丁醇与2﹣甲基﹣2﹣丁醇互为同分异构体
B.![]() 的核磁共振氢谱有5个峰
的核磁共振氢谱有5个峰
C.根据核磁共振氢谱能鉴别1﹣溴丙烷和2﹣溴丙烷
D.用KMnO4酸性溶液能鉴别CH3CH═CHCH2OH和CH3CH2CH2CHO
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物a的分子式和己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是( )
A.a分子中可能有三个甲基
B.a的分子式为C6H10
C.a的一氯代物可能有三种
D.a能与溴的四氯化碳溶液发生取代反应
查看答案和解析>>
科目: 来源: 题型:
【题目】电解质溶液与人类生活息息相关,请回答下列问题
(1)某温度下,Kw=1×10﹣12( molL﹣1)2 , 若保持温度不变,向水中滴入稀硫酸恰好使溶液中c(H+)/c(OH﹣)=1×1010 , 则此时水电离出的c(H+)=molL﹣1 .
(2)常温下若溶液由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2 mL混合而得,则下列说法正确的是 .
A.若混合后溶液呈中性,则c(H+)+c(OH﹣)=2×10﹣7mol/L
B.若V1=V2 , 混合后溶液的pH一定等于7
C.若混合后溶液呈酸性,则V1一定大于V2
D.若混合后溶液呈碱性,则V1一定小于V2
(3)下列曲线中,可以描述乙酸(甲,Ka=1.8×10﹣5 mol/L)和一氯乙酸(乙,Ka=1.4×10﹣3 mol/L)在水中的电离度与浓度关系的是 . 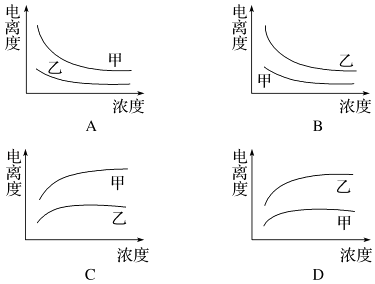
(4)在下列实验中,能证明醋酸酸性比盐酸酸性弱的是 .
A.将等体积、pH=4的盐酸和醋酸稀释成pH=5的溶液,测量所需加入水量的多少
B.向等体积、等pH的盐酸和醋酸中分别加入同量的相应钠盐固体,测溶液的pH有无变化
C.向等体积、等浓度的盐酸和醋酸分别加入足量锌粉,测量产生氢气的体积
D.用等体积、等浓度的盐酸和醋酸做导电性实验,根据灯泡的明亮程度.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com