
科目: 来源: 题型:
【题目】1g氢气燃烧生成液态水放出142.9kJ的热量,表示该反应的热化学方程式正确的是( )
A.2H2(g)+O2(g)═2H2O(l)△H=﹣142.9 kJmol﹣1
B.H2(g)+ ![]() O2(g)═H2O(l)△H=﹣285.8 kJmol﹣1
O2(g)═H2O(l)△H=﹣285.8 kJmol﹣1
C.2H2+O2═2H2O△H=571.6 kJmol﹣1
D.H2(g)+ ![]() O2(g)═H2O(g)△H=﹣285.8 kJmol﹣1
O2(g)═H2O(g)△H=﹣285.8 kJmol﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】在细胞内含量极少,但对维持生命活动必不可少的元素有( )
A.Fe Mn Zn Mg B.Zn Cu Mg Ca
C.Zn Cu B Mn D.Mg Mn Cu Mo
查看答案和解析>>
科目: 来源: 题型:
【题目】我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。研究发现,青铜器在潮湿环境中发生电化学腐蚀的原理示意图如下,下列说法正确的是

A. 腐蚀过程中,青铜基体是正极
B. CuCl在腐蚀过程中降低了反应的焓变
C. 若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为0.448L
D. 将糊状Ag2O涂在被腐蚀部位,可以防止青铜器进一步被腐蚀,Ag2O与催化层发生复分解反应
查看答案和解析>>
科目: 来源: 题型:
【题目】已知气态烃A的密度是相同状况下氢气密度的14倍,有机物A~E能发生下图所示一系列变化,则下列说法错误的是
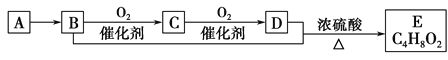
A. A分子中所有原子均在同一平面内
B. C4H8O2含酯基的同分异构体有4种
C. C的水溶液又称福尔马林,具有杀菌、防腐性能
D. 等物质的量的B、D与足量钠反应生成气体的量相等
查看答案和解析>>
科目: 来源: 题型:
【题目】将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。
(1)Cu2+基态核外电子排布式为________________________;[Cu(NH3)4]SO4·H2O中,不考虑空间构型,[Cu(NH3)4]2+的结构可用示意图表示为___________。
(2)乙醇分子中C原子轨道杂化类型为___________,H2O与H+以配位键形成H3O+,则H3O+的空间构型为__________(用文字描述)。
(3)N、O、S第一电离能由大到小的顺序为____________________。
(4)某含有结晶水的铜的氯化物的晶胞结构如图所示,该化合物的化学式是________。
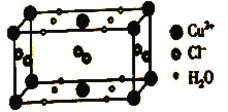
查看答案和解析>>
科目: 来源: 题型:
【题目】为保护环境,应减少二氧化硫、氮氧化物和二氧化碳等物质的排放量。
(1)用CH4催化还原煤燃烧产生的氮氧化物,可以消除污染。
已知:CH4(g) + 2NO2(g)=N2(g) +CO2(g) + 2H2O(g) △H=-867.0 kJ/mol
NO2(g)=![]() N2O4(g) △H=-28.5 kJ/mol
N2O4(g) △H=-28.5 kJ/mol
写出CH4催化还原N2O4(g)生成CO2、N2和H2O(g)的热化学方程式 。
(2)一定条件下,将NO2与SO2以体积比1∶2置于恒温恒容的密闭容器中,发生NO2(g)+SO2(g)![]() SO3(g)+NO(g),测得反应达到平衡时NO2与SO2体积比为1∶5,则平衡常数K= (填数值)。
SO3(g)+NO(g),测得反应达到平衡时NO2与SO2体积比为1∶5,则平衡常数K= (填数值)。
(3)如图1是一种用NH3、O2脱除烟气中NO的原理,该原理中NO最终转化为H2O和 (填化学式),当消耗1mol NH3和0.5molO2时,除去的NO在标准状况下的体积为 L。

(4)研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。有人利用图2所示装置(均为惰性电极)从海水中提取CO2(海水中无机碳95 % 以HCO3-存在),有利于减少环境中温室气体含量。
①a室的电极反应式为 。
②b室中提取CO2的反应的离子方程式为 。
③b室排出的海水(pH<6)不可直接排回大海,需用该装置中产生的物质对b室排出的海水进行处理,合格后才能排回大海。处理的方法是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】汽车尾气中含有CO、NO等有害气体。
(1)汽车尾气中NO生成过程的能量变化示意图如下:
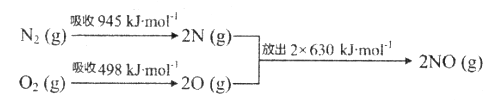
该条件下,1mol N2和1molO2完全反应生成NO,会_______________(填“吸收”或“放出”)________kJ能量。
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如下图所示:
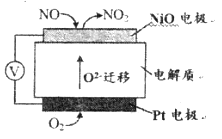
①NiO电极上发生的是_______________反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从_______电极流向______电极(填“NiO”或“Pt”);Pt电极上的电极反应式为_______________。
(3)一种新型催化剂能使NO和CO发生反应:2NO+2CO ![]() 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
实验 编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | 280 | 1.20×10-3 | B | 124 |
Ⅲ | 350 | A | 5.80×10-3 | 82 |
①请把表中数据补充完整:A_______________;B_______________。
②能验证温度对化学反应速率影响规律的是实验_______________(填实验序号)。
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如下图所示,其中表示实验Ⅱ的是曲线_________(填“甲”或“乙”)。
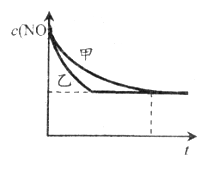
查看答案和解析>>
科目: 来源: 题型:
【题目】谢弗勒尔盐(Cu2SO3·CuSO3·2H2O)是一种深红色固体,不溶于水和乙醇,100℃时发生分解。可由CuSO4·5H2O和SO2等为原料制备,实验装置如下图所示:

(1)装置A在常温下制取SO2时,用较浓的硫酸而不用稀硫酸,其原因是_______________。
(2)装置B中发生反应的离子方程式为_______________。
(3)装置C的作用是____________________。
(4)从B中获得的固体需先用蒸馏水充分洗涤,再真空干燥。
①检验洗涤已完全的方法是__________________。
②不用烘干的方式得到产品,其原因是________________。
(5)请补充完整由工业级氧化铜(含少量FeO)制备实验原料(纯净CuSO4·5H2O)的实验方案:向工业级氧化铜中边搅拌边加入稍过量的硫酸溶液,微热使其完全溶解,_______________,过滤,用95%酒精洗涤晶体2~3次,晾干,得到CuSO4·5H2O。
[已知:①该溶液中氢氧化物开始沉淀与沉淀完全时的pH范围分别为:Fe(OH)2(5.8,8.8);Cu(OH)2(4.2,6.7);Fe(OH)3(1.1,3.2)。②在水溶液中超过100℃,硫酸铜晶体易失去结晶水。③硫酸铜晶体溶解度曲线如右图所示]

查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组的同学用下图所示装置进行氯气的性质实验。
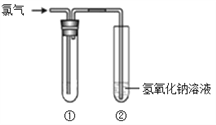
请回答:
(1)若要得到干燥的氯气,则①中所加的试剂应为_____。
(2)若①中盛放的是湿润的红纸条,则观察到的现象为_____。
(3)若①要验证氯气具有氧化性,则所用的溶液不能是_____(填序号)。
a. FeCl2 b. 溴水 c. KI溶液
(4)装置②中反应的离子方程式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应:2HI(g) ![]() H2(g)+I2(g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
H2(g)+I2(g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
A.HI、H2、I2的浓度相等
B.HI、H2、I2的浓度不再发生变化
C.HI、H2、I2在密闭容器中共存
D.容器内气体的颜色不再发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com