
科目: 来源: 题型:
【题目】2005年10月12日北京时间上午9时,中国酒泉卫星发射中心成功将“神舟6号”飞船送入太空,这一壮举又一次受到世界关注.火箭推进器中有强还原剂液体肼(N2H4)和强氧化剂液态双氧水.当它们混合时,即产生大量氮气和水蒸气并放出大量热.已知:0.4mol液态肼与足量的液态双氧水反应生成氮气和水蒸气,放出256.652kJ的热量.
(1)反应的热化学方程
(2)又已知H2O(l)=H2O(g)△H=44kJ.mol﹣1 . 则16g液态肼与足量的液态双氧水反应生成氮气和液态水时放出的热量是kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外还有一个很大优点是 .
(4)燃料电池在航天器得到大量应用;科研人员新近开发出一种由甲醇、氧气以及强碱作电解质溶液的新型手机电池,充电一次可供手机连续使用一个月,据此请回答以下问题:
①甲醇是极,电极反应
②电池反应的离子方程式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
(1)氨气的制备

①氨气的发生装置可以选择上图中的________,反应的化学方程式为______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中_____________ | ②反应的化学方程式 ____________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③_______________ | ④______________ |
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中A与B反应生成C,其反应速率分别用v(A),v(B),v(C)表示,已知v(A),v(B),v(C)之间有以下关系3v(A)=2v(B),3v(C)=2v(B),则此反应可表示为( )
A.2A+3B=2C
B.A+3B=2C
C.3A+B=2C
D.A+B=C
查看答案和解析>>
科目: 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径如图所示。下列说法正确的是![]()

A. 途径①所用混酸中H2SO4与HNO3物质的量之比最好为2:3
B. 利用途径③制备16g硫酸铜,消耗硫酸的物质的量为0.1mL
C. 生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量:①=②=③
D. 与途径①、③相比,途径②更好地体现了绿色化学思想
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用氯碱工业中的固体废物盐泥(主要成分为Mg(OH)2、CaCO3、BaSO4,除此之外还有NaCl、Al(OH)3、Fe(OH)3、Mn(OH)2等。)与废稀硫酸反应制备七水硫酸镁,产率高,既处理了三废,又有经济效益。其工艺流程如下:
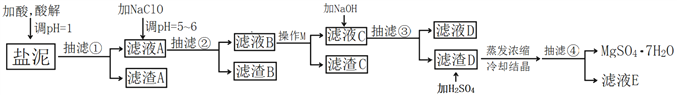
已知:
i)部分阳离子以氢氧化物形式完全沉淀时溶液的pH
沉淀物 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
pH值(完全沉淀) | 10.02 | 8.96 | 3.20 | 4.70 | 11.12 |
ii)两种盐的溶解度图(单位为g/100g水)

根据以上流程图并参考表格pH数据和溶解度图,请回答下列问题。
(1)酸解时,加入的酸为____________,在酸解过程中,想加快酸解速率,请提出两种可行的措施____________、____________。
(2)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是____________。
(3)本工艺流程多次用到抽滤操作,其优点在于____________,四次抽滤时:抽滤①所得滤渣A的成分为____________、CaSO4;抽滤②所得滤渣B的成分为MnO2、____________、____________;抽滤③所得滤液C中主要杂质阳离子的检验方法是____________;抽滤④将产品抽干。
(4)依据溶解度曲线,操作M应采取的方法是适当浓缩,____________。
(5)每制备1吨MgSO4·7H2O,需要消耗盐泥2吨。若生产过程中的转化率为70%,则盐泥中镁(以氢氧化镁计)的质量分数约为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】1828年,德国化学家弗里德里希·维勒首次使用(NH4)2SO4与氰酸钾KCNO人工合成了尿素CO(NH2)2,打破了有机化合物的"生命力"学说。
(1) (NH4)2SO4与KCNO合成尿素反应的化学方程式为____________。
(2)某小组同学在实验室条件下,拟用CO2和NH3,在催化剂的作用下合成尿素。
①用CO2和NH3合成尿素 CO(NH2)2反应的化学方程式为____________。
②实验所需的CO2可用多种装置来制备,要想达到“随开随用、随关随停”的目的,下列装置A、B、C、D、E中符和要求的有____________(填字母)。
③若用F装置收集氨气,则气体应由导管口____________(填“a”或“b”)进入。




(3)尿素样品中氮含量可以用甲醛法标定,其原理如下:首先用浓硫酸分解试样,使试液中的胺生成硫酸铵并放出二氧化碳;将过量的硫酸中和后得到中性铵盐,再用甲醛(HCHO)与硫酸铵作用生成六次甲基四铵盐离子(CH2)6N4H+和硫酸;最后用标准氢氧化钠溶液滴定。
①甲醛与硫酸铵反应的离子方程式为____________;
②滴定选用的指示剂为____________。滴定终点的现象为____________。
③若称取样品m g,溶解后配成250mL溶液。取25.00mL样品溶液于250 mL锥形瓶中,加入10mL w%的甲醛溶液,充分反应后,加入1~2滴指示剂,用浓度为a mol/L的NaOH标准溶液滴定至终点(已知滴定时,1 mol六次甲基四铵盐离子(CH2)6N4H+消耗OH﹣的能力与1mol H+相当)。重复2次,消耗NaOH标准溶液的体积平均值为b mL。则该样品中氮的质量分数为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于常见化学物质的应用不正确的是( )
A.干冰能用作冷冻剂
B.明矾可用作净水剂
C.味精可用作食品调味剂
D.苏打是一种膨松剂,可用于制作馒头和面包
查看答案和解析>>
科目: 来源: 题型:
【题目】电动汽车以锂电池提供动力,锂电池技术已经成为汽车研究的前沿科技某锂电池的电池反应为:xLi+Li3-xNiCoMnO6![]() Li3NiCoMnO6,下列说法正确的是
Li3NiCoMnO6,下列说法正确的是![]()
A. 该电池的充、放电过程互为可逆反应
B. 放电时,电池的负极反应为Li-e-=Li+
C. 放电过程中,Li+向电池的负极移动
D. 该电池可以采用醋酸、乙醇等作为电解质溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组互为同分异构体的是![]()
A. 35Cl和37Cl B. CH3CH2OH和CH3OCH3
C. CH3CH3和CH3CH2CH3 D. H2O和H2O2
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是![]()
A. 容器内压强不随时间变化
B. v正(X) =v逆(Z)
C. 容器内X、Y、Z的浓度之比为l:2:2
D. 单位时间内消耗0.1molX的同时生成0.2molZ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com