
科目: 来源: 题型:
【题目】在人口居住密度较大的城区和建筑群中,室内空气的污染有时会比室外更严重.下列室内空气污染物中属于无机物的是( )
A.甲醛(HCHO)
B.苯(C6H6)
C.甲苯(C7H8)
D.一氧化碳(CO)
查看答案和解析>>
科目: 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.得到的废液中含有Fe2+、Cu2+、Fe3+和Cl﹣.为回收铜并得到纯净的FeCl3溶液,下面是综合利用的主要流程:
(1)FeCl3溶液和铜反应的离子方程式为__。
(2)上述方框内物质A和X的化学式:A__,X__。上述流程中有关Fe2+和Fe3+相互转化的离子方程式是__、__。
查看答案和解析>>
科目: 来源: 题型:
【题目】由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A.②④⑤③①B.③②④①⑤C.③④②⑤①D.②④③⑤①
查看答案和解析>>
科目: 来源: 题型:
【题目】在体积恒定的密闭容器中,一定量的SO2与1.25molO2在催化剂作用下加热到600℃发生反应:2SO2(g)+O2(g) ![]() 2SO3(g)△H<0 。30s气体的物质的量减少0.45mol时反应达到平衡,在相同的温度下测得气体压强为反应前的80%。下列有关叙述正确的是
2SO3(g)△H<0 。30s气体的物质的量减少0.45mol时反应达到平衡,在相同的温度下测得气体压强为反应前的80%。下列有关叙述正确的是
A. 达到平衡时,气体的密度是反应前的80%
B. 将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量为209.7g
C. 该温度下的平衡常数为101.25L/moL
D. 0~30s时SO3生成速率为3.0×10-2mol/(L.s)
查看答案和解析>>
科目: 来源: 题型:
【题目】【选修5——有机化学基础】以芳香族化合物A和有机物D为原料,制备异戊酸薄荷醇酯(M)和高聚物(N)的一种合成路线如下图所示(部分反应条件已省略):

已知: I.A→B的原了利用率为100%;
II. ![]() (R1、R2表示氢原子或烃基)。
(R1、R2表示氢原子或烃基)。
请回答下列问题:
(1)用系统命名法对G命名,其化学名称为______________________。
(2)E的结构简式为____________________________。
(3)A→B的反应类型为_______。B分子中最多有____个原子共平面。
(4)C+G→M的化学方程式为_____________________________________。
(5)同时满足下列条件的B的同分异构体有______种(不考虑立体异构)。
①苯环上连有两个取代基 ②能发生银镜反应
(6)参照上述合成路线和信息,以苯乙烯为原料(无机试剂任选),设计制备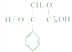 的合成路线______。
的合成路线______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某含氧有机化合物X,其相对分子质谞为46,其中碳元素的质量分数为52.2%,氢元素的质量分数为13.0%。 X可与金属钠反应放出氢气。请回答下列问题:
(1)X的结构简式为________。
(2)X与酸性K2Cr2O7溶液反应可生成Z,在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,若120 g X和150 g Z反应能生成106 g W,计算该反应的产率__________ (产率=实际产量/理论产量×100%,结果保留到小数点后一位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】【选修3——物质结构与性质】B、C、N、Si是几种常见的重要非金属元素,其形成的各种化合物在自然界中广泛存在。
(1)基态硅原子的电子排布式为________________________________。
B、C、N元素原子的第一电离能由大到小的顺序为______________________。
(2)BF3与一定量的水可形成如图所示晶体R。
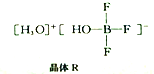
①晶体R中各种微粒间的作用力涉及___________(填字母代号)。
a.离子键 b.共价键 C.配位键 d.金属键 e.范德华力
②晶体R中阴离子的空间构型为___________________________。
(3)乙二胺(H2NCH2CH2NH3)与CuCl2溶液可形成配离子(结构如图所示),乙二胺分子中氮原子的杂化类型为_______。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的佛点高得多,其原因是_______。
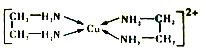
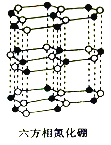
(4)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。它的晶体结构如图所示。六方相氮化硼是否含有π键?______(填“含”或“不含”),其质地软的原因是________________________________________,该物质能否导电?____________(填“能”或“不能”),其原因是______________________________。
(5)SiC是原子晶体,其晶胞结构类似金刚石,假设正方体的边长为acm,估算SiC晶体的密度为______ g·cm-3(用含NA、a的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用硫酸铝酸性溶液制备可溶性的碱式硫酸铝[Ala(SO4)b(OH)c],并用它对烟气进行脱硫处理的过程如图1: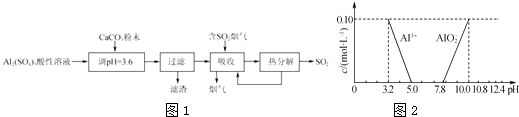
(1)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Ala(SO4)b(OH)c . 过滤时所用的玻璃仪器有、和烧杯,滤渣的主要成分为(填化学式).
(2)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将(填“增大”“减小”或“不变”).
(3)Ala(SO4)b(OH)c中a、b、c的代数关系式为 .
(4)已知在常温下溶液中Al3+、AlO2﹣的浓度与溶液pH的关系如图2所示.为确定碱式硫酸铝的组成,进行如下实验:
①取2.18g碱式硫酸铝样品在空气中灼烧至恒重,样品质量减少了0.36g.
②另取2.18g碱式硫酸铝溶于水,调节溶液的pH到5.0~7.8.
③将②产生的沉淀过滤、洗涤、灼烧至恒重,称量剩余固体为1.02g.
请计算样品中Al3+和SO42﹣的物质的量之比(写出计算过程).
查看答案和解析>>
科目: 来源: 题型:
【题目】材料的不断发展可以促进社会的进步.
①“天宫二号”内大量使用了碳纤维复合材料,在碳纤维复合材料中,碳纤维属于(填“增强材料”或“基体材料”);资源舱大量采用铝锂合金,选用铝锂合金而不选用铁合金的主要原因是 .
②“天宫二号”姿控系统使用耐辐照石英玻璃作为光学材料,石英玻璃主要成分的化学式为 .
③聚乙烯塑料常用于食品包装,聚乙烯的结构简式为 , 聚乙烯塑料属于(填“热固性”或“热塑性”)塑料.
④2015年某研究机构用一种新材料镍纳米粒子作催化剂,将二氧化碳和氢气在加热条件下转化为甲烷,该反应的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com