
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,请按要求回答问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中元素______的非金属性最强,元素_____的金属性最强(填元素符号)。
(2)表中元素③的原子结构示意图______;元素⑨形成的氢化物的电子式___________。
(3)表中元素④、⑨形成的氢化物的稳定性顺序为_____> (填化学式)。
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为_____> (填化学式)。
(5)表中元素③、④、⑥、⑦的原子半径大小为____> > > (填元素符号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列化学方程式,并指出反应类型:
(1)CH4与Cl2光照生成CH3Cl__________________________________,反应类型________。
(2)乙烯与水反应_________________________________________,反应类型__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据以下信息回答有关问题:
I.NOx是汽车尾气的主要污染物之一。
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:

该反应的△H=________________________。
(2)科学家通过实验发现,在紫外线照射下TiO2会使空气中的某些分子产生活性基团OH,并且活性基团OH可与NO2、NO发生反应生成硝酸和水。根据左下图示,请写出OH与NO反应的化学方程式______________________________________。

(3)电解法可将工业废气中含有的NO2消除。原理是先将NO2转化为N2O4,然后电解得到N2O5 (常温下为无色固体,常做绿色硝化剂)。电解原理如右上图所示,该电解池中生成N2O5的电极反应式是___________。
Ⅱ为研究哈伯法合成氨反应,T℃时,在容积为2 L恒容容器中通入4 mol N2和12mol H2,反应如下:N2(g)+3H2(g) ![]() 2NH3(g),若25min时反应达到平衡,各物质浓度随时间变化曲线如下图中甲、乙、丙。回答下列问题:
2NH3(g),若25min时反应达到平衡,各物质浓度随时间变化曲线如下图中甲、乙、丙。回答下列问题:

(1)0-25min内,反应的平均速率v(H2)为_________。
(2)T℃时,该反应的平衡常数K=_____________ (用最简分数表达)。
(3)T℃时,若起始充入8mol N2和24 mol H2,则反应刚达到平衡时,表示c( H2)在右图中相应的点为_____(填字母)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,可逆反应A(气)+3B(气)![]() 2C(气)若达到平衡的标志是
2C(气)若达到平衡的标志是
A. C的生成速率与B的生成速率相等
B. A、B、C的浓度不再发生变化
C. 单位时间内生成nmolA,同时生成3nmolB
D. A、B、C的分子数之比为1:3:2
查看答案和解析>>
科目: 来源: 题型:
【题目】Hg是水体污染的重金属元素之一。水溶液中二价汞的主要存在形态与C1-、OH-的浓度关系如图所示[图中的物质或粒子只有Hg(OH)2为难溶物;pCl=-lgc(Cl-)]。下列说法不正确的是
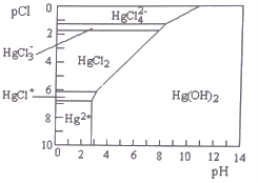
A. 可用如下方法除去污水中的Hg2+: FeS(s)+ Hg2+(aq)=HgS(s)+Fe2+(aq)
B. 当溶液pCl保持在1,pH在6~8时,汞元素主要以HgCl42-形式存在
C. HgCl2是一种强电解质,其电离方程式是:HgCl2=HgCl++Cl-
D. 当溶液pH保持在5,pCl由2改变至6时.可使HgCl2转化为Hg(OH)2
查看答案和解析>>
科目: 来源: 题型:
【题目】某人做酶的相关实验时,在试管中依次加入质量分数为3%的可溶性淀粉溶液2mL,2%的新鲜淀粉酶溶液2mL,放入适宜温度的热水中,保温5min。然后加入质量浓度为0.1g/mL的NaOH溶液1mL,摇匀,再加入质量浓度为0.01g/mL的CuSO4溶液4滴,摇匀,试管中液体的颜色是( )
A.砖红色 B.无色 C.蓝色 D.紫色
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于组成细胞的化合物的叙述中正确的是
A.糖类、固醇、氨基酸、核苷酸都含有基本元素 C、H、O、N
B.细胞中无机盐离子的含量对维持细胞的酸碱平衡有重要作用
C.蛋白质具有调节作用,如胰岛素和酶等
D.DNA与蛋白质构成的染色体是细胞核中的遗传物质
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,M、N能在溶液中发生反应生成P和Q: ![]() 。
。
A.将0.2 mol·L-1 M溶液和0.2 mol·L-1 N溶液各20 mL混合
B.将0.5 mol·L-1 M溶液和0.5 mol·L-1 N溶液各50 mL混合
C.将1 mol·L-1 M溶液和1 mol·L-1 N溶液各10 mL混合,同时倒入30 mL蒸馏水
D.将1 mol·L-1 M溶液20 mL和1.2 mol·L-1 N溶液60 mL混合
反应开始时,反应速率由大到小的顺序是。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响,在常温下按照如下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol L-1 FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol L-1 FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol L-1 FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是。
(2)实验①和②的目的是。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是。
(3)写出实验③的化学反应方程式:。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析如图能够得出的实验结论是。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com