
科目: 来源: 题型:
【题目】土法酿造葡萄酒(只加糖的纯天然酿酒法)容易出问题,有报道说,喝了自制葡萄酒差点失明。主要原因是发酵过程产生的菌种多达百种,难以控制,而产生对神经有毒的甲醇等物质。科学酿酒加SO2等辅料。我国国家标准(GB2760-2014)规定葡萄酒中SO2的残留量≤0.25g/L。
(1)葡萄酒中添加SO2的作用可能是________。
A.氧化细菌 B.抗氧化 C.漂白 D.增酸作用
I.实验方案一
利用SO2的漂白性检测干白葡萄酒(液体为无色)中的SO2或HSO3。设计如图1的实验:
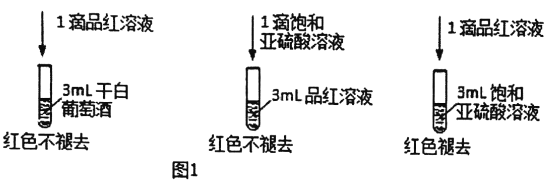
(2)甲同学得出实验结论: 干白葡萄酒中不含SO2或HSO3。这个结论是否合理?说明理由_________。
Ⅱ.实验方案二
如图2是在实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。

(3)关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没瓶中固体,写出C装置反应的方程式______,每消耗1molNa2O2,则转移电子数___________。
(4)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F中,为了证明SO2有还原性,并从绿色化学的角度考虑,则Z试剂可以是___________,现象是___________。
Ⅲ.实验方案三
用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入图3 装置(电极均为惰性材料) 进行实验,可用于制备硫酸,同时获得电能:

(5)M极发生的电极反应式为__________。N极区溶液pH______(变大、变小、不变)。
(6)若使该装置的电流强度达到2.0A,理论上8 分钟应向负极通入标准状况下气体的体积为___L (已知: 1个e所带电量为1.6×10-19C,阿伏伽德罗常数6×1023)。
查看答案和解析>>
科目: 来源: 题型:
【题目】核黄素又称为维生素B2 , 可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳.核黄素分子的结构为  已知:
已知: ![]()
有关核黄素的下列说法中,不正确的是( )
A.该化合物的分子式为C17H22N4O6
B.酸性条件下加热水解,有CO2生成
C.酸性条件下加热水解,所得溶液加碱后有NH3生成
D.能发生酯化反应
查看答案和解析>>
科目: 来源: 题型:
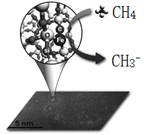
【题目】中科院一项最新成果实现了甲烷高效生产乙烯,甲烷在催化作用下脱氢,在气相中经自由基偶联反应生成乙烯,如图所示。
物质 | 燃烧热(kJ/mol) |
氢气 | 285.8 |
甲烷 | 890.3 |
乙烯 | 1411.5 |
(1)已知相关物质的燃烧热如上表,写出甲烷制备乙烯的热化学方程式_________。
(2)在400℃时,向1L的恒容反应器中充入1molCH4,发生上述反应,测得平衡混合气体中C2H4的体积分数为20.0 %。则在该温度下,其平衡常数K=_______。按化学平衡移动原理,在图(a)中画出该反应的平衡转化率与温度及压强(p1>p2)的关系曲线。_______________________
(3)在制备C2H4时,通常存在副反应:2CH4(g)![]() C2H6(g)+H2(g)。在常温下,向体积为1L的恒容反应器中充入1molCH4,然后不断升高温度,得到图(b)。
C2H6(g)+H2(g)。在常温下,向体积为1L的恒容反应器中充入1molCH4,然后不断升高温度,得到图(b)。
①在200℃时,测出乙烷的量比乙烯多的主要原因是_________________________。
②在600℃后,乙烯的体积分数减少的主要原因是__________________________。

(4)工业上常采用除杂效率高的吸收-电解联合法,除去天然气中的杂质气体H2S,并转化为可回收利用的单质硫,其装置如下图所示。

通电前,先通入一段时间含H2S的甲烷气,使部分NaOH吸收H2S转化为Na2S,再接通电源,继续通入含杂质的甲烷气,并控制好通气速率。装置中右端碳棒为_________极,左端碳棒上的电极反应为_________________________,右池中的c(NaOH):c(Na2S)______________(填“增大”、“基本不变”或“减小)。
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表和元素周期律可指导人们进行规律性推测和判断。下列说法中不合理的是
A. 若X+和Y2﹣的核外电子层结构相同,则原子序数:X>Y
B. 硅、锗都位于金属与非金属的交界处,都可以做半导体材料
C. 盐酸(HCl)酸性比H2SiO3强,可推断出元素的非金属性:Cl>Si
D. Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH>Ba(OH)2
查看答案和解析>>
科目: 来源: 题型:
【题目】用丙醛(CH3CH2CHO)制取 ![]() 的过程中发生的反应类型为( ) ①取代 ②消去 ③加聚 ④水解 ⑤氧化 ⑥还原.
的过程中发生的反应类型为( ) ①取代 ②消去 ③加聚 ④水解 ⑤氧化 ⑥还原.
A.①④⑥
B.⑤②③
C.⑥②③
D.②④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】某工业废液主要成分为SiO2、FeO、Fe2O3、Al2O3 等,为综合利用,对其进行如下处理,制备Al2O3及(NH4)2Fe(SO4)2·6H2O。

相关数据如下:
Kb(NH3·H2O) | 1.8×10-5 | 溶解度/g | 10℃ | 30℃ | 50℃ |
Ksp[A1(OH)3] | 1.3×10-33 | (NH4)2SO4 | 73.0 | 78.0 | 84.5 |
Ksp[Fe(OH)2] | 8.0×10-16 | FeSO4·7H2O | 40.0 | 60.0 | |
Ksp[Fe(OH)3] | 4.0×10-38 | |(NH4)2Fe(SO4)2·6H2O | 18.1 | 24.5 | 31.3 |
(1)酸浸过程中产生的滤渣的主要成分是_______________。
(2)滤液①中加入铁粉的作用是__________________。
(3)已知加入氨水前,溶液中H+、Fe2+、Al3+的浓度分别为0.02 mol/L、0.16mol/L、0.04mol/L,加人氨水后,溶液的体积刚好增加1倍。为防止Fe2+ 产生沉淀,则溶液中的pH不能超过_______,此时溶液中n(NH3·H2O):n(NH4+)≤_____________;若调节溶液pH为5,则溶液中所有离子的物质的量浓度由大到小排列的顺序是_________________。
(4)由滤液②制备(NH4)2Fe(SO4)2·6H2O 晶体时,为防止有(NH4)2SO4或FeSO4晶体析出,须先向滤液②中加人适量的______________,再蒸发浓缩、__________、过滤、__________、干燥。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮化镓(GaN)被称为第三代半导体材料,其应用已经取得了突破性的进展。
已知:(i)氮化镓性质稳定,不与水、酸反应,只在加热时溶于浓碱。
(ii)NiCl2 溶液在加热时,先转化为Ni(OH)2,后分解为NiO。
(iii)制备氮化镓的反应为:2Ga+2NH3![]() 2GaN+3H2
2GaN+3H2
某学校化学兴趣小组实验室制备氮化镓,设计实验装置如图所示:

设计实验步骤如下:
①滴加几滴NiCl2 溶液润湿金属镓粉末,置于反应器内。
②先通入一段时间后的H2,再加热。
③停止通氢气,改通入氨气,继续加热一段时间。
④停止加热,继续通入氨气,直至冷却。
⑤将反应器内的固体转移到盛有盐酸的烧杯中,充分反应过滤、洗涤、干燥。
(1)仪器X中的试剂是___________,仪器Y的名称是__________________。
(2)指出该套装置中存在一处明显的错误是________________________。
(3)步骤①中选择NiCl2 溶液,不选择氧化镍的原因是____________________。
a.增大接触面积,加快化学反应速率
b使镍能均匀附着在镓粉的表面,提高催化效率
c.为了能更好形成原电池,加快反应速率
(4)步骤③中制备氮化镓,则判断该反应接近完成时观察到的现象是____________________。
(5)请写出步骤⑤中检验产品氮化镓固体洗涤干净的操作________________________。
(6)镓元素与铝同族,其性质与铝类似,请写出氮化镓溶于热NaOH溶液的离子方程式:______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】类比推理是重要的学科思想,下列根据已知进行推理正确的是( )
选项 | 已知 | 类比推理 |
A |
|
|
B |
|
|
C | 常温下,浓硝酸使铁钝化 | 浓硝酸与铜不反应 |
D |
| 过量 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于酶的叙述中正确的是 ( )
A.由有分泌功能的细胞产生,并且能调节生物体的生命活动
B.生物体内的酶在不断更新
C.都是在核糖体上合成的
D.与双缩脲试剂发生作用都可产生紫色反应
查看答案和解析>>
科目: 来源: 题型:
【题目】有关 ![]() 分子结构的下列叙述中正确的是( ) ①除苯环外的其余碳原子有可能都在一条直线上
分子结构的下列叙述中正确的是( ) ①除苯环外的其余碳原子有可能都在一条直线上
②除苯环外的其余碳原子不可能都在一条直线上
③12个碳原子不可能都在同一平面上
④12个碳原子有可能都在同一平面上.
A.①②
B.②③
C.①③
D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com