
科目: 来源: 题型:
【题目】正交硫和单斜硫是硫元素的两种常见单质,其晶状结构如左下图所示;构成晶体的微粒均是S8分子,其分子结构如右下图所示。回答下列问题:

(1)正交硫和单斜硫互称为硫元素的________________。
(2)S8分子中,硫原子之间形成的化学键是_____(填“离子键”或“共价键”)。
(3)已知正交硫的熔点为112.8 ℃,沸点为444.6 ℃,硬度较小。晶状的正交硫是________晶体,构成晶体的微粒间的相互作用力是___________________。
(4)已知:S8(正交) =S8(单斜) ΔH=+2.64 kJ·molˉ1。正交硫与单斜硫相比,相对比较稳定的是_______________。正交硫转化为单斜硫时,发生________(填“物理变化”或“化学变化”)。
(5)已知通常状况下4g 硫粉完全燃烧放出37 kJ的热量,写出该反应的热化学方程式___________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组以CoCl26H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体Cox(NH3)y ClZ . 为测定其组成,进行如下实验. Ⅰ.氨的测定:精确称取wg样品,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1mLc1molL﹣1的盐酸标准溶液吸收.蒸氨结束后取下接收瓶,用c2molL﹣1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液.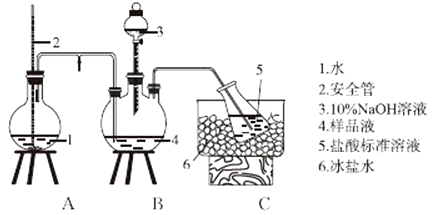
氨的测定装置(已省略加热和加持装置)
Ⅱ.氯的测定:另准确称取wg样品,配成溶液后用AgNO3标准溶液滴定.已知:AgCl为白色沉淀Ksp(AgCl)=1.8×10﹣10;Ag2CrO4为砖红色沉淀,Ksp(Ag2CrO4)=1.2×10﹣12;Ag2S为黑色沉淀,Ksp(Ag2S)=6.3×10﹣50 .
Ⅲ.根据样品质量为wg即可确定样品中Co元素的质量,进而确定样品的化学组成.
回答下列问题:
(1)实验前,按图组装好装置后,如何检查该装置的气密性;
(2)盛装10%NaOH溶液的仪器名称;
(3)样品中氨的质量分数表达式为;
(4)标准硝酸银溶液应装在棕色的式滴定管中;若滴定管未用标准液润洗,则测定Cl﹣的量 .(填“偏大”“偏小”)
(5)在测定氯的过程中,应选用(填“K2CO3”或“K2S”)为指示剂,判断达到测定终点时的操作和现象为 .
(6)当达到滴定终点时,若c(Ag+)=1.0×10﹣5 molL﹣1 , ![]() =,(或
=,(或 ![]() =)(根据所选指示剂进行填空)
=)(根据所选指示剂进行填空)
查看答案和解析>>
科目: 来源: 题型:
【题目】有三种有机物的分子式均为C8H8,其键线式分别为,X: ![]() ,Y:
,Y: ![]() ,Z:
,Z: ![]() .下列说法正确的是
.下列说法正确的是
A. X 能使酸性高锰酸钾溶液褪色,也能使溴的四氯化碳溶液褪色
B. Y 能发生取代反应、加成反应和氧化反应
C. X、Y、Z互为同分异构体,它们二氯代物的同分异构体数目相同
D. X、Y、Z分子中所有原子一定在同一平面内
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气是21世纪的新型能源.制氢的方法之一是以煤的转化为基础,部分反应如下: CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣41kJmol﹣1
CaO(s)+CO2(g)CaCO3(s)△H=﹣172kJmol﹣1
CO2(g)+4H2(g)CH4(g)+2H2O(g)△H=﹣187kJmol﹣1
(1)写出CO与H2生成CH4和水蒸气的热化学方程式 .
(2)某温度下,在10L密闭容器中投入CO2、H2和CaO,仅发生CO2(g)+4H2(g)CH4(g)+2H2O(g)和CaO(s)+CO2(g)CaCO3(s)两个反应,部分物质的物质的量与时间的关系如表所示:
物质 | CO2 | H2 | CaO |
0 | 0.50 | 1.00 | 0.40 |
2 | 0.35 | 0.60 | a |
6 | 0.20 | 0.20 | b |
8 | 0.20 | 0.20 | b |
①反应在0~2min内的平均反应速率v(H2)=
②b=
③反应到达平衡后,改变反应的某些条件,再次达到平衡时,不正确的是(填字母)
A.扩大容器体积c(H2)增大 B.升高温度,n(CO2)增大
C.充入少量H2 , CaCO3质量减小 D.充入少量CO2 , c(CH4)增大
④此温度下,反应CO2(g)+4H2(g)CH4(g)+2H2O(g)的化学平衡常数K= . 若向10L容器中投入CO2、H2和CH4各0.1mol,H2O(g)xmol,要使v正(CO2)>v逆(CO2),x的取值范围为
(3)若以CH4、O2组成燃料电池,在酸性条件下负极电极反应式为.当两极消耗3.36L气体(标准状况)时,将产生的气体(假设全部逸出)通入50mL2molL﹣1 NaOH溶液中,下列说法正确的是
A.反应过程中共转移电子1.2mol
B.所得溶液为Na2CO3和NaHCO3的混合溶液
C.c(Na+ )>c(CO32﹣)>c(OH﹣ )>c(HCO3﹣)>c(H+)
D.c(OH﹣)=2c(H2CO3)+c(HCO3﹣ )+c(H+ )
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A是一种重要的有机合成中间体,经常用来合成多种高分子化合物。已知A分子中不含甲基。由A合成的两种高分子化合物的路线如下图所示:
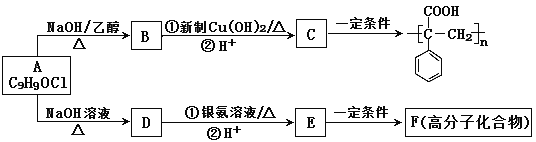
(1)写出C中含有的官能团名称___________________ 。
(2)由A生成B的反应类型为______________________________________。
(3)C的核磁共振氢谱有________组峰
(4)写出A生成D的化学方程式_______________________________________。
(5)F的结构简式是___________________。
(6)苯环上的二取代芳香化合物W是D的同分异构体,且W分子中只具有一个官能团,则W的结构共有_____________种。
查看答案和解析>>
科目: 来源: 题型:
【题目】表是A、B、C、D五中有机物质的相关信息:
A | B | C | D | E |
①能使溴的四氯化碳溶液褪色; | ①由C、H两种元素组成; | ①由C、H、O三种元素组成; | ①相对分子质量比C少2; | ①由C、H、O三种元素组成; |
(1)A与氢气发生加成反应后生成分子F,F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2 . 当n=时,这类有机物开始出现同分异构体.
(2)A与溴的四氯化碳溶液反应的生成物的结构简式;该生成物在一定条件下可用于制取最简单的二元醇方程式为: .
(3)B具有的性质是(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在催化剂作用下,B与溴反应的化学方程式: .
(4)C与E反应能生成酯,该反应类型为;其化学反应方程式为: .
(5)D在一定条件下能发生银镜反应,其化学反应方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com