
科目: 来源: 题型:
【题目】有关如图所示原电池的叙述,正确的是(盐桥中装有含琼胶的KCl饱和溶液)( )
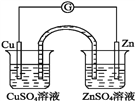
A. 铜片上发生氧化反应 B. 取出盐桥后,电流计依然发生偏转
C. 反应中,盐桥中的K+会移向CuSO4溶液 D. 反应前后铜片质量不改变
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子中,在酸性溶液中能大量共存的无色溶液( )
A.Na+、Cl-、NO3-、SO42-B.K+、Cu2+、NO3-、Cl-
C.Mg2+、Cl-、SO42-、HCO3-D.Ba2+、NO3-、Cl-、CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】锌及其化合物在生产生活中应用比较广泛。
(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
①ZnFe2O4中Fe的化合价是___________。
②工业上利用反应ZnFe2(C2O4)3·6H2O![]() ZnFe2O4+2CO2↑+4CO↑+6H2O 制备ZnFe2O4该反应中还原产物是___(填化学式),每生成1mol ZnFe2O4转移的电子总数是__________。
ZnFe2O4+2CO2↑+4CO↑+6H2O 制备ZnFe2O4该反应中还原产物是___(填化学式),每生成1mol ZnFe2O4转移的电子总数是__________。
(2)工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下:
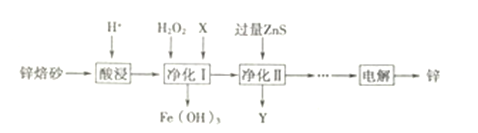
①酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率,为达到这一目的,还可采用的措施是_______(任答一条)。写出ZnFe2O4溶于酸的离子方程式__________。
②净化I中H2O2 参与反应的离子方程式为___________
③净化Ⅱ中Y 的主要成分是_____(填化学式)。
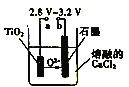
(3)利用锌锰电池在800~1000℃时电解TiO2可制得金属钛,装置如图所示。图中a电极的材料为_____,阴极的电极反应式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A. -44.2kJ·mol-1 B. +44.2kJ·mlo-1
C. -330kJ·mol-1 D. +330kJ·mlo-1
查看答案和解析>>
科目: 来源: 题型:
【题目】学习与研究化学经常要进行实验,请完成以下课题:
(1)玻璃棒的作用主要有以下三种,请回答下列问题: a.搅拌 b.引流 c.蘸取溶液
①实验室配制一定物质的量浓度溶液,将固体溶解时,玻璃棒的作用是(填字母),
②将烧杯中的溶液注入容量瓶时,玻璃棒的作用是(填字母),
③用浓盐酸检验氨气时,玻璃棒的作用是(填字母),
④粗盐提纯时,用过滤的方法除去不溶性的泥沙,玻璃棒的作用是(填字母).
(2)现用98%的浓H2SO4(ρ)=1.84g/cm3)配制浓度为0.5mol/L的稀硫酸500mL. ①选用的玻璃仪器除了量筒、玻璃棒、烧杯,还用到、 .
②将浓H2SO4沿烧杯内壁慢慢注入盛水的烧杯中,不断搅拌的目的是 , 若搅拌过程中有液体溅出,会使最终结果(填“偏高”、“偏低”或“无影响”).
③定容时必须使溶液凹液面与刻度线相切,若俯视会使结果(填“偏高”、“偏低”或“无影响”).
查看答案和解析>>
科目: 来源: 题型:
【题目】已知3.6 g碳在6.4 g氧气中燃烧,至反应物耗尽,测得放出热量a kJ。又知12.0 g碳完全燃烧,放出热量为 b kJ。则热化学方程式C(s)+![]() O2(g)===CO(g) ΔH=Q 中Q等于( )
O2(g)===CO(g) ΔH=Q 中Q等于( )
A. -(a-b) kJ·mol-1 B. -(a+b) kJ·mol-1
C. -(5a-0.5b) kJ·mol-1 D. -(10a-b) kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.MgCl2的形成过程可表示为![]()
![]()
B.H2O分子的结构式可表示为H—O—H
C.NaOH是离子化合物,所以不含共价键
D.Na2S的电子式为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】能够说明金属锌的还原性比铁的还原性强的是( )
A.都能与盐酸反应产生氢气B.都能与硫酸铜溶液反应生成铜
C.锌溶于氯化亚铁溶液并有铁生成D.都能与氧气反应生成氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com