
科目: 来源: 题型:
【题目】下列几项中,在生物体内含量较少,但是对于维持生物体的正常生命活动必不可少的元素是
A. Fe、Mn、Zn、Mg B. Cu、Zn、Mn、K
C. Mn、Zn、B、Cu D. Cu、N、S、Mo
查看答案和解析>>
科目: 来源: 题型:
【题目】电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%.现取20mL pH=3的 CH3COOH溶液,加入0.2molL﹣1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( ) 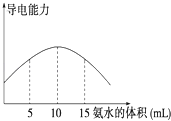
A.0.5%
B.1.5%
C.0.1%
D.1%
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质的性质和该性质的应用均正确的是
A. 常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器盛装浓硫酸
B. SiO2不与任何酸反应,可用石英制造耐酸容器
C. ClO2具有还原性,可用于自来水的杀菌消毒
D. Al、Fe、Cu对应的氧化物均为碱性氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%.其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( ) A.2 mol C
B.2 mol A、2mol B和1 mol He(不参加反应)
C.1 mol B和1 mol C
D.2 mol
A.3 mol B和3 mol C
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列有关稀溶液中离子浓度的说法正确的是( )
A.同浓度的四种溶液:①NH4Cl ②(NH4)2SO4③NH4HSO4④NH4Al(SO4)2溶液,c(NH4+)浓度的大小关系:②>④>③>①
B.一定浓度的NaHS溶液中:c(Na+)+c(OH﹣)=c(H+)+c(HS﹣)+2c(H2S)
C.若0.1 mol/L NH4Cl溶液pH=5,则其中离子浓度最大与最小的差值为(0.1﹣10﹣5)mol/L
D.现有四种溶液:①pH=4的H2SO4溶液 ②pH=4的NH4Cl溶液 ③pH=10的氨水 ④pH=10的CH3COONa溶液,其中水电离出的氢离子浓度大小关系为:②=④>③>①
查看答案和解析>>
科目: 来源: 题型:
【题目】在T℃时,Ba(OH)2的稀溶液中c(H+)=10﹣amolL﹣1 , c(OH﹣)=10﹣b molL﹣1 , 已知a+b=12.向该溶液中逐滴加入pH=4的盐酸,测得混合溶液的部分pH如下表所示:
序号 | 氢氧化钡溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | c |
③ | 22.00 | 22.00 | d |
假设溶液混合前后的体积变化可忽略不计,则下列说法不正确的是( )
A.a=8
B.b=4
C.c=5
D.d=6
查看答案和解析>>
科目: 来源: 题型:
【题目】有a、b、c、d四个金属电极,G为电流计,有关的反应装置及部分反应现象记录如下:
实验 |
|
|
|
|
部分实 | a极质量减小 | 溶液中的SO42﹣﹣向b极移动 | d极溶解c极 | 电子从d极 |
由此可判断这四种金属的活动性顺序是( )
A.d>a>b>c
B.a>b>c>d
C.b>c>d>a
D.a>b>d>c
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、X是中学化学常见的物质,A、B、C均由短周期元素组成,转化关系如图。
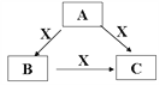
请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,向C的水溶液中通入过量的CO2可得B的白色胶状沉淀。
①A中含有的金属元素为_________(写元素名称),它在周期表中的位置为_____________。
②写出B → C反应的离子方程式为___________________________________。
(2)若A为稀HNO3,X为常见黑色金属单质,写出A→B反应的离子方程式__________。
(3)若A、B、C三种化合物的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生。
①A中所含有的化学键是________________
②自然界中存在B、C和H2O按一定比例结晶而成的固体,取一定量该固体溶于水配成一定物质的量浓度的溶液100mL,所用到的玻璃仪器有玻璃棒、烧杯、________、_________。
③若测得上述溶液中金属阳离子的浓度为0.5mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为 ____________ g 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,在体积为2L的密闭容器中充入1mol A和b mol B气体,发生如下反应:A(g)+B(g)2C(g),5min后反应达到平衡时n(A)为0.4mol.在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度的关系如下图所示.下列叙述正确的是( ) 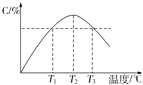
A.0~5 min,C物质的平均反应速率为0.04 molL﹣1min﹣1
B.图中温度T1时的正反应速率等于温度T3时的正反应速率
C.该反应温度T2时的平衡常数大于温度T3时的平衡常数
D.图中T2时,若只增大压强,则正、逆反应速率不改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com