
科目: 来源: 题型:
【题目】下列物质反应后可生成 BrCH2CH2Br 的是( )
A.乙烯和溴化氢加成
B.乙烷和溴化氢光照
C.乙烯通入溴的四氯化碳溶液中
D.乙烷通入溴的四氯化碳溶液中
查看答案和解析>>
科目: 来源: 题型:
【题目】CoCO3是一种制造锂电池电极的原料。以含钴废渣(主要成分CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
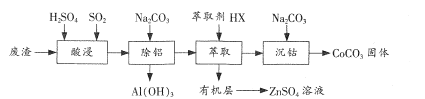
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol/L计算)

(1)“酸浸”时通入SO2的目的是__。
(2)“除铝”时调节溶液pH范围为__,该过程中主要反应的离子方程式为__。
(3)“萃取”过程可表示为ZnSO4(水层)+2HX(有机层)![]() ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是__。
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是__。
(4)“沉钴”时Na2CO3溶液需缓慢滴加的原因是 __。
(5)CoCO3隔绝空气灼烧可以生成Co2O3,该反应的化学方程式为_______ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据问题填空:
(1)已知反应:①C(s)+ ![]() O2(g)=CO(g)△H1=﹣110.5kJmol﹣1②C(s)+O2(g)═CO2(g)△H2=﹣393.5kJmol﹣1
O2(g)=CO(g)△H1=﹣110.5kJmol﹣1②C(s)+O2(g)═CO2(g)△H2=﹣393.5kJmol﹣1
写出表示CO燃烧热的热化学方程式 .
(2)搭载神舟十一号航天飞船的长征二号F运载火箭的助推器、芯一级、芯二级应用的燃料全部是液态偏二甲肼和液态四氧化二氮.其中偏二甲肼(C2H8N2)为火箭燃料,四氧化二氮(N2O4)为氧化剂,当它们混合时,立即产生大量氮气、二氧化碳和水蒸气,并放出大量热. 若0.1mol 偏二甲肼与N2O4完全反应时,放出 526.65kJ的热量.写出该反应的热化学方程式: .
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图是从元素周期表中截取下来的,甲、乙、丙为短周期主族元素,下列说法中正确的是( )
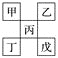
A. 丁一定是金属元素,其金属性比丙强
B. 丙的最高价氧化物水化物显强酸性
C. 乙的氢化物是以分子形式存在,且分子间存在氢键
D. 戊的原子序数一定是甲的5倍,且原子半径比甲大
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组要完成中和热的测定实验.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、量筒、稀盐酸(0.5molL﹣1)、稀 NaOH溶液(0.55molL﹣1),尚缺少的实验玻璃用品是、 .
(2)写出表示稀盐酸和稀氢氧化钠溶液反应中和热的热化学方程式(中和热为57.3kJmol﹣1): .
(3)若用稀醋酸、稀硫酸、浓硫酸分别和稀氢氧化钠溶液反应来测定中和热,恰好完全反应时对应的热效应分别为△H1、△H2、△H3的大小关系是 .
(4)每组实验所用氢氧化钠溶液和稀盐酸的体积均为 50mL,可近似认为该实验中稀盐酸和稀氢氧化钠溶液的密度均为 1g/cm3,中和后生成溶液的比热容c=4.18J/(g℃),实验中记录数据如表所示,请填写表中空白:
编号 | 起始温度T1/℃ | 终止温度T2/℃ | 平均温度差T2﹣T1/℃ | △H | ||
盐酸 | NaOH | 平均值 | ||||
① | 26.2 | 26.0 | 26.1 | 29.2 |
|
|
② | 25.9 | 25.9 | 25.9 | 29.2 | ||
③ | 26.4 | 26.2 | 26.3 | 29.5 | ||
查看答案和解析>>
科目: 来源: 题型:
【题目】观察下列几个装置示意图,有关叙述正确的是( ) 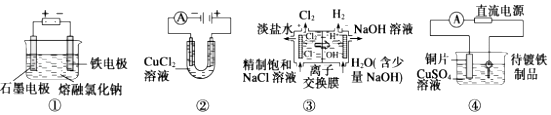
A.装置①工业上可用于生产金属钠,电解过程中石墨电极产生金属
B.装置②中阳极产生的气体可以使湿润的淀粉碘化钾试纸变蓝
C.装置③中的离子交换膜允许阳离子、阴离子和小分子水通过
D.装置④的待镀铁制品应与电源正极相连
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是一种重要的化工产品,硫酸的用量被视为一个国家工业发达水平的一种标志。反应2SO2+O2![]() 2SO3是工业制取硫酸的主要反应之一,下列说法不正确的是( )
2SO3是工业制取硫酸的主要反应之一,下列说法不正确的是( )
A. 该反应为可逆反应,在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫
B. 达到平衡后,反应就停止了,正、逆反应速率相等且都为零
C. 在利用上述反应生产三氧化硫时,要考虑适当增大化学反应速率
D. 在利用上述反应生产三氧化硫时,要考虑使尽可能多的二氧化硫转化为三氧化硫
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A. 乙醇、乙酸、乙酸乙酯都能发生取代反应
B. 石油裂化和裂解的目的均是为了将长链烃转化为短链烃
C. 石油裂化得到的汽油可使溴水、酸性高锰酸钾溶液褪色,褪色原理不同
D. 等物质的量的乙烯、丙烯分别充分燃烧,所耗氧气的物质的量一样多
查看答案和解析>>
科目: 来源: 题型:
【题目】Boderlscens研究反应:H2(g)+I2(g) ![]() 2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:
2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:
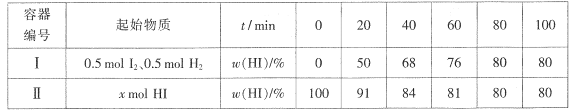
研究发现上述反应中![]() 其中
其中![]() 为常数。下列说法正确的是
为常数。下列说法正确的是
A. 温度为T时该反应的![]()
B. 容器I中前20 min的平均速率v(HI)=0.0125mol.L-1.min-1
C. 若起始时,向容器I中加入物质的量均为0.l mol的H2、I2、HI,反应逆向进行
D. 若两容器中![]() 且
且 ![]() 则x的值一定为1
则x的值一定为1
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中含有两种溶质NaCl和H2SO4 , 物质的量之比为3:1.用石墨作电极电解溶液,根据电极产物,可明显分为三个阶段.下列叙述不正确的是( )
A.阴极只析出H2
B.阳极先析出Cl2 , 后析出O2
C.电解最后阶段为电解水
D.溶液pH不断增大,最后为7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com