
科目: 来源: 题型:
【题目】实验室利用废铜合金(含少量铁和铝)来制取硫酸铜晶体(CuSO4·5H2O),方案如下:

金属离子生成氢氧化物沉淀的pH可参考下列数据:
Fe3+ | Fe2+ | Cu2+ | Al3+ | |
开始沉淀时的pH | 2.2 | 7.5 | 5.2 | 3.7 |
完全沉淀时的pH | 3.2 | 9.0 | 6.7 | 4.7 |
请回答:
(1)若溶解合金时加入的混酸由2 L 3 mol·L-1硫酸和1 L 2 mol·L-1硝酸混合而成,则反应后生成标准状况下的NO的体积最多为____________L。
(2)加入H2O2的目的是____________。
(3)为保证产品的纯度,M物质最好选用________(填字母),调节pH的范围为____________。
a.Cu(OH)2 b.H2SO4 c.NH3·H2O d.Na2CO3
(4)滤液D中加入硫酸的目的为_______________________________________。
(5)从溶液E制得CuSO4·5H2O晶体所需要的步骤为________、结晶、过滤和干燥。
(6)0.80g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。试确定200℃时固体物质的化学式______________。

查看答案和解析>>
科目: 来源: 题型:
【题目】现有常见金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间存在如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。其中B是地壳中含量居第一的金属元素。请回答下列问题:

(1)写出金属B和气体丙的化学式__________、_________。
(2)写出反应①的化学反应方程式______________________________,写出反应⑤的离子方程式__________________________________。
(3)用溶液G与铜反应可制作印刷电路板,其离子方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】请按要求回答下列问题:
(1)铝热反应在工业生产中的重要用途之一是焊接钢轨,其反应的化学方程式为:______________________;“硅材料”又被称为信息材料,作为半导体材料广泛用于制造集成电路的是____________(填化学式)。
(2)胃舒平是治疗胃酸(HCl)过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理是(用离子方程式表示):___________________。
(3)反应2H2CrO4 + 3H2O2 = 2Cr(OH)3 + 3O2↑+ 2H2O中H2O2的变化过程为H2O2→O2。
① 该反应的还原剂是______________________________。
② 在该反应方程式中标明电子转移的方向和数目:_______________
2H2CrO4 + 3H2O2 = 2Cr(OH)3 + 3O2↑+ 2H2O
③ 若反应中转移了3 mol电子,则产生的气体在标准状况下体积为_________L。
查看答案和解析>>
科目: 来源: 题型:
【题目】在给定条件下,下列划线物质在化学反应中能被完全消耗的是( )
A. 用40 mL 10 mol/L浓盐酸与8.7 g 二氧化锰共热制取氯气
B. 标况下,将2.7 g 铝片投入到20 mL 18 mol/L的浓硫酸中
C. 向120 mL 2 mol/L 的盐酸中加入5.6g 铁
D. 向Ba(OH)2和NaOH各0.1 mol的混合溶液中通入标准状况下2.24 L CO2 气体
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列各图曲线表征的信息,得出的结论不正确的是


A. 图1表示常温下向体积为10 mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1CH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH-)
B. 图2表示用水稀释pH相同的盐酸和醋酸时溶液的pH变化曲线,其中Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a
C. 图3表示H2与O2发生反应过程中的能量变化,H2的燃烧热为285.8 kJ·mol-1
D. 由图4得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入适量CuO,调节溶液的pH至4左右
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A.同周期元素中,ⅠA族元素的原子半径最小
B.仅由非金属元素不可能形成离子化合物
C.目前使用的元素周期表中,最长的周期含有32种元素
D.凡是有化学键断裂的过程一定发生了化学反应
查看答案和解析>>
科目: 来源: 题型:
【题目】聚丁二酸乙二醇酯(PES)是一种生物可降解的聚酯,它在塑料薄膜、食品包装和生物材料方面有着广泛的应用.其结构简式为: 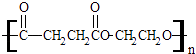 ①聚丁二酸乙二醇酯(PES)是由两种单体通过反应(填反应类型)制得的.形成该聚合物的两种单体是 .
①聚丁二酸乙二醇酯(PES)是由两种单体通过反应(填反应类型)制得的.形成该聚合物的两种单体是 .
②这两种单体相互之间也可能形成一种八元环状酯,请写出该环状化合物的结构简式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】钛酸钡是一种强介电化合物材料,具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”,工业制取方法如下,先获得不溶性草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],煅烧后可获得钛酸钡粉体。

(1)酸浸时发生的反应的离子方程式为__________________;
(2)配制TiCl4溶液时通常将TiCl4固体溶于浓盐酸再加水稀释,其目的是_________________________;
(3)加入H2C2O4溶液时,发生反应的化学方程式为____________________;可循环使用的物质X是________(填化学式),设计实验方案验证草酸氧钛钡晶体是否洗涤干净:_______________________;
(4)煅烧草酸氧钛钡晶体得到BaTiO3的同时,生成高温下的气体产物有CO、_______和_________;
(5)工业上用饱和Na2CO3溶液处理重晶石(主要成分是BaSO4),待达到平衡后,移走上层清液,重复多次操作,将其转化为易溶于酸的BaCO3,再由BaCO3制备其它钡盐。已知常温下:Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.58×10-9,请问至少需要______ mol·L-1的碳酸钠溶液浸泡才能实现上述转化(忽略CO32-的水解)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com