
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性;A、D同主族,D的焰色反应为黄色;E的简单阳离子与X具有相同电子数,且E是同周期中简单离子半径最小的元素;F元素的原子最外层比次外层少两个电子,C、G两种元素的原子最外层共有13个电子。则
(1)F在元素周期表中的位置为_______________。
(2)在2 L的密闭容器中,充入2 mol B2和3 mol A2,在一定条件下发生反应,5 s后测得A2为1.8 mol,则以B2的表示的反应速率v(B2)为__________________________。
(3)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为_______________。
(4)D2F溶液在空气中长期放置发生反应,生成一种强碱与D2F2。D2F2与过氧化钠的结构和化学性质相似,其溶液显黄色。D2F2的电子式为_______,写出D2F在空气中长期放置生成D2F2的化学反应方程式为:_____________。D2F2的溶液与稀硫酸反应产生的现象为_____________。
(5)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol A4B4熔融电离生成两种离子各1mol,则该物质熔融时的电离方程式为____________。
(6)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。

则曲线Y表明M中的溶质为________;原NaOH溶液的物质的量浓度为_______;由曲线X、Y可知,两次实验通入的CO2的体积比为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学实验小组的同学将打磨过的镁条投入到滴有酚酞的饱和NaHCO3溶液中,发现反应迅速,产生大量气泡和白色不溶物,溶液的浅红色加深。该小组同学对白色不溶物的成分进行了探究和确定。
I.提出假设:
(1)甲同学:可能只是MgCO3
乙同学:可能只是__________________
丙同学:可能是xMgCO3·yMg(OH)2
(2)在探究沉淀成分前,需将沉淀从溶液中过滤、洗涤、低温干燥,洗涤沉淀的操作方法是_________。
Ⅱ.定量实验探究:取一定量已干燥过的沉淀样品,利用下列装置测定其组成(部分固定夹持装置未画出),经实验前后对比各装置的质量变化来分析沉淀样品的组成,得出丙同学的假设是正确的。请回答下列问题:

(3)写出xMgCO3·yMg(OH)2受热分解的化学方程式_________________________(用x、y 表示)
(4)①实验中合理的实验装置连接顺序为;e→____→_____→____→_____→____→_____→____(各装置只使用一次)___________________
②实验一段时间后,当装置B中_____________(填实验现象)时,停止加热,说明沉淀样品已完全分解,然后打开f处的活塞,缓缓通入空气数分钟的目的是_____________________________________。
③指导老师认为在上述实验装置末端还需再连接一个装置D,若无此装置,则会使测出的x∶y的值_______________(填“偏大”、“偏小”或“无影响”)
(5)若改进实验后,最终装置B 质量增加m 克,装置D质量增加n克,则x∶y=________(用含m、n 的代数式表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】某周期第ⅡA族元素的原子序数为x,则同周期的第ⅣA族元素的原子序数为( )
A.只能是x+2B.可能是x+8或x+18
C.可能是x+13D.可能是x+2或x+12或x+26
查看答案和解析>>
科目: 来源: 题型:
【题目】铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:

已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为2Na2SiO3+2NaAlO2+2H2O=Na2A12Si2O8↓+4NaOH。请回答下列问题:
(1)铝土矿中Al2O3与氢氧化钠溶液反应的离子方程式为_________________________________。
(2)在工艺流程中“酸化”时,加入的最佳物质B是________,理由是_______________________,写出酸化过程发生反应的化学方程式:________________________________。
(3)工业上用Al2O3与C、Cl2在高温条件下反应制取AlCl3,理论上每消耗6.0 g碳单质,转移1 mol电子,则反应的化学方程式为__________________________________。
(4)某同学推测铝与氧化铁发生铝热反应得到的熔融物中还含有Fe2O3,设计了如下方案来验证:取一块该熔融物投入少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe2O3。
则物质甲是_________(填化学式),请判断该同学设计的实验方案的合理性_________(填“合理”或“不合理”)。原因是_______________________________________(若合理,则不用填写)。
查看答案和解析>>
科目: 来源: 题型:
【题目】
三硫化四磷是黄绿色针状结晶,其结构如图所示.不溶于冷水,溶于叠氮酸、二硫化碳、苯等有机济剂,在沸腾的NaOH稀溶液中会迅速水解。回答下列问题:

(1)Se是S的下一周期同主族元素,其核外电子排布式为_______。
(2)第一电离能:S____(填“>”或“<”,下同)P,电负性:S____P
(3)三硫化四磷分子中P原子采取______杂化,与PO3-互为等电子体的化合物分子的化学式为______。
(4)二硫化碳属______(填“极性”或“非极性”)分子。
(5)用NA表示阿伏伽德罗常数的数值,0.1mol三硫化四磷分子中含有的孤电子对数为____。
(6)纯叠氮酸(HN3)在常温下是一种液体,沸点较高,为308.8K,主要原因是________。
(7)氢氧化钠具有NaCl型结构,其晶胞中Na+与OH-之间的距离为acm ,晶胞中Na+的配位数为_______,用NA表示阿伏伽德罗常数的数值,NaOH的密度为_____g/cm3。
查看答案和解析>>
科目: 来源: 题型:
【题目】把质量为mg的铜丝灼烧变成黑色,立即放入下列物质中,使铜丝变成红色,而且质量仍为mg的是 ( )
A. 稀H2SO4 B. C2H5OH C. CH3COOH溶液 D. NaOH溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列组成生物体的化学元素中属于微量元素的一组是
A. C、H、N、P、Mn B. Cl、Fe、S、N、Mg
C. B、Cu、Zn、Mn、Mo D. N、P、K、Cu、Fe、I
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢气体生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行试验。
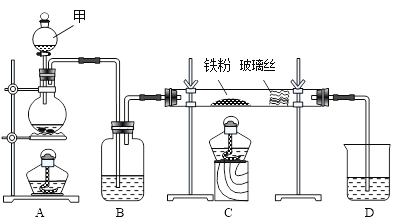
回答下列问题:
(1)制取无水氯化铁实验中,仪器甲的名称为_______________,进行实验时,应先点燃___________(选填A或C)处酒精灯。
(2)制取无水氯化铁的实验中,A中反应的离子方程式为_______________________,装置B中加入的试剂是____________________。
(3)制取的无水氯化铁中混有少量氯化亚铁,其原因是__________________(化学方程式表示)。为除去氯气中混有的少量HCl,可以在装置A、B间加入装有_______________的洗气瓶。
(4)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是_____________(填化学式)。长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_____________(填数字代号)。
① O2 ② Cl2 ③ CO2 ④ HClO
(5)制取无水氯化亚铁实验中,装置A用来制取HCl气体,其化学方程式为:NaCl +H2SO4 (浓) ![]() NaHSO4+ HCl↑,通过装置C后尾气的成分是_________________。若仍用D的装置进行尾气处理,存在的主要问题是_________________________________________。
NaHSO4+ HCl↑,通过装置C后尾气的成分是_________________。若仍用D的装置进行尾气处理,存在的主要问题是_________________________________________。
(6)制取无水氯化亚铁实验中,若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3常用的试剂是________________。(填化学式)欲制得纯净的FeCl2,在实验操作中应先__________________________,再___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物H (结构简式为 )是合成高分子化合物M的单体,H可以通过有机物A (分子式为C7H8O) 和丙酮为原料来进行合成,E为中间产物(结构简式为
)是合成高分子化合物M的单体,H可以通过有机物A (分子式为C7H8O) 和丙酮为原料来进行合成,E为中间产物(结构简式为 )其合成路线如图:
)其合成路线如图:

己知:![]()
请回答下列问题:
(1)A的名称为_________,G 中含氧官能团的名称是________________;①的反应类型是__________。
(2)检验有机物A中官能团的方法为______________________________。
(3)高分子化合物M 的结构简式为____________________。
(4)反应③的化学反应方程式为______________________________。
(5)有机物C有多种同分异构体,其中苯环上只有两个侧链的芳香酯的同分异构体有__________种
(6)已知: ,以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成
,以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成![]() ,此合成路线为
,此合成路线为 ,请完成接下来的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上下注明试剂和反应条件)。____________
,请完成接下来的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上下注明试剂和反应条件)。____________
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。已知铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
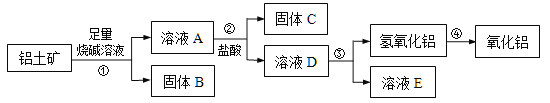
(1)固体B的主要用途有(写出1条即可)________________。
(2)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是________________________________;_______________________________________;
第③步中,用足量氨水制氢氧化铝的化学方程式是________________________________。
(3)将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是__________。(保留一位小数)
(4)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com