
科目: 来源: 题型:
【题目】海水是镁的主要来源之一.从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥;④电解得到产物.
(1)以上提取镁的全过程中,没有涉及的化学反应类型是(填序号).
A.分解反应
B.化合反应
C.置换反应
D.复分解反应
(2)下列关于提取镁的说法中不正确的是(填序号).
A.此法的优点之一是原料来自大海
B.进行①②③步骤的目的是富集MgCl2
C.可用电解熔融氧化镁的方法制取镁
D.电解冶炼镁要消耗大量电能
(3)电解熔融氧化镁制取镁的化学反应方程式 .
(4)③中沉淀物与盐酸反应的离子反应方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各项中的两种物质不论以何种比例混合,只要混合物的总物质的量一定,则完全燃烧消耗O2的物质的量保持不变的是( )
A. C2H6、C2H6O B. C3H6、C2H4 C. C3H4、C2H6O D. C2H4、C2H6O
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物H是合成免疫抑制剂药物霉酚酸的中间体,可由如下路径合成得到. 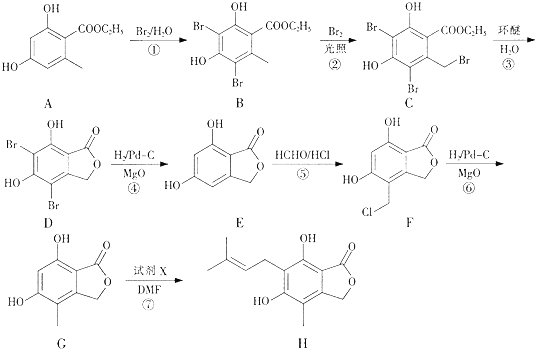
(1)有机物A中的含氧官能团的名称为 .
(2)由C转化为D的反应类型为 .
(3)反应⑦除了得到有机物H外还得到HBr,试剂X的结构简式为 .
(4)步骤⑤可得到副产品有机物J,有机物J和有机物F互为同分异构体,写出有机物J的结构简式:(任写一种).
(5)E的一种同分异构体满足下列条件: Ⅰ.可以发生银镜反应,且能够与NaHCO3反应产生CO2;
Ⅱ.是芳香族化合物,且核磁共振氢谱图显示分子中有4种不同化学环境的氢.
写出该同分异构体的结构简式: .
(6)已知:直接与苯环相连的卤素原子难以与NaOH水溶液发生取代反应.根据已有知识并结合相关信息,写出以 ![]() HCHO为原料制备
HCHO为原料制备 ![]() 合成路线流程图(无机试剂任用).合成路线流程图示例如下: CH3CH2OH
合成路线流程图(无机试剂任用).合成路线流程图示例如下: CH3CH2OH ![]() H2C=C2H
H2C=C2H ![]()
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】科学史上每一次重大发现都极大地推进了科学的发展。门捷列夫对化学的贡献在于( )
A.提取了治疟药物青蒿素
B.开发了合成氨的生产工艺
C.揭示了燃烧的本质
D.提出了元素周期律
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上常用铁碳混合物处理含CuSO4废水获得金属铜。当休持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时问变化的曲线如图所示。下列推论不合理的是
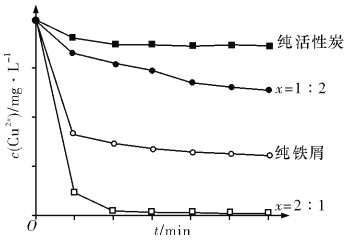
A. 由图可知,活性炭对Cu2+具有一定的吸附作用
B. 铁屑和活性炭会在溶液中形成微电池,铁屑为负极
C. 利用铁碳混合物回收含CuSO4废水中铜的反应原理:Fe+CuSO4=FeSO4+Cu
D. 增大铁碳混合物中铁碳质量比(x),一定会提高废水中Cu2+的去除速率
查看答案和解析>>
科目: 来源: 题型:
【题目】数十年来,化学工作者对碳的氧化物和氢化物做了广泛深入的研究并取得了一些重要成果. 已知:C(s)+O2(g)=CO2(g);△H=﹣393kJmol﹣1
2CO (g)+O2(g)=2CO2(g);△H=﹣566kJmol﹣1
2H2(g)+O2(g)=2H2O(g);△H=﹣484kJmol﹣1
(1)工业上常采用将水蒸气喷到灼热的炭层上实现煤的气化(制得CO、H2),该反应的热化学方程式是 .
(2)上述煤气化过程中需向炭层交替喷入空气和水蒸气,喷入空气的目的是;该气化气可在加热和催化剂下合成液体燃料甲醇,该反应方程式为 .
(3)电子工业中使用的一氧化碳常以甲醇为原料通过脱氢、分解两步反应得到. 第一步:2CH3OH(g)═HCOOCH3(g)+2H2(g)△H>0
第二步:HCOOCH3(g)═CH3OH(g)+CO(g)△H>0
①第一步反应的机理可以用图1表示:图中中间产物X的结构简式为 .
②以甲醇制一氧化碳的反应为反应(填“吸热”、“放热”).
(4)天然气可重整生产化工原料,最近科学家们利用天然气无氧催化重整获得芳香烃X.由质谱分析得X的相对分子质量为106,其核磁共振氢谱如图2,则X的结构简式为 .
(5)C2H4可用于烟气脱硝.为研究温度、催化剂中Cu2+负载量对其NO去除率的影响,控制其他条件一定,实验结果如3图所示.为达到最高的NO去除率,应选择的反应温度和Cu2+负载量分别是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸盐在水溶液中有四种含铁型体,25℃时,它们的物质的量分数随pH的变化如图所示。下列叙述错误的是
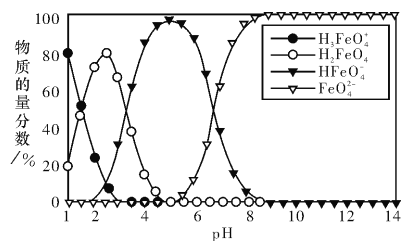
A. 已知H3FeO4+的电离半衡常数分别为:K1=2.5×10-2,K2=4.8×10-4,K3=5.0×10-8,当pII=4吋,溶液中![]()
B. 为获得尽可能纯净的高铁酸盐,应控制pH≥9
C. 向pH=5的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为HFeO4ˉ+OHˉ=FeO42-+H2O
D. pH=2时,溶液中主要含铁型体浓度的大小关系为c(H2FeO4)>c(H3FeO4+)> c (HFeO4ˉ)
查看答案和解析>>
科目: 来源: 题型:
【题目】水泥是重要的建筑材料.水泥熟料的主要成分为![]() 、
、![]() ,并含有一定量的铁、铝和镁等金属的氧化物.实验室测定水泥样品中钙含量的过程如图所示:
,并含有一定量的铁、铝和镁等金属的氧化物.实验室测定水泥样品中钙含量的过程如图所示:

回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸.加入硝酸的目的是________,还可使用________代替硝酸.
(2)沉淀![]() 的主要成分是________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_____________________________________________
的主要成分是________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_____________________________________________
(3)加氨水过程中加热的目的是__________________.沉淀![]() 的主要成分为________、________(填化学式).
的主要成分为________、________(填化学式).
(4)草酸钙沉淀经稀![]() 处理后,用
处理后,用![]() 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:
标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为: ![]() .实验中称取
.实验中称取![]() 水泥样品,滴定时消耗了
水泥样品,滴定时消耗了![]() 的
的![]() 溶液
溶液![]() ,则该水泥样品中钙的质量分数为________.
,则该水泥样品中钙的质量分数为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com