
科目: 来源: 题型:
【题目】2SO2(g)十O2(g)=2SO3(g) △H =-198kJ·mol-1,在V2O3存在时,该反应机理为:V2O3+ SO2-→+2VO3+ SO3(快) 4VO2+O2→2 V2O3(慢)。下列说法正确的是
A. 反应速率主要取决于V2O3的质量 B. VO2是该反应的催化剂
C. 该反应逆反应的活化能大于198kJ/mol D. 升高温度,该反应的△H增大
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下的定容密闭容器中,当下列物理量不再变化时,可表明反应:A(g)+B(g)![]() C(g)+D(g) 已达化学平衡状态的是( )
C(g)+D(g) 已达化学平衡状态的是( )
A. 混合气体的压强 B. B的物质的量浓度 C. 混合气体的密度 D. v(A)正 = v(D)正
查看答案和解析>>
科目: 来源: 题型:
【题目】过碳酸钠( Na2CO4)是一种很好的供氧剂,其与稀盐酸反应的化学方程式为:2Na2CO4+4HCl=4NaCl+2CO2 +O2+2H2O.市售过碳酸钠一般都含有碳酸钠,为测定某过碳酸钠样品(只含Na2CO4和Na2CO3)的纯度,某化学兴趣小组采用以下两种方案实施:
方案一:![]()
(1)操作①和③的名称分别为
(2)上述操作中,使用到玻璃棒的有 __(填操作序号)。
(3)请简述操作③的操作过程
方案二:按下图安装好实验装置,Q为一塑料气袋,随意取适量样品于其中,打开分液漏斗活塞,将稀盐酸滴入气袋中至充分反应。

(4)为测定反应生成气体的总体积,滴稀盐酸前必须关闭 ,打开 (填“K1”、“K2”或“K3”)。导管a的作用是 。
(5)当上述反应停止后,使K1、K3处于关闭状态,K2处于打开状态,再缓缓打开Kl。 B中装的固体试剂是 ,为何要缓缓打开K1? 。
(6)实验结束时,量筒I中有xmL水,量筒Ⅱ中收集到了ymL气体,则样品中过碳酸钠的质量分数是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】为确定FeSO4溶液置于空气中是否变质,所选检验试剂能达到目的是( )
A. NaOH溶液 B. KSCN溶液 C. BaCl2溶液 D. 硝酸钡溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下所示:

(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:________________________
(2)“矿渣”中除了S以外,还有____________(填化学式);“回收S”过程中温度控制在50~60℃之间,不宜过高或过低的原因是____________________________________
(3)“保温除铁”过程中,加入CuO的目的是____________________________________;“蒸发浓缩、冷却结品”过程中,要用HNO3溶液调节溶液的pH,其理由是____________
(4)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为________________________;向“滤液M”中加入(或通入) ____________(填母代号),可得到另一种流程中可循坏利用的物质。
a.铁 b.氯气 c.高锰酸钾![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】碳和氮的化合物在生产、生活中广泛存在。请回答下列问题:
(1)资料显示,可用次氯酸钠处理废水中的氨氮(NH3),使其转化为氮气除去。其主要反应如下
I.NH3(aq)+ HClO(aq)= NH2 Cl(aq)+H2O(1)
II. 2NH2 Cl(aq)+HClO(aq)=N2(g) +H2O(1)+3HCl(aq)
①以上反应中HClO的来源用化学用语解释是__________________________________
②实验测得.废水中pH与氨氮去除率的关系如图所示。pH较高时,氨氮去除率下降的原因是____________________________________
 c
c
(2)甲酶是重要的化工原料,又可作为燃料,工业上可利用CO或CO2来生产燃料甲醇。已知制备甲醇的有关反应的化学方程式及其在不同温度下的化学平衡常数如下表所示。

①下列措施能使反应③的平衡体系中![]() 增大的是________(填字母代号)。
增大的是________(填字母代号)。
A.将H2O(g)从体系中分离出去 B.充人He(g),使体系压强增大
C.升高温度 D.恒容时再充入1mol H2 (g)
②500℃时测得反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度分別为0.8mol·L-1、0.1mol·L-1、0.3mol·L-1、0.15mol·L-1,则此时v(正) ________ (填“>” “=”或“<”) v (逆)
(3)常温下,在(NH4)2C2O4溶液屮,反应NH4++C2O42-+H2O ![]() NH3·H2O+HC2O4ˉ的化学平衡常数K=____________。(已知:常温下,NH3·H2O的电离平衡常数Kb=2×10-5,H2C2O4的电离衡常数Ka1=5×10-2、Ka2=5×10-5)
NH3·H2O+HC2O4ˉ的化学平衡常数K=____________。(已知:常温下,NH3·H2O的电离平衡常数Kb=2×10-5,H2C2O4的电离衡常数Ka1=5×10-2、Ka2=5×10-5)
(4)电解硝酸上业的尾气NO可制备NH4NO3,其工作原理如图所示:

①阴极的电极反应式为____________________________________
②将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为_________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
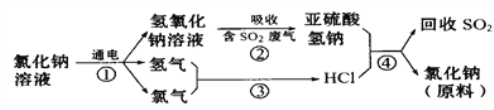
写出反应②的化学方程式______________________________。
(2)亚硫酸氢钠与甲醛经过一定反应,可以合成俗称“吊白块”的物质(该物质对人体有害),其结构简式为HOCH2SO3Na,根据其结构特点,可判断“吊白块”能发生的反应有________。
A.皂化反应 B.加聚反应 C.与金属钠反应 D.氧化反应
(3)近日,中科院大连化物所孙剑、葛庆杰研究员团队发现了二氧化碳高效转化新过程,通过设计一种新型多功能复合催化剂,首次实现了CO2 直接加氢制取高辛烷值汽油(用C5H12表示),试写出该反应的化学方程式____________________________________。
(4)煤的气化和液化属于______________(填“物理”或“化学”)变化。
(5)可燃冰属于新能源,我国是全球第一个成功稳定开采可燃冰的国家某种可燃冰(甲烷水合物)晶体中,平均每46个水分子构成8个分子笼,每个分子笼可容纳1个甲烷分子或1个水分子,若这8个分子笼中有6个容纳的是甲烷分子,另外2个被水分子填充,则这种可燃冰的平均组成可表示为____________
(6)海水中溴含量为65mg·L-1。若1L 海水中有95%的溴元素被氧化为Br2 经热空气吹出,溴单质残留量为3%。最后用SO2 将90%的Br2 还原成Br-,所得溶液体积为50mL,则所得溶液中溴离子浓度为原海水中溴离子浓度的_____________倍(计算结果精确到0.1)。
查看答案和解析>>
科目: 来源: 题型:
【题目】环丁基甲酸是有机合成中一种有用的中间体。某研究小组以丙烯醛为原料,设计了如下路线合成环丁基甲酸(部分反应条件、产物巳省略)。
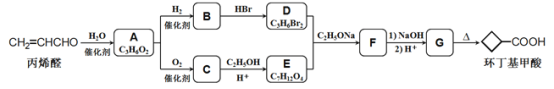
已知:
请回答下列问题:
(1)由丙烯醛生成化合物A的反应类型为____________
(2)化合物C的结构简式是________________________
(3)下列说法中不正确的是____________(填字母代号)。
A.化合物A能与 NaHCO3溶液反应
B.化合物B和C能形成高聚物
C.化合物G的化学式为C6H8O4
D.1mol化合物B与足量金属钠反应能牛成1mol氢气
(4)写出D+E→F的化学方程式:___________________________________
(5)环丁基甲酸与苯酚反应生成一种酯X,化合物X满足下列条件的所同分异构体有____________种,写出其中一种的结构简式:________________________
①能使FeCl3溶液变紫色;
②含有丙烯醛中所有的官能团;
③1H-NMR谱显示分子中含有5种不同化学环境的氢原子
(6)以1,3-丁二烯和化合物E为原料可制备环戊基甲酸![]() ,请选用必要的试剂设计合成路线____________________________________________________________
,请选用必要的试剂设计合成路线____________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com