
科目: 来源: 题型:
【题目】已知:正四面体形分子E和直线形分子G反应,生成四面体形分子L和直线形分子M(组成E分子的元素的原子序数均小于10,组成G分子的元素为第三周期元素)。下列判断中正确的是( )
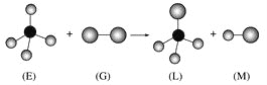
A. 常温常压下,L是一种液态有机物
B. E的二溴代物只有两种结构
C. G具有强氧化性和漂白性
D. 上述反应的类型是取代反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验过程中,始终无明显现象的是
A. NO2通入FeSO4溶液中B. CO2通入CaCl2溶液中
C. NH3通入AgNO3溶液中D. SO2通入Ba(NO3)2溶液中
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质在元素组成上最相似的一组是( )
A. 糖原、胰岛素、性激素 B. 纤维素、性激素、抗体
C. 葡萄糖、脱氧核糖、核糖核酸 D. 磷脂、DNA、RNA
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述不正确的是
A. 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体
B. 煤的干馏和石油的分馏均属化学变化
C. ![]() 可用于文物年代的鉴定,
可用于文物年代的鉴定,![]() 与
与![]() 互为同位素
互为同位素
D. 用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
查看答案和解析>>
科目: 来源: 题型:
【题目】对可逆反应aA(g)+bB(g)cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系: ![]() =K(为一常数),K称为化学平衡常数,其反应的K值只与温度有关.现有反应:CO(g)+H2O (g)CO2(g)+H2(g)△H<0.在850℃时,K=1.
=K(为一常数),K称为化学平衡常数,其反应的K值只与温度有关.现有反应:CO(g)+H2O (g)CO2(g)+H2(g)△H<0.在850℃时,K=1.
(1)若升高温度到950℃时,达到平衡时K1(填“大于”“小于”或“等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和x mol H2 , 则:
①当x=5.0时,上述平衡向(填“正反应”或“逆反应”)方向移动.
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】将物质的量均为3.00mol物质A、B混合于5L容器中,发生如下反应:3A+B2C,在反应过程中C的物质的量分数随温度变化如图所示: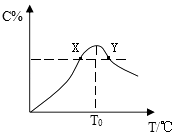
(1)T0对应的反应速率v(正)v(逆)(用“=”、“>”或“<”表示,下同);
(2)此反应的正反应为热;(填“放”或“吸”)
(3)X、Y两点A物质正反应速率的大小关系是YX;
(4)温度T<T0时,C%逐渐增大的原因是:;
(5)若Y点的C的物质的量分数为25%,则参加反应的A物质的量为mol.
查看答案和解析>>
科目: 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是

A. 正极反应为AgCl +e-=Ag +Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目: 来源: 题型:
【题目】将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一.煤转化为水煤气的主要化学反应为:C+H2O(g) ![]() CO+H2 . C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
CO+H2 . C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
①C(s)+O2(g)=CO2(g)△H1=﹣393.5kJmol﹣1;
②H2(g)+ ![]() O2(g)=H2O(g)△H2=﹣242.0kJmol﹣1;
O2(g)=H2O(g)△H2=﹣242.0kJmol﹣1;
③CO(g)+ ![]() O2(g)=CO2(g)△H3=﹣283.0kJmol﹣1;
O2(g)=CO2(g)△H3=﹣283.0kJmol﹣1;
试回答:
(1)请你根据以上数据,写出C(s)与水蒸气反应生成CO和H2的热化学方程式: .
(2)比较反应热数据可知,1molCO(g)和1molH2(g)完全燃烧放出的热量之和,比1molC(s)完全燃烧放出的热量(填“多”或“少”).
甲同学据此认为:“煤炭燃烧时加少量水,可以使煤炭燃烧放出更多的热量”.乙同学根据盖斯定律作出了下列循环图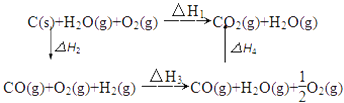
请你写出△H1、△H2、△H3、△H4之间存在的关系式 .
乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同.”请分析:甲、乙两同学的观点正确的是(填“甲”或“乙”)同学,另一同学出现错误观点的原因是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com