
科目: 来源: 题型:
【题目】利用化学反应:Fe+CuSO4==FeSO4+Cu,可以设计出一种原电池。该原电池工作时
A.Fe为正极B.Cu为负极
C.正极上发生氧化反应D.负极上发生氧化反应
查看答案和解析>>
科目: 来源: 题型:
【题目】I.2Al+Fe2O3![]() Al2O3+2Fe在化学反应过程中产生超高热,曾用于钢轨焊接。完成下列填空:
Al2O3+2Fe在化学反应过程中产生超高热,曾用于钢轨焊接。完成下列填空:
(1)氧元素在元素周期表中的位置为_______________,其离子结构示意图为__________。
(2)铝盐常用作净水剂,用文字和化学用语进行解释_______________________________。
(3)氧的非金属性强于氮,用元素周期律知识分析原因_____________________________。
(4)Al2O3与NaOH溶液反应的离子方程式为______________________________________。
II.NH4Al(SO4)2·12H2O水溶液呈_____性(选填“酸”、“碱”或“中”),比较溶液中离子浓度大小c(NH4+)_____c(Al3+)(选填“>”、“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组用题图1装置(夹持装置略)收集某葡萄酒中SO2 , 并对含量进行测定. 
(1)仪器A的名称是 .
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为 .
(3)除去C中过量的H2O2 , 然后用0.0900mol/LNaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的 .
(4)若滴定终点时溶液的pH=8.8,则选择的指示剂为 .
(5)该测定结果往往比实际值偏高,分析是由于采用试剂不当引起的,可能的原因为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨工业中,每生产2molNH3 , 放出92.4kJ热量.
(1)写出合成氨反应的热化学方程式为 .
(2)已知: 
1mol N﹣H键断裂吸收的能量等于kJ.
(3)已知关于铁的氧化物存在下列三个热化学方程式: Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=﹣24.8kJ/mol ①
Fe2O3(s)+ ![]() CO(g)═
CO(g)═ ![]() Fe3O4(s)+
Fe3O4(s)+ ![]() CO2(g)△H=﹣15.73kJ/mol ②
CO2(g)△H=﹣15.73kJ/mol ②
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ/mol ③
则CO还原FeO的热化学方程式为CO(g)+FeO(s)═Fe(s)+CO2(g)△H=kJ/mol.
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组欲测定某已部分变质的小苏打样品中Na2CO3的质量分数,设计如下实验方案。
【方案一】称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为_______________。
(2)实验中,需加热至恒重的目的是_______________。
【方案二】称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-==BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为_______________。
(3)实验中判断沉淀是否完全的方法是_______________。
【方案三】按如下图所示装置进行实验:
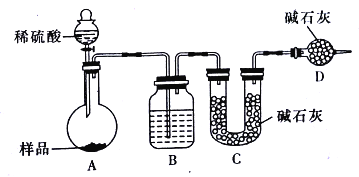
(1)D装置的作用是_______________。分液漏斗中_________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80g,则样品中Na2CO3的质量分数为________________(保留三位有效数字)
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存的在一个明显缺陷是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】侯氏制碱法制造纯碱同时副产氯化铵。在母液处理上,有关说法错误的是
A. 水浴加热,有利于NH4Cl更多地析出
B. 加入食盐,增大Cl-的浓度,使NH4Cl更多地析出
C. 通入氨气,增大NH4+的浓度,使NH4Cl更多地析出
D. 通入氨气,使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 用如图装置电解精炼镁
用如图装置电解精炼镁
B. 用如图装置验证试管中铁丝发生析氢腐蚀
用如图装置验证试管中铁丝发生析氢腐蚀
C. 如图装置中Mg作负极,Al作正极
如图装置中Mg作负极,Al作正极
D. 用如图装置对二次电池进行充电
用如图装置对二次电池进行充电
查看答案和解析>>
科目: 来源: 题型:
【题目】用A、B、C三种装置都可制取溴苯,请仔细分析三套装置,然后回答下列问题。

(1)写出三个装置中都发生反应的化学方程式_____________、________________;写出B的试管中还发生的反应的化学方程式__________________。
(2)装置A、C中长导管的作用是____________________________________________。
(3)B、C装置已连接好,并进行了气密性检验,也装入了合适的药品,接下来要使反应开始,对B应进行的操作是_____________________,对C应进行的操作是__________。
(4)A中存在加装药品和及时密封的矛盾,因而在实验中易造成的不良后果是_______。
(5)B中采用了双球吸收管,其作用是_________________________________________;反应后双球管中可能出现的现象是___________________________;双球管内液体不能太多,原因是__________________________________________。
(6)B装置也存在两个明显的缺点,使实验的效果不好或不能正常进行,这两个缺点是________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】花椒毒素(Ⅰ)是白芷等中草药的药效成分,也可用多酚A为原料制备,合成路线如下:

回答下列问题:
(1)①的反应类型为_____________________;B分子中最多有_________个原子共平面。
(2)C中含氧官能团的名称为______________________;③的“条件a”为____________________。
(3)④为加成反应,化学方程式为__________________________________。
(4)⑤的化学方程式为__________________________________。
(5)芳香化合物J是D的同分异构体,符合下列条件的J的结构共有_________种,其中核磁共振氢谱为五组峰的J的结构简式为_________________。(只写一种即可)。
①苯环上只有3个取代基;②可与NaHCO3反应放出CO2;③1mol J可中和3mol NaOH。
(6)参照题图信息,写出以 为原料制备
为原料制备 的合成路线(无机试剂任选) :______________
的合成路线(无机试剂任选) :______________
查看答案和解析>>
科目: 来源: 题型:
【题目】铬铁矿的成分主要为FeCr2O4,另含有少量Al2O3和SiO2。从铬铁矿中提取铁、铬的化合物,并获得副产物的工艺流程如下:
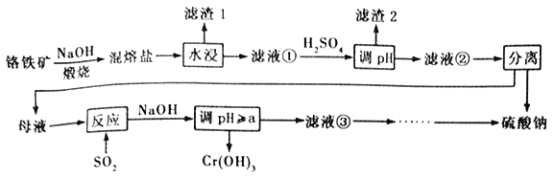
已知“混熔盐”中含有Na2CrO4和NaFeO2,其中NaFeO2极易水解。试回答下列问题:
(1)“滤渣1”为红褐色沉淀,其化学式为_________________;向滤液①中加H2SO4“调pH”的目的:一是使CrO42-转化为Cr2O72- ;二是____________________________。
(2)“煅烧”铬铁矿时,主要反应的化学方程式为_______________________________。
(3)根据右图溶解度(S)~温度(T)曲线判断,对滤液②进行的最佳“分离”方法为_________(填序号)。
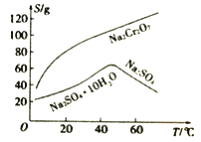
A.蒸发结晶 B.蒸发浓缩,趁热过滤 C.蒸发浓缩,冷却结晶,过滤
(4)“反应”的离子方程式为_______________________________。
(5)Cr(OH)3溶于盐酸生成配离子[CrCln(H2O) 6-n]x+。0.0015 mol [CrCln(H2O) 6-n]x+与氢离子交换树脂(HR)完全发生离子交换:
[CrCln(H2O) 6-n]x++xHR→Rx[CrCln(H2O) 6-n]+xH+,生成的H+可与25.00 mL0.1200 mol·L -1NaOH溶液恰好中和。则该配离子的化学式为__________________。
(6)已知25℃时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=1.0×10-32。则使Cr3+恰好完全沉淀,即溶液中c(Cr3+) =1.0×10-5 mol·L -1时,应调节溶液pH的最小值a为多少? (列式计算)____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com