
科目: 来源: 题型:
【题目】已知25°时,乙酸和三氯乙酸的电离常数分别是:Ka(CH3COOH)═1.80×10﹣5 , Ka(CCl3COOH)═0.60,在物质的量浓度均为0.1molL﹣1的CH3COONa和CCl3COONa混合溶液中,下列关系正确的是( )
A.c(Na+)═c(CCl3COO﹣)+c(CH3COO﹣)
B.c(CCl3COO﹣)﹣c(CH3COO﹣)═c(CH3COOH)﹣c(CCl3COOH)
C.c(OH﹣)>c(CCl3COO﹣)>c(CH3COO﹣)
D.c(CH3COOH)>c(CCl3COOH)>c(OH﹣)
查看答案和解析>>
科目: 来源: 题型:
【题目】取三张蓝色石蕊试纸用蒸馏水润湿后贴在玻璃片上,然后按顺序分别滴加足量的浓硝酸、浓硫酸和浓盐酸,三张纸最终变成( )
A.白色、红色、红色
B.红色、红色、红色
C.红色、黑色、白色
D.白色、黑色、红色
查看答案和解析>>
科目: 来源: 题型:
【题目】食用醋中含有乙酸。下列关于乙酸的说法正确的是( )
A.结构简式为:C2H4O2 B.分子式为:CH3COOH
C.可与金属Na反应生成H2 D.分子中原子之间只存在单键
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钇(Y)具有重要的国防价值,但因过度开采已濒临枯竭。通过硫酸浸泡深海磷灰石矿,可以得到Y3+的浸出液:
表1 浸出液成分
Al3+ | Fe3+ | Ca2+ | PO43- | Mg2+ | Mn2+ | Y3+ | |
浓度/(mgL-1) | 7670 | 9460 | 550 | 640 | 5600 | 1500 | 70.2 |
(1)浸出液可用有机溶剂(HR)进行萃取,实现Y3+的富集(已知:Y3+与Fe3+性质相似),原理如下:Fe3+ + 3HR ![]() FeR3 + 3H+ Y3+ + 3HR
FeR3 + 3H+ Y3+ + 3HR ![]() YR3 + 3H+ (已知:FeR3、YR3均易溶于HR)
YR3 + 3H+ (已知:FeR3、YR3均易溶于HR)
浸出液在不同pH下萃取的结果如图1。
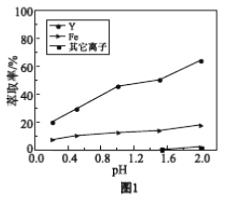
①用化学平衡原理解释,随pH增大,Y3+萃取率增大的原因________。
②结合图1解释,工业上萃取Y3+之前,应首先除去Fe3+的原因是________。
(2)采用“中和沉淀法”和“磷酸法”可以除铁。
表2 Fe3+、Y3+去除率
终点pH | 去除率/% | |
Fe3+ | Y3+ | |
3.0 | 87.84 | 19.86 |
3.5 | 92.33 | 23.63 |
4.5 | 99.99 | 44.52 |
5.0 | 99.99 | 89.04 |
中和沉淀法:向浸出液中加入NaOH除Fe3+,去除率如表2所示。
①该实验条件下,Fe3+去除率比Y3+大的可能原因________。
磷酸法:将磷酸(H3PO4:三元弱酸)加入到浸出液中,再加入Na2CO3溶液,调pH为2.5,过滤除去磷酸铁沉淀(FePO4),滤液中剩余的Fe3+、Y3+浓度如表3。
表3 滤液中Fe3+、Y3+的浓度
Fe3+ | Y3+ | |
浓度/(mgL-1) | 508 | 68.9 |
② 配平“磷酸法”除铁过程中的离子方程式
Fe3+ + + = FePO4↓+ CO2↑+ ,___________________
③ 综合分析表1、表2、表3,工业上采用“磷酸法”除铁的原因________。
(3)经“磷酸法”除铁后,用有机溶剂HR萃取Y3+,可通过________(填操作)收集含Y3+的有机溶液。
(4)综合分析以上材料,下列说法合理的是________。
a. 分析图1可知,pH在0.2~2.0范围内,有机溶剂中的Fe3+多于水溶液中的Fe3+
b. 表2中 Y3+损失率在20%左右的原因可能是生成的Fe(OH)3对Y3+的吸附
c. 表2中 pH在4.5~5.0范围内,Y3+损失率变大的可能原因:Y3+ + 3OH- = Y(OH)3↓
d. 有机溶剂萃取Y3+的优点是Ca2+、Mg2+、Mn2+等金属离子萃取率极低
查看答案和解析>>
科目: 来源: 题型:
【题目】在强酸性溶液中可大量共存的离子组是( )
A.Na+、K+、Cl-、F-
B.Fe2+、ClO-、NO3-、Na+
C.Fe2+、Mg2+、SO42﹣、Cl-
D.CO32﹣、SO42﹣、Na+、K+
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2的绿色减排、捕捉、转化是人类可持续发展的重要战略之一。
(1)CO2来源之一是汽车尾气
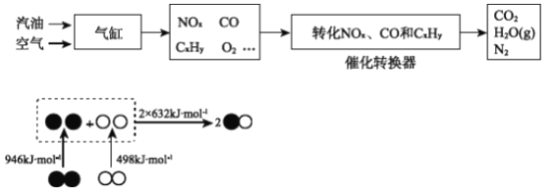

①根据上图,写出气缸内产生NO的热化学方程式________。
②写出转换器中在催化剂作用下NOx和CO反应的化学方程式________。
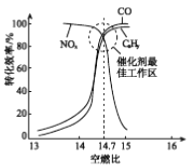
③在催化转换器中机动车尾气转化效率与空燃比(空气与燃油气的体积比)的关系如右图。若空燃比小于14.7,氧气不足,CxHy和CO不能被完全氧化,导致其转化效率降低;若空燃比大于14.7,则NOx的转化效率降低,原因是________。
(2)利用NaOH溶液可以“捕捉” CO2
已知:0.448L CO2(已折算标准状况)被NaOH溶液充分吸收,得到100mL含有Na2CO3和NaHCO3的吸收液。
①向吸收液中加入足量BaCl2溶液得到沉淀,经过滤、洗涤、干燥后,称重为1.97g,则吸收液中c(Na2CO3) = ________。(该条件下NaHCO3与BaCl2不反应)
②对该吸收液,下列判断正确的是________。
a . c (CO32- ) > c (HCO3- )
b. 2c (CO32- ) + c (HCO3- ) + c (OH- ) = c (H+ ) + c (Na+ )
c. c (H2CO3) + c (HCO3- ) + c (CO32- ) =0.2molL-1
(3)工业上可用CO2来制甲醇
①CO2 (g) + 3H2(g) ![]() CH3OH(g) + H2O(g) ΔH < 0
CH3OH(g) + H2O(g) ΔH < 0
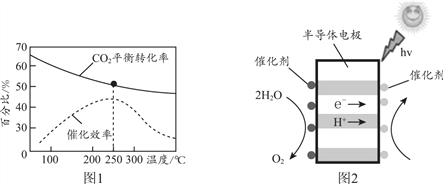
根据图1分析,实际工业生产中,反应温度选择250℃的理由________。
②利用光电催化原理,由CO2和H2O制备CH3OH的装置如图2。写出右侧的电极反应式________。
查看答案和解析>>
科目: 来源: 题型:
【题目】匹多莫德是一种免疫调节剂,其合成路线如下:

已知:i ![]()
ii ![]()
(1)A中官能团名称________。
(2)B的结构简式________。
(3)②的反应类型________。
(4)写出谷氨酸生成F的化学方程式________。
该过程,还可能生成高聚物,写出任意一种的结构简式________。
(5)③的化学方程式________。
(6)写出半胱氨酸与HCHO反应生成G的化学方程式________。
(7)结合信息,写出以乙醇和必要无机试剂合成![]() 的路线________。
的路线________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知: 2NO2(g)+ CH4(g)![]() N2(g)+ CO2(g)+ 2H2O(g) ΔH,向容积为2L的恒容密闭容器中,充入NO2和CH4的混合气体0.3mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如右图所示。[投料比=
N2(g)+ CO2(g)+ 2H2O(g) ΔH,向容积为2L的恒容密闭容器中,充入NO2和CH4的混合气体0.3mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如右图所示。[投料比=![]() ] ;下列说法不正确的是
] ;下列说法不正确的是

A. ΔH < 0
B. X > 2
C. 400K时,反应的平衡常数为5×10-2
D. 投料比为2时,Q点v逆(CH4)小于P点的v逆(CH4)
查看答案和解析>>
科目: 来源: 题型:
【题目】利用如图所示装置进行下列实验,现象和结论均正确的是
选项 | ① | ② | ③中现象 | 结论 | 装置图 |
A | 浓硝酸 | Cu | 淀粉-KI溶液变蓝 | NO2为氧化性气体 |
|
B | 稀硫酸 | Na2SO3 | 品红溶液褪色 | Na2SO3未变质 | |
C | 浓盐酸 | MnO2 | FeBr2溶液变为黄色 | 氧化性:Cl2>Br2 | |
D | 浓氨水 | NaOH | 湿润红色石蕊试纸变蓝 | NH3为碱性气体 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】高聚物(L)是一种来源于生物学灵感的新型粘合剂,其原料取材于植物和贻贝。下列关于高聚物(L)的说法中不正确的是

A. 单体之一为![]()
B. 在一定条件下能发生水解反应
C. 生成1mol L的同时,会有(x+y-1)mol H2O生成
D. 1mol L最多可与3mol H2发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com