
科目: 来源: 题型:
【题目】如图所示装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡.试回答: 
(1)a为极,d极的电极反应式为: .
(2)电解开始时,在B烧杯的中央滴几滴淀粉溶液,你能观察到的现象是 . 电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应为: .
(3)当d电极上收集到44.8ml气体(标准状况)时停止电解,若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】(以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2 , 负极通入丙烧,电解质是熔融碳酸盐,电池总反应方程式为:C3H8+5O2═3CO2+4H2O.
(1)已知:2C3H8(g)+7O2(g)═6CO(g)+8H2O(l)△H1C(s)+O2(g)═CO2(g)△H2
2C(s)+O2(g)═2CO(g)△H3
则 C3H8(g)+5O2((g)═3CO2(g)+4H2O(l)△H=(用△H1、△H2、△H3表示)
(2)写出该电池正极的电极反应式:,电池工作时CO32﹣移向(填“正极”或“负极”);用该电池电解1000mL lmol/L的AgNO3溶液(惰性电极),此电解池的反应方程式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以钴以Co2O3CoO的形式存在,吸附在铝箔的单面或双面,锂混杂于其中.从该废料中回收(CoO) 的工艺流程如图: 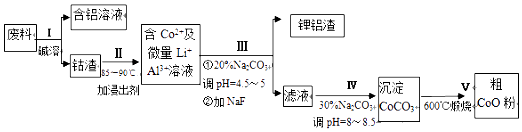
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 .
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴.则浸出钴的化学反应方程式为(产物中只有一种酸根) . 在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴的主要原因 .
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3 , 碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式 .
(4)碳酸钠溶液在过程III和IV中所起作用有所不同,请写出在过程IV中起的作用是 .
(5)在Na2CO3溶液中存在多种粒子,下列各粒子浓度关系正确的是(填序号).
A.c(Na+)=2c(CO32﹣)
B.c(Na+)>c(CO32﹣)>c(HCO3﹣)
C.c(OH﹣)>c(HCO3﹣)>c(H+)
D.c(OH﹣)﹣c(H+)=c(HCO3﹣)+2c(H2CO3)
查看答案和解析>>
科目: 来源: 题型:
【题目】温度时,用惰性电极电解硝酸钠的不饱和溶液.若两极板收集到气体总体积为22.4aL时,剩余溶液恢复至原温度,析出溶质mg(溶质不带结晶水);若两极收集到气体总体积为33.6aL时,剩余溶液恢复至原温度,析出溶质ng.则硝酸钠在该温度时的溶解度是(气体体积均已折合为标准状况下的体积)( )
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g) + 4NH3(g) ![]() 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。
①能说明该反应已达到平衡状态的标志是_______
a.反应速率![]() ( NH3) =
( NH3) =![]() ( N2)
( N2)
b.容器内压强不再随时间而发生变化
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
②某次实验中测得容器内NO及N2的物质的量随时间变化如图所示,图中b点对应的速率关系是![]() (正)____
(正)____![]() (逆)(填“﹥”、“﹤”或“﹦”),d点对应的速率关系是
(逆)(填“﹥”、“﹤”或“﹦”),d点对应的速率关系是![]() (正)____
(正)____![]() (逆)(填﹥、﹤或﹦)。
(逆)(填﹥、﹤或﹦)。

(2)298 K时,若已知生成标准状况下2.24 L NH3时放出热量为4.62 kJ。写出合成氨反应的热化学方程式_______。在该温度下,取1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量总小于92.4 kJ,其原因是________。
(3)一定条件下,在2 L密闭容器内,反应2NO2(g)![]() N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
选项 | 加入的金属 | 是否有气体产生 |
A | 铜 | 有 |
B | 铁 | 有 |
C | 铝 | 无 |
D | 镁 | 无 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】锌和二氧化锰是电池工业中主要原料,其中一种Zn﹣MnO2同槽电解的工业生产试验工艺流程涉及的主要反应有: ①MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O
②MnSO4+ZnSO4+2H2O ![]() MnO2+Zn+2H2SO4
MnO2+Zn+2H2SO4
下列说法正确的是( )
A.①中MnO2是氧化剂,ZnSO4是还原产物
B.①中每产生16gS时转移电子的物质的量为2mol
C.按照②电解时,生成MnO2的电极为阴极
D.该工艺流程中H2SO4可循环
查看答案和解析>>
科目: 来源: 题型:
【题目】某氧化物与 NaOH 溶液反应生成易溶于水的化合物 M,将少量 M 溶液滴入稀盐酸中,有白色沉淀产生,则该氧化物是
A.Fe2O3B.SiO2C.A12O3D.MgO
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.1molH2O的质量是18g
B.氮原子的质量就是氮的相对原子质量
C.1molH2SO4中含1molH2
D.氢氧化钠的摩尔质量是40g
查看答案和解析>>
科目: 来源: 题型:
【题目】下面所写的有机反应方程式及其类型都正确的是
A.  取代反应
取代反应
B. 2CH3CHO+ O2 → 2CH3COOH 氧化反应
C. CH2=CH2 + Br2 → CH3CHBr2 加成反应
D. HCOOH + CH3CH2OH ![]() HCOOCH3CH2+ H2O 取代反应
HCOOCH3CH2+ H2O 取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com