
科目: 来源: 题型:
【题目】下列物质的熔、沸点高低顺序正确的是( )
A. 金刚石,晶体硅,二氧化硅,碳化硅 B. CI4>CBr4>CCl4>CH4
C. MgO>KCl>Hg>I2>O2 D. 金刚石>生铁>纯铁>钠
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
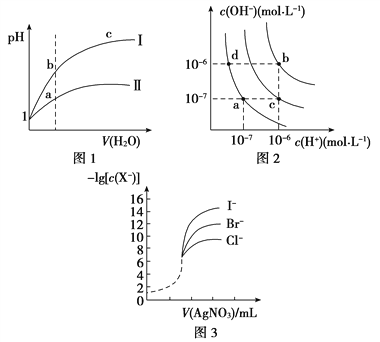
A. 图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B. 图2中纯水仅升高温度,就可以从a点变到c点
C. 图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
D. 用0.010 0 mol/L硝酸银标准溶液,滴定浓度均为0.100 0 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是
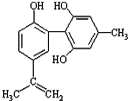
A.该物质与苯酚属于同系物,遇FeCl3溶液呈紫色
B.滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
C.该分子中的所有碳原子不可能共平面
D.1mol此物质分别与浓溴水和H2反应时最多消耗Br2和H2为4mol和7mol
查看答案和解析>>
科目: 来源: 题型:
【题目】作为工业生产的催化剂和制备纳米MgO的材料,草酸镁(MgC2O4·2H2O)有着广阔的应用和发展前景。回答下列问题:
(1)MgC2O4·2H2O的制备

已知氯化镁、草酸铵、草酸镁在水中的溶解度如下表:
氯化镁 | 草酸铵 | 草酸镁 | |
20℃ | 54.6g | 4.45g | 微溶 |
70℃ | 61.0g | 22.4g | |
100℃ | 73.3g | 34.7g |
实验方法:(i)加热煮沸蒸馏水,取300mL冷却至70℃,加140g MgCl2·6H2O,此制MgCl2溶液;
(ii)按照图示装置装好药品,连接好装置;
(iii)在磁力加热搅拌的情况下,缓缓滴入饱和(NH4)2C2O4溶液,并水浴加热,直至不再产生白色沉淀为止;
(iv)分离沉淀、洗涤,得MgC2O4·2H2O晶体。
①装置中仪器甲的名称是_____,其冷水进水口为_____填“a”或“b”)。
②仪器乙中c部位的作用是____________________。
③检验产品洗涤干净的方法是________________。
(2)MgC2O4·2H2O分解产物的探究
利用下图所示装置探究MgC2O4·2H2O分解产物CO、CO2 等的性质。
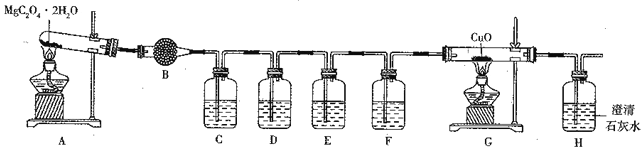
①A中发生反应的化学方程式为______________________。
②装置B中盛装的药品是_____,装置C的作用是______,装置D中的试剂是______,装置G中的现象是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机化合物M是一种治疗恶性肿瘤的合成药物。制备M的一种合成路线如图所示:

已知:  (R为烃基)。
(R为烃基)。
(1)A的化学名称是________。
(2)由A生成B和B生成C的反应类型分别是_________、________。
(3)由C生成D的化学方程式是____________________。
(4)写出E的结构简式:________,X是E的同分异构体,且X满足下列条件:
①能发生银镜反应;②遇浓FeCl3溶液变色;③分子结构中只含一个碳环结构。
符合上述条件的X有_____种,其中核磁共振氢谱显示有5种不同化学环境的氢,峰面积比为2:2:2:1:1的结构简式是_____________。
(5)根据题给信息,写出用CH3CHO和 为原料制备
为原料制备 的合成路线:_________________(其他试剂任选)。
的合成路线:_________________(其他试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A.实验用过的药品可以不经过处理直接丢弃
B.易分解实验药品应存放在无色玻璃瓶中
C.凡是给玻璃仪器加热,都要加垫石棉网,以防止仪器炸裂.
D.实验室制备有毒有害气体需要在通风橱中进行,必须对尾气进行吸收或处理,防止中毒或污染大气。
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒容密闭容器中,可逆反应C(s)+CO2(g)![]() 2CO(g),达到平衡状态的标志是
2CO(g),达到平衡状态的标志是
A. 单位时间内生成nmolCO2的同时生成2nmolCO
B. 单位时间内生成nmolCO2的同时生成nmolC
C. 混合气体的密度不再改变的状态
D. 混合气体的压强不再改变的状态
查看答案和解析>>
科目: 来源: 题型:
【题目】铜和硫的化合物在化工、医药材料等领域具有广泛的用途。回答下列问题:
(1)原子轨道是指电子在原子核外的___________,基态S原子的原子轨道数是____个。
(2)基态Cu原子中,核外电子占据的原子轨道为球形的最高能级符号是______,占据该能级的电子数为__________。
(3)Cl、S、Se在元素周期表中处于相邻的位置,其第一电离能的大小顺序为_______。
(4)下图是含元素Cu、S的有机物的结构简式:

①该有机化合物结构中含有的化学键类型是_______(填“共价键““离子键”或“共价键、离子键”)、配位键,其中1个该有机物分子中配位键数为_____个,这些配位键中提供孤电子对的元素是__________。
②S原子的杂化方式为_______、带*N原子的杂化方式为_______。
(5)下图是Cu-Au合金的一种立方晶体结构:

已知该合金的密度分dg/cm3,阿伏加德罗常数的值为NA,若Au原子的半径为bpm(lpm=10-10cm),则铜原子的半径为______cm(写出计算表达式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】NaClO2(亚氯酸纳)是常用的消毒剂和漂白剂,工业上可采用电解法制备,工作原理如图所示。下列叙述正确的是
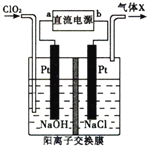
A. 若直流电源为铅蓄电池,则b极为Pb
B. 阳极反应式为ClO2+e-=ClO2-
C. 交换膜左测NaOH的物质的量不变,气体X为Cl2
D. 制备18.1gNaClO2时理论上有0.2molNa+由交换膜左侧向右侧迁移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com