
科目: 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
实验编号 | HA物质的量浓度 | NaOH物质的量浓度 | 混合溶液的pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | c | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸 .
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2(选填“是”或“否”).混合液中离子浓度c(A﹣)与 c(Na+)的大小关系是 .
(3)丙组实验结果分析,HA是酸(选填“强”或“弱”).该混合溶液中离子浓度由大到小的顺序是 .
(4)丁组实验所得混合溶液中由水电离出的c(OH﹣)=molL﹣1 . 写出该混合溶液中下列算式的精确结果(不需做近似计算).c(Na+)﹣c(A﹣)=molL﹣1 c(OH﹣)﹣c(HA)=molL﹣1 .
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液能与锌片作用产生H2 , 则该溶液中可以大量共存的离子组是( )
A.Na+、NO3﹣、K+、Fe2+
B.Fe2+、Na+、SO42﹣、K+
C.K+、I﹣、NO3﹣、H+
D.NH4+、NO3﹣、Na+、HCO3﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】如表物质与其所含化学键类型、所属化合物类型完全正确的一组是( )
选项 | A | B | C | D |
物质 | CaCl2 | H2O2 | AlCl3 | NH4Cl |
所含化学键类型 | 离子键、共价键 | 共价键 | 离子键 | 离子键、共价键 |
所属化合物类型 | 离子化合物 | 共价化合物 | 离子化合物 | 共价化合物 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、W、D、E为短周期元素,且原子序数依次增大,五种元素核内质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)A2W的电子式为________。
(2)B中质子数和中子数相等的核素符号为____,E元素在周期表中的位置为_______ 。
(3)W、D、E三种元素的简单离子半径由小到大的顺序为_______(填离子符号)。
(4)在一定条件下,D元素的单质能与A元素的单质化合生成DA,DA能与水反应放氢气,则其化学方程式为_______,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是______L(标准状况下)。
(5)若要比较D和E的金属性强弱,下列实验方法可行的是_______。
a.将D单质置于E的盐溶液中,若单质D不能置换出单质E,说明D的金属性弱
b.将少量D、E的单质分别投入到水中,若D反应而E不反应,说明D的金属性强
C.比较相同条件下D和E的最高价氧化物对应水化物的溶解性若前者比后者溶解度大,说明D的金属性强
查看答案和解析>>
科目: 来源: 题型:
【题目】某新型有机酰胺化合物M在l业生产中有重要的作用,其合成路线如下:

已知:①A是烃的含氧衍生物,相对分子质量为58,碳和氢的质量分数之和为44.8%,核磁共振氢谱显示为一组峰,可发生银镜反应。
②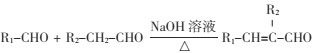
③![]()
④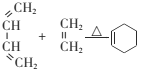
回答下列问题:
(1)E的结构简式为 ___,G的名称为_____
(2)B中含有官能团的名称为_______。
(3)C-D的反应类型为 ___。
(4)写出 F+H—M的化学反应方程式____。
(5)芳香族化合物W有三个取代基,是C的同分异构体,能与FeCl3溶液发生显色反应。 0.5 molW可与足量的Na反应生成1gH2,H核磁共振氢谱显示为五组峰,符合以上条件的W的同分异构体共有___ 种,写出其中一种的结构简式____。
(6)参照上述合成路线.以CH2=CH2和HOCH2CH2OH为原料(无机试剂任选),设计制备![]() 的合成路线________。
的合成路线________。
查看答案和解析>>
科目: 来源: 题型:
【题目】H、N、Na、Al、Ti等元素在能源、材料等领域应用广泛。回答下列问题:
(一)氢化铝钠( NaAlH4)是一种新型轻质储氢材料,掺人少量Ti的NaAlH4在150℃时释氢,在170℃、15.2 MPa条件下又重复吸氢。NaAlH4可南AlCl3和NaH在适当条件下合成。NaAlH4的品胞结构如右图所示,为长方体。

(1)基态Ti原子的价电子排布式为 ___,L能层中电子云的形状有___ 种。
(2)AlCl3在178℃时升华,属于____晶体,其蒸气的相对分子质量约为267,蒸气分子的结构式为____(标明配位键),其中Al原子的杂化方式为_______。
(3)写出与AIH4-空间构型相同的-种分子和一种离子_________(填化学式)。
(4)NaAlH4晶体中,与AlH4紧邻且等距的Na+有_______个;NaAlH4晶体的密度为 _____g/cm3(用含n的代数式表示)。
(二)叠氮化钠和氢叠氮酸( HN3)已一步步进入我们的生活,如汽车安全气囊等。
(5)写出与N3-互为等电子体的一种分子_____填分子式)。
(6)氢叠氮酸(HN3)可由肼(N2H4)被HNO2氧化制得,同时生成水。下列叙述错误的是______(填标号)
A.上述生成HN3的化学方程式为:N2H4+HNO2=HN3+2H2O
B.NaN3的晶格能大于KN3的晶格能
C.氢叠氮酸(HN3)和水能形成分子间氢键
D.HN3和N2H4都是由极性键和非极性键构成的非极性分子。
E.HN3分子中四个原子可能在一条直线上
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物的结构简式如图所示, 下列说法中不正确的是( )

A. 1mol该有机物和过量的金属钠反应最多可以生成1.5 molH2
B. 该有机物消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2
C. 可以用酸性KMnO4溶液检验其中的碳碳双键
D. 该有机物能够在催化剂作用下发生酯化反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在通常情况下能大量共存,并且可以用浓硫酸干燥的一组气体是( )
A.SO2、H2S、O2
B.CO、H2、Cl2
C.NO、H2、O2
D.HCl、CO、NH3
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.
(1)甲池是装置.
(2)乙池中A(石墨)电极的名称是 .
(3)写出通入CH3OH的电极的电极反应式: .
(4)乙池中反应的化学方程式为 .
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况);此时丙池某电极上析出1.60g某金属,则丙池中的某盐溶液可能是(填序号).
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3 .
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下:甲分子和乙分子反应生成丙分子和丁分子,下列说法不正确的是( ) 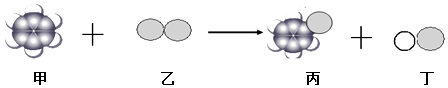
A.分离甲和丙可以采用蒸馏法
B.甲的空间构型是平面正六边形
C.丙不属于烃类物质
D.该反应类型是置换反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com