
科目: 来源: 题型:
【题目】下列离子在水溶液中能大量共存的是( )
A.Na+、Cl﹣、HCO3﹣、Ca2+
B.OH﹣、Na+、Mg2+、HCO3﹣
C.Na+、Cl﹣、H+、Ag+
D.Na+、SiO32﹣、H+、Cl﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】某课题组为了深入探究二氧化硫的性质设计以下装置进行了实验。
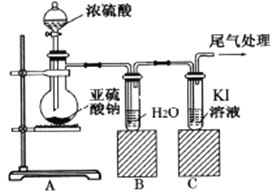
步骤一:检验装置气密性后向B、C中各加入20mL图示液体。
步骤二 :打开A中活塞,反应进行10分钟后关闭活塞。
步骤三:用pH计分别测量B、C 试管中溶液的pH。
结合上述实验,回答以下问题:
(1) 甲同学认为两瓶中pH大致相等,原因是二氧化硫溶于水后生成了酸性物质。该物质发生电离,其电离方程式为___________。
(2) 乙同学认为C瓶中pH可能更小,因为C中二氧化硫会像氧化硫化氢一样与碘离子发生氧化还原反应。通过pH计测定,B瓶中pH为2.13,C瓶中pH为1.05。为了解释该实验现象,该同学提出进行多次平行实验,目的是____________。测定结果如下:
第1次实验 | 第2次实验 | 第3 次实验 | |
B 瓶中pH | 2.15 | 2.10 | 2. 17 |
C 瓶中pH | 1.10 | 1.12 | 1.09 |
实验发现: C瓶中溶液的酸性始终比B瓶中的酸性强。
(3) 通过仔细观察,C瓶中溶液从无色变成浅黄色同时出现黄色浑浊,继续通入气体溶液又逐渐变为无色。其中溶液变黄且出现浑浊的过程对应的离子方程式为________,为了检验产物,中间取出少许溶液加入______,溶液变蓝,证明乙同学判断正确;黄色溶液又逐渐变为无色对应的化学反应方程式为_______________。
(4) 最终结论:
①B瓶中溶液呈弱酸性是由于__________。
②C瓶中溶液呈强酸性是由于生成了_________,该过程中体现出二氧化硫哪些化学性质_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应一定属于放热反应的是( )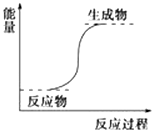
A.氢氧化钡晶体和氯化铵晶体的反应
B.能量变化如图所示的反应
C.化学键断裂吸收的能量比化学键形成放出的能量少的反应
D.不需要加热就能发生的反应
查看答案和解析>>
科目: 来源: 题型:
【题目】【化学-选修5:有机化学基础】
尼龙-6(聚-6-氨基已酸)和尼龙-66(聚己二酸己二胺) 是两种常用的有机高分子纤维,是目前世界上应用最广、产量最大、性能优良的合成纤维。其合成路线如下:
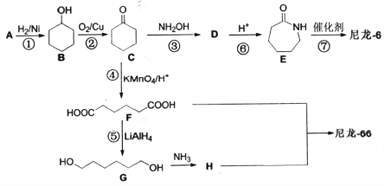
已知:a.A是一种常见的酸性工业原料b. 
请回答以下问题:
(1)C与H中所含的官能团名称分别为_______、_______。
(2)A的结构简式为___________。
(3)合成路线中与D互为同分异构体的化合物是____(填写分子代号),与第②步的反应类型相同的反应步骤是___。
(4)合成尼龙-66的化学反应方程式为________ 。
(5)写出F的同分异构体中所有满足下列条件的物质的结构简式_______。
a.能发生水解反应,且1mol该物质能与2mol银氨溶液发生银镜反应;
b.能与碳酸氢钠溶液反应产生气泡;
c.核磁共振氢谱显示4组峰,氢原子个数比为1:1:2:6。
(6)因为分子结构中含有-NH2,这两种尼龙作为纺织材料时经常采用_____进行印染。(填“酸性染料“或“碱性染料”)
(7)结合上述合成路线,由已知化合物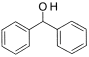 设计路线合成
设计路线合成 (其余小分子原料自选)。
(其余小分子原料自选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)![]() N2O4g)(无色),如图所示.
N2O4g)(无色),如图所示.

(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(Ls),乙中v(N2O4)=6mol/(Lmin),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4) |
B.容器内压强不再发生变化 |
C.X的体积分数不再发生变化 |
D.容器内气体原子总数不再发生变化 |
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W、R是5种短周期元素,原子序数依次增大。已知X组成的单质是最理想的气体燃料,Y是形成化合物种类最多的元素,Z的原子最外层电子数是次外层电子数的3倍,W、R处于同一周期,W是该周期中金属性最强的元素,W与R能形成化合物WR.
请回答下列问题:
(1)Z在周期表中的位置是_________;R的原子结构示意图是_____________。
(2)工业上用化合物WR冶炼W的单质,若要得到2.3tW,至少需要WR的质量是_____。
(3)W与Z形成的化合物W2Z2可作供氧剂,该化合物含有的化学键类型有________________,其反应原理是_______________________________(用化学方程式表示)
(4)在一定条件下,R单质能与硫反应生成一种用途广泛的硫化剂S2R2;S2R2与足量水反应有黄色沉淀生成,同时生成能使品红溶液褪色的无色气体,则该反应的化学方程式是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知元素A、B、C均为前三周期的元素,其中A、B同主族,B是其同周期中原子半径最大的元素。C与A、B均不在同一周期,且与C同主族的某金属的氧化物具有两性。请回答:
(1)A、B、C 三种元素中第一电离能最小的元素是______ (填元素符号),其基态原子核外电子排布为______________。
(2)C元素的单质可与Cl2反应生成CCl3,该分子为_____结构,是_____(填“极性分子”“非极性分子”),与水反应剧烈产生“白烟”,其方程式为______________。
(3)A、B两种元素可形成化合物X,写出X的电子式_______。
(4)A、C两种元素可形成化合物Y(C2A6),其中心原子的杂化方式为_______。
(5)A、.B、C三种元素组成的化合物Z(分子式为BCA4),该物质曾作为一种还原剂,这是由于A 的价态为__________。
(6)Z形成的晶体属于立方晶系,晶胞参数为apm,其晶体类型为______,晶胞如下图所示(图中A原子被省略),在此晶胞中,含有_____个B原子。晶胞密度表达式为____ g·cm-3 (用a和NA表示)。

查看答案和解析>>
科目: 来源: 题型:
【题目】如图是人类从海水资源中提取某些重要化工原料的流程示意图:
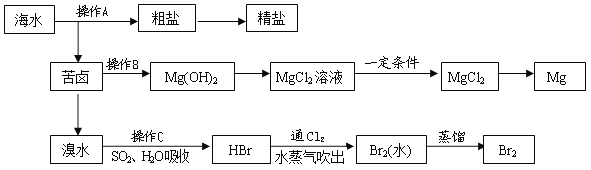
请回答下列问题:
(1)操作A是__________________和过滤(填实验基本操作名称)
(2)操作B需加入下列试剂中的一种,最合适的是________(选填编号)
A. 氢氧化钠溶液 B. 澄清石灰水
C. 石灰乳 D. 碳酸钠溶液
(3)向苦卤中通入Cl2,发生反应的离子方程式是_____________________,用SO2水溶液吸收Br2 ,吸收率可达95%,有关反应的离子方程式为___________________。
(4)工业上由无水MgCl2制取镁的化学方程式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】天然气( 主要成分为甲烷)是一种高效的清洁能源,也是一种重要的化工原料,利用天然气制备甲醇、乙醇、二甲醚(CH3OCH3)、乙烯(C2H4)等物质的主要反应有:
①CH4(g)+H2O(g)=CO(g)+ 3H2(g) △H1= + 206.2 kJ/ mol
②CO(g)+2H2(g)=CH3OH(g) △H2=- 90.1kJ/ mol
③2CH3OH(g) = CH3OCH3(g) + H2O(g) △H3=- 24.5kJ/ mol
④2CH3OH(g) ![]() C2H4(g) + 2H2O(g) △H4=- 29.1kJ/ mol
C2H4(g) + 2H2O(g) △H4=- 29.1kJ/ mol
⑤CH3OCH3(g)== C2H5OH(g) △H5=- 50.7 kJ /mol
请回答下列问题:
(1)反应2CH4(g)+H2O(g)= C2H5OH(g)+2H2(g)的△H =______kJ/mol;根据化学原理,可 以同时加快该反应的速率和提高甲烷转化率的措施有_______________________。

(2)CO与H2在一定条件下,同时发生②和③的反应,产生二甲醚的结果如上图所示。260℃时,CO转化率虽然很高,而二甲醚的产率却很低,可能的原因是 ( 答出一条即可) _______;CO 与H2 合成二甲醚的最佳的温度是_____________。
(3) 对于气体参与的反应如反应④[2CH3OH(g) ![]() C2H4(g) + 2H2O(g)],可以用某组分B的平衡压强(PB)代替物质的量浓度(c)表示平衡常数(Kp),则反应④的平衡常数表达式Kp=____;也可以用压强(PB)变化表示化学反应速率,体积不变的密闭容器中充入一定量的CH3OH气体发生反应④,在10分钟内,容器的压强由xkPa 升高到ykPa,则这段时间该反应的化学反应速率v(CH4)=_____________。
C2H4(g) + 2H2O(g)],可以用某组分B的平衡压强(PB)代替物质的量浓度(c)表示平衡常数(Kp),则反应④的平衡常数表达式Kp=____;也可以用压强(PB)变化表示化学反应速率,体积不变的密闭容器中充入一定量的CH3OH气体发生反应④,在10分钟内,容器的压强由xkPa 升高到ykPa,则这段时间该反应的化学反应速率v(CH4)=_____________。
(4) 反应①~⑤中有多种物质可以做燃料电池的燃料,其中H2是单位质量燃料释放电能最多的物质,若与下列物质构成电池,H2 与_______构成的电池比能量最大。
a.H2O2 b.Cl2 C.O2 d.NiOOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com