
科目: 来源: 题型:
【题目】电解原理在化学工业中有着广泛的应用。现将设计的原电池通过导线与下图中电解池相连,其中a为电解液,X和Y是两块电板板,则:

(1)若X和Y均为惰性电极,a为饱和NaCl溶液,则电解时检验Y电极反应产物的方法是________________________。
(2)若X、Y分别为石墨和铁,a仍为饱和的NaCl溶液,则电解过程中生成的白色固体物质的电解总反应方程式为:________________,将其露置在空气中可观察到的现象为______。
(3)若X和Y均为情性电板,a为一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1molCu(OH)2,恰好恢复电解前的浓度,则电解过程中转移的电子的物质的量为______。
(4)某同学为了使反应2HCl+2Ag=2AgC1+H2↑能在上述装置中进行,则电解液及电极分别为:___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两池电极材料都是铁棒与碳棒(如图)。诸回答下列问题:

(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的_____棒;乙池中的____棒。
②在乙池中阳极的电极反应是____________。
(2)若两池中均盛放饱和NaCl溶液。
①写出乙池中总反应的离子方程式:___________________。
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5:1,且生成两种酸。该反应的化学方程式为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家提出“绿色自由”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH).该反应的热化学方程式为:CO(g)+2H2(g)→CH3OH(g)+H2O(g)△H
(1)若在一个定温定容的容器中发生上述反应,反应达到平衡的标志是 .
A.CO2和CH3OH的浓度相等
B.H2的百分含量保持不变
C.容器内压强保持不变
D.3v正(H2)=v逆(H2O)
E.容器中混合气体的密度保持不变
(2)若将CO2和H2的混合气体分成五等份,将它们分别充入温度不同、容积相同的恒容容器中发生上述反应.反应相同时间后,测得甲醇的体积分数 (CH3OH)与反应温度T的关系如图1,则上述CO2转化为甲醇的反应的△H0(填“>”、“<”、“=”) 
(3)上述反应在实际生产中采用的温度是300℃,其目的是 .
(4)300℃时,将CO2与H2按1:3的体积比充入某密闭容器中,CO2的平衡转化率(a)与体系总压强(P)的关系如图2所示.回答问题: ①若其他条件不变,将A点的体积压缩至原来的一半,一段时间后反应再次达到平衡,与原平衡相比较下列说法正确的是 .
A.CO2的浓度减小
B.正反应速率增大,逆反应速率减小
C.CO2和H2的体积比仍然是1:3
D.H2的体积分数减小②B点平衡混合气体的平均摩尔质量为 22.7g/mol (保留一位小数).
查看答案和解析>>
科目: 来源: 题型:
【题目】处理工业酸性废水中NO3-的电解池工作原理如图所示,电解总反应为4NO3-+4H+![]() 2N2↑+5O2↑+2H2O。下列说法正确的是
2N2↑+5O2↑+2H2O。下列说法正确的是
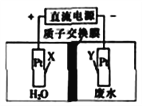
A. X电极上发生还原反应
B. Y电极上发生的电极反应为2NO3-+10e-+12H+==N2↑+6H2O
C. 电解池工作时,H+从质子交换膜右侧向左侧移动
D. 电解池工作时,电路中每通过2mol电子,生成15.68L气体
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列几种有机物: A.CH4B.(CH3)2C=CH﹣CH3 C.C2H2
D.C6H14 E.CH2=CH﹣CH=CH2 F.环戊烷
(1)上述有机物中互为同系物的是 , 互为同分异构体的是 .
(2)用系统命名法对B进行命名 .
(3)A可与Cl2反应生成二氯甲烷,用﹣个化学方程式表示该反应 .
(4)B发生加聚反应的化学方程式为 .
(5)用个化学方程式表示C与足量溴水所反应的 .
(6)如图表示的是一种叫做双烯合成的有机反应,请写出 B 与 E发生双烯合成所得产物的结构简式 . ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列叙述正确的是
A. 1molAlCl3在熔融状态时含有的离子总数为0.4NNA
B. 1molOH-与17gNH3所含的电子数分别为9NA和10NA
C. 常温常压下,0.1molNH3与0.1molHCl充分反应后所得的产物中含有的分子数为0.1NA
D. 13.8gNO2与足量水反应,转移的电子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(1)CO2可用于生产甲醇,已知:2CO2(g)+6H2(g) ![]() CH2=CH2(g)+4H2O(g) ΔH=QkJ/mol。一定条件下,按不同的投料比X(X=n(H2)/n(CO2))向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
CH2=CH2(g)+4H2O(g) ΔH=QkJ/mol。一定条件下,按不同的投料比X(X=n(H2)/n(CO2))向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。

①X1_______X2(填“>”或“<”,后同),Q_______0。
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为______。
③TK时,在该容积可变的恒压密闭容器中发生上述反应,测得有关数据如下表所示:
物质的量(mol) 时间(min) | 0 | 5 | 10 | 15 | 20 |
H2(g) | 6.00 | 5.40 | 5.10 | 5.80 | 5.80 |
CO2(g) | 2.00 | 1.80 | 1.70 | 1.60 | 1.60 |
CH2=CH2(g) | 0 | 0.10 | 0.15 | 0.20 | 0.20 |
已知在10min时只改变了一个反应条件,用改变的条件可能是______。
④下列情况下能表明该反应达到平衡状态的是_____。
a.气体密度不变 b.混合气休的平均摩尔质量不变 c.消耗速率:2v(H2O)=v(CO2)
(3)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
① 若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=______ [常温下K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11]。
② 欲用5L Na2CO3溶液将23.3 g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为_________。[已知:常温下Ksp(BaSO4)=1×10-7、Ksp(BaCO3)=2.5×10-6]。(忽略溶液体积积的变化)
查看答案和解析>>
科目: 来源: 题型:
【题目】从冬青中提取出的有机物A可用合合成抗结肠炎药物Y及其他化学品,合成路线如图:
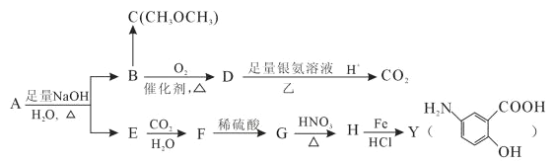
根据上述信息回答:
(1)请写出Y中含氧官能团的名称_________________________。
(2)写出反应③的反应类型:________________________________。
(3)写出反应①的化学方程式:_______________________________________。
(4)A的同分异构体I和J是重要的医药中间体,在浓硫酸的作用下I和J分别生成![]() 和
和![]() ,鉴别I和J的试剂为____________________。
,鉴别I和J的试剂为____________________。
(5)G的同分异构体中,满足下列条件的有_____________种。
①能发生银镜反应 ②能与氯化铁溶液发生显色反应
其中核磁共振氢谱显示四种不同类型的吸收峰。且其峰面积之比为1:2:2:1的结构简 式为____(写一种)。
(6)A的另一种同分异构体K用于合成高分子材料M(![]() ),K 可由L(
),K 可由L(![]() )制得。请写出以L为原料制得M 的合成路线流程图( 无机试剂任用)。流程图示例如下:
)制得。请写出以L为原料制得M 的合成路线流程图( 无机试剂任用)。流程图示例如下:![]() ___________________________
___________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y两元素可形成XY3型共价化合物,则X、Y最外层的电子排布可能是( )
A. X:3s23p2 Y:3s23p5 B. X:2s22p3 Y:2s22p4
C. X:3s23p1 Y:2s22p5 D. X:2s22p3 Y:1s1
查看答案和解析>>
科目: 来源: 题型:
【题目】硫和钒的相关化合物,在药物化学及催化化学等领域应用广泛。回答下列问题:
(1)基态钒原子的外围电子轨道表达式为__________,钒有+2、+3、+4、+5 等多种化合价,其中最稳定的化合价是______________,VO43-的几何构型为___________。
(2)2-巯基烟酸氧钒配合物(图1) 是副作用小的有效调节血糖的新型药物。

①该药物中S 原子的杂化方式是____________,所含第二周期元素第一电离能按由大到小顺序的排列是__________________。
②2-巯基烟酸(图2)水溶性优于2-疏基烟酸氧钒配合物的原因是___________________。
(3)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域П键”,下列物质中存在“离域П键”的是___________。
A.SO2 B.SO42- C.H2S D.CS2
(4)某六方硫钒化合物晶体的晶胞如图3所示,该晶胞的化学式为_____________。图4为该晶胞的俯视图,该晶胞的密度为________g/cm3 (列出计算式即可)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com