
科目: 来源: 题型:
【题目】下列电离方程式书写正确的是( )
A.H2SO4═H22++SO42﹣
B.NaHCO3═Na++H++CO32﹣
C.NaOH═Na++O2﹣+H+
D.Na2SO4═2Na++SO42﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏加德罗常数,下列叙述中正确的是
A. 标准状况下,11.2 L CH3CH2OH 中含有的分子数目为0.5NA
B. 常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
C. 标准状况下,6. 72 L NO2与水充分反应转移的电子数目为0.1NA
D. 100g 46%的乙醇溶液中,含H-O键的数目为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】对含氮物质的研究和利用有着极为重要的意义.
(1)N2、O2和H2相互之间可以发生化合反应,已知反应的热化学方程式如下: N2(g)+O2(g)=2NO(g)△H=+180kJmol﹣1;
2H2(g)+O2(g)=2H2O(g)△H=﹣483kJmol﹣1;
N2(g)+3H2(g)=2NH3(g)△H=﹣93kJmol﹣1 .
则氨的催化氧化反应的热化学方程式为 .
(2)汽车尾气净化的一个反应原理为:2NO(g)+2CO(g)N2(g)+2CO2(g)△H<0. 一定温度下,将2.8mol NO、2.4mol CO通入固定容积为2L的密闭容器中,反应过程中部分物质的物质的量变化如图1所示.
①NO的平衡转化率为 , 0~20min平均反应速率v(NO)为mol/(Lmin);该温度下的化学平衡常数数值是 . 25min时,若保持反应温度不变,再向容器中充入CO、N2各0.8mol,则化学平衡将 移动(填“向左”、“向右”或“不”).
②下列可说明该反应已经达到平衡的是 .
a. v生成(CO2)=v消耗(CO)
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.单位时间内消耗2n mol CO2的同时生成n mol N≡N
e.NO、CO、N2、CO2的浓度相等
③反应达到平衡后,改变某一个条件,如图2曲线①⑧中正确的是 
查看答案和解析>>
科目: 来源: 题型:
【题目】相似相溶(经验规律):一般来说,由极性分子组成的溶质易溶于极性分子组成的溶剂,非极性分子组成的溶质易溶于非极性分子组成的溶剂。以下可以用相似相溶规律说明的是( )
A. Cl2可溶于水 B. I2可溶于水
C. HCl易溶于水 D. NH3易溶于苯
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物其结构简式如图,关于该有机物,下列叙述不正确的是( )
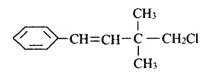
A. 能使酸性KMnO4溶液、溴水褪色,原理相同
B. 1 mol该有机物能与H2发生反应,消耗H2物质的量为4mol
C. 一定条件下,能发生加聚反应
D. 该有机物苯环上的一个H被取代,有3种同分异构体
查看答案和解析>>
科目: 来源: 题型:
【题目】(题文)(题文)碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素。在实验室中,从海藻里提取碘的流程和实验装置如下:

(1)指出上述提取碘的过程中有关实验操作的名称:步骤③_________,步骤⑤______。
(2)写出步骤④对应反应的离子方程式:______________________________。
(3)提取碘的过程中,可供选择的有机试剂是_______________。(请填代号)
A. 酒精 B. 醋酸 C. 四氯化碳 D. 苯
(4)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是_________________________________________________________。
(5)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图实验装置中存在的错误之处:________________。
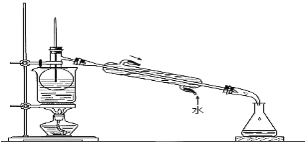
查看答案和解析>>
科目: 来源: 题型:
【题目】H 是合成抗炎药洛索洛芬钠的关键中间体,它的一种合成路线如下:
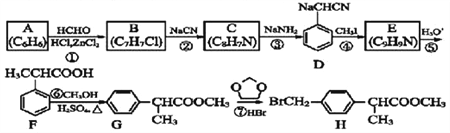
回答下列问题:
(1)质谱仪检测A的质谱图中,最大质荷比的数值是________。G中官能团名称是__________。
(2)B的结构简式为_________________________。
(3)反应②的反应类型为_________________________。反应④的化学方程式为____________。
(4)写出满足下列条件的F的同分异构体的结构简式:________________________。
I.能与FeCl3溶液发生显色反应
II.能发生银镜反应
III.核磁共振氢谱有4组峰且峰面积之比为6:2:1:1
(5)仿照H 的合成路线,设计一种由![]() 的合成路线______。
的合成路线______。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下有浓度均为0.1molL﹣1的四种溶液: ①Na2CO3②NaHCO3③HCl ④NH3H2O
(1)有人称溶液①是油污的“清道夫”,原因是(用离子方程式解释)
(2)这四种溶液中水的电离程度由大到小的顺序是(用序号填写)
(3)向④中加入少量氯化铵固体,此时 ![]() 的值(填“增大”“减小”或“不变”).
的值(填“增大”“减小”或“不变”).
(4)等体积混合③和④的溶液,此时溶液中[NH4+]+[NH3H2O]=molL﹣1(填数值);此时溶液中离子浓度的大小顺序是:;若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积④的体积(填“大于”小于”或“等于”)
(5)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的c( H+)= molL﹣1 .
查看答案和解析>>
科目: 来源: 题型:
【题目】钼酸钠晶体(Na2MoO4·2H2O)是一种金属腐蚀抑制剂。工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图所示:

(1)途径I碱浸时发生反应的化学反应方程式为________________________________________。
(2)途径II氧化时还有Na2SO4生成,则反应的离子方程式为_____________________________。
(3)已知途径I的钼酸钠溶液中c(MoO42-)=0.40 mol/L,c(CO32-)=0.10mol/L。由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去CO32-。当BaMoO4开始沉淀时,CO32-的去除率是____________[已知Ksp(BaCO3)=1×10-9、Ksp(BaMoO4)=4.0×10-8,忽略溶液的体积变化]。
(4)分析纯的钼酸钠常用钼酸铵[(NH4)2MoO4]和氢氧化钠反应来制取,若将该反应产生的气体与途径I所产生的气体一起通入水中,得到正盐的化学式是__________________________。
(5)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如下图:

①当硫酸的浓度大于90%时,碳素钢腐蚀速率几乎为零,原因是________________________。
②若缓释剂钼酸钠-月桂酸肌氨酸总浓度为300mg·L-1,则缓蚀效果最好时钼酸钠(M=206g/mol) 的物质的量浓度为__________________(计算结果保留3位有效数字)。
(6)二硫化钼用作电池的正极材料时接受Li+的嵌入,锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2![]() Lix(MoS2)n。则电池放电时正极的电极反应是:_____________________。
Lix(MoS2)n。则电池放电时正极的电极反应是:_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】滴定实验是化学学科中重要的定量实验. 已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下实验:
①称量1.0g样品溶于水,配成250mL溶液;
②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴酚酞溶液;
④用0.1000mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如表:
滴定序号 | 待测液体积(mL) | 所消耗标准盐酸的体积(mL) | |
滴定前 | 滴定后 | ||
① | 25.00 | 0.50 | 20.60 |
② | 25.00 | 6.00 | 26.00 |
③ | 25.00 | 1.10 | 21.00 |
请回答下列问题:
(1)滴定终点时的现象是 .
(2)所配制的250mL样品液中NaOH的物质的量浓度是 molL﹣1;试样中NaOH的质量分数为 .
(3)若出现下列情况,测定结果偏高的是 . a.滴定前用蒸馏水冲洗锥形瓶
b.在摇动锥形瓶时不慎将瓶内溶液溅出
c.滴定前有气泡,滴定后气泡消失
d.酸式滴定管滴至终点对,俯视读数
e.酸式滴定管用蒸馏水洗后,未用标准液润洗.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com