
科目: 来源: 题型:
【题目】Ⅰ现有下列五种有机物:①CH4、②CH2=CH2、③CH3CH2OH、④ CH3 CH2CH2 CH3 、⑤CH3COOH请回答:
(1)写出⑤的官能团的名称______。(2)与①互为同系物的是______(填序号)。
Ⅱ.下表是A、B、C三种有机物的有关信息:
A | ①能使溴的四氧化碳溶液褪色;②比例模型为: ③能与水在一定条件下反应生成C |
B | ①由C、H、O三种元素组成;②球棍模型为 |
C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应; ③能与B反应生成相对分子质量为86的酯 |
请结合信息回答下列问题:
(1)A与氢气发生加成反应后生成物质D,写出符合下列要求的有机物的结构简式:_______。
①与D互为同系物 ②分子中碳原子总数是4 ③分子里带有一个支链
(2)对于物质B有关说法正确的是_____ (填序号) 。
①无色无味液体 ②有毒 ③易溶于水 ④具有酸性,能与碳酸钙反应 ⑤官能团是-OH
(3)下列试剂中,能用于检验C中是否含有水的是______ (填序号)。
①CuSO4·5H2O ②无水硫酸铜 ③浓硫酸 ④金属钠
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2是引起“温室效应”的主要物质,CO2的甲烷化可以实现其循环利用。
甲烷化过程中,可能发生如下反应:
I. CO2 (g)+4H2(g) ![]() CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1
II. CO2 (g)+4H2(g) ![]() CO(g)+2H2O(g) △H2
CO(g)+2H2O(g) △H2
已知反应II中相关的化学键键能数据如下:
化学键 | H—H | C=O | C | H—O |
E/(kJ·mol-1) | 436 | 750 | 1076 | 463 |
由此计算△H2=_________________。
(2)在常压、催化剂条件下,将CO2 和H2 (体积比为1:4,总物质的量为m mol)置于密闭容器中,发生反应I和II。测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)

①由图1和图2可知,△H1___0(填“>”或“<”),____________可影响催化剂的选择性。
②由图1可知CO2的转化率呈现先升高后降低的变化趋势,其原因是________________________________。
③下列措施能提高CO2平衡转化率的是__________(填标号)
A.提高原料气中H2所占比例 B.适当增大压强 C.升高温度 D.增大催化剂的比表面积 E.前段加热,后段冷却
④350℃时,反应在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应I的平衡常数为_____(用m、V表示)。
⑤550℃时,反应在t2时刻达到平衡,此时容器中H2O(g)的物质的量为__mol(用m表示)
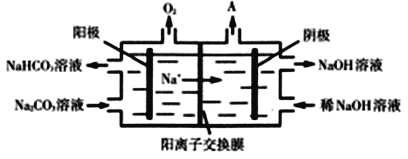
(3)CO2与NaOH溶液反应得到Na2CO3溶液。电解Na2CO3溶液的原理如图所示,阳极的电极反应式为______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铜及其化合物在工农业生产有着重要的用途,氯化铜、氯化业铜经常用作催化剂。其中CuCl广泛应用于化工和印染等行业。
【查阅资料】(i)氯化铜:从水溶液中结晶时,在15℃以下得到四水物,在15-25.7℃得到三水物,在26~42℃得到二水物,在42℃以上得到一水物,在100得到无水物。
(ii)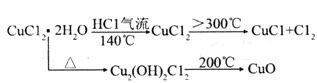
(1)实验室用如图所示的实验仪器及药品制备纯净、干燥的氧气并与铜反应(铁架台,铁夹略)制备氯化铜。

①按气流方向连接各仪器接口顺序是:
a→_____、_____→_____、_____→_____、_____→_____。
②本套装置有两个仪器需要加热,加热的顺序为先_____后_______
(2)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,写出该反应的化学方程式:_____________________。
(3)现欲从(2)所得溶液获得纯净的CuCl22H2O,进行如下操作:
①首先向溶液中加入H2O2溶液然后再加试剂X用于调节pH,过滤,除去杂质,X可选用下列试剂中的(填序号)
a.NaOH b.NH3H2O C.CuO d.CuSO4
②要获得纯净CuCl22H2O晶体的系列操作步骤为:向①所得滤液中加少量盐酸,蒸发浓缩、_____、_____、洗涤、干燥。
(4)用CuCl22H2O为原料制备CuCl时,发现其中含有少量的CuCl2或CuO杂质,若杂质是CuCl2,则产生的原因是______________。
(5)设计简单的实验验证0.1mol/L的CuCl2溶液中的Cu2+对H2O2的分解具有催化作用:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】钒是一种熔点高、硬度大、无磁性的金属,广泛应用于钢铁、航空航天、能源、化工等领域。目前工业上使用一种新工艺,以便从冶炼铝的固体废料一赤泥中提取金属钒,赤泥主要含有Fe2O3、Al2O3、V2O5和CuO,具体工艺流程图如下:
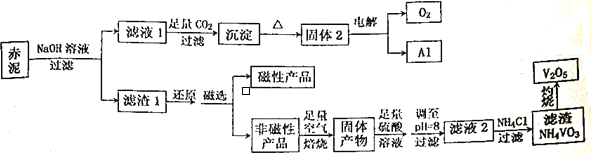
已知:钒有多种价态,其中+5价最稳定。钒在溶液中主要以VO2+和VO3-的形式存在,且存在平衡VO2++H2O![]() VO3-+2H+。回答下列问题:
VO3-+2H+。回答下列问题:
(1)磁性产品的化学式为_________________________。
(2)赤泥加入NaOH溶液,发生的离子反应方程式为___________________。能否用氨水代替NaOH溶液,___________(填“能”或“不能”),理由是___________________________________________。
(3)滤液1生成沉淀的离子反应方程式为_________________________________________。
(4)调至pH=8的目的有两个,一是___________________,二是使VO2+转化为VO3-,此时溶液中VO2+和VO3-的物质的量之比为a:b,VO2++H2O![]() VO3-+2H+的平衡常数K=____________________。
VO3-+2H+的平衡常数K=____________________。
(5)滤液2加氯化铵生成NH4VO3的离子方程式为__________________________,该反应能发生是因为__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.下表为元素周期表的一部分,请按要求回答问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中元素______的非金属性最强,元素_____的金属性最强(填元素符号)。
(2)表中元素④、⑨形成的氢化物的稳定性顺序为_____>______(填化学式)。
(3)表中元素③、④、⑥、⑦的原子半径大小为____>____>___>___(填元素符号)。
Ⅱ.A、B、W、D、E为短周期元素,且原子序数依次增大,五种元素核内质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)A2W的电子式为________。(2) E元素在周期表中的位置为_______ 。
(3)W、D、E三种元素的简单离子半径由小到大的顺序为_______(填离子符号)。
(4)在一定条件下,D元素的单质能与A元素的单质化合生成DA,DA能与水反应放氢气,则其化学方程式为_______
(5)若要比较D和E的金属性强弱,下列实验方法可行的是_______。
a.将D单质置于E的盐溶液中,若单质D不能置换出单质E,说明D的金属性弱
b.将少量D、E的单质分别投入到水中,若D反应而E不反应,说明D的金属性强
C.比较相同条件下D和E的最高价氧化物对应水化物的溶解性若前者比后者溶解度大,说明D的金属性强
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,左室容积为右室的两倍,温度相同,现分别按照如图所示的量充入气体,同时加入少量固体催化剂使两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡,下列说法不正确的是( )
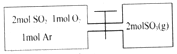
A. 第一次平衡时,SO2的物质的量左室更多
B. 入气体未反应前,左室压强和右室样大
C. 第一次平衡时,左室内压强一定小于右室
D. 第二次平衡时,SO2的总物质的量比第一次平衡时左室SO2的物质的量的2倍还要多
查看答案和解析>>
科目: 来源: 题型:
【题目】将4gNaOH溶解在10mL水中,然后稀释成1L溶液,从中取出10mL,这10mL溶液的物质的量浓度是( )
A.1molL﹣1
B.0.1molL﹣1
C.0.01molL﹣1
D.10molL﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.写出下列反应电极方程式
(1)(﹣)Zn|ZnSO4溶液||CuSO4|Cu(+),负极反应:________
(2)(﹣)Pb|H2SO4(浓)|PbO2(+) 正极反应:______________
(3)(﹣)H2(Pt)|KOH溶液|(Pt)O2(+) 负极反应:_____________
Ⅱ.某化学兴趣小组用下图所示装置进行电化学原理的实验探究,试回答下列问题:
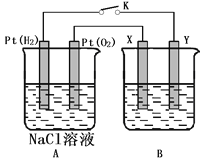
(1)通O2的Pt电极为电池_____________极(填电极名称),其电极方程式为_____________。
(2)若B电池为精炼铜,且粗铜中含有Zn、Fe、Ag、Au等杂质,则该电池阳极泥的主要成分是_______。
(3)若X、Y均是铜,电解质溶液为NaOH溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是Cu2O,试写出该电极发生的电极反应式为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发 生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用 kJ/mol 表示。请认真观察下图,然后 回答问题。

(1)图中所示反应是_____(填“吸热”或“放热”)反应。
(2)已知拆开 1mol H—H 键、1mol I—I、1mol H—I 键分别需要吸收的能量为 436kJ、151kJ、299kJ。则由 1mol 氢气和 1mol 碘反应生成 HI 会_____(填“放出”或“吸 收”)______kJ 的热量。在化学反应过程中,是将_____转化为_________。
(3)下列反应中,属于放热反应的是_____,属于吸热反应的是_____。
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳
⑤食物因氧化而腐败 ⑥Ba(OH)2·8H2O 与 NH4Cl 反应 ⑦铁粉与稀盐酸反应
查看答案和解析>>
科目: 来源: 题型:
【题目】四种常见有机物分子的比例模型示意图如下,其中甲、乙、丙为烃,丁为烃的衍生物。
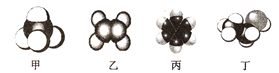
(1)可以鉴别甲和乙的试剂为__________;
a.稀硫酸 b.溴的四氯化碳溶液 c.水 d.酸性高锰酸钾溶液
(2)上述物质中有毒、有特殊气味,且不溶于水、密度比水小的是______(填名称),将其加入溴水中,振荡后静置,观察到的现象是______。
(3)以乙为主要原料合成乙酸,合成路线如图所示:(已知2CH3CHO+O2![]() 2CH3COOH)
2CH3COOH)
![]()
①丁生成A的化学方程式为_______________;
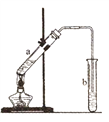
②如图,丁与乙酸在浓硫酸作用下发生反应,当观察到b试管中有明显现象时,停止实验。生成的有机物的结构简式为___________;试管b中的溶液是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com