
科目: 来源: 题型:
【题目】下列关于酸性高锰酸钾溶液褪色的说法正确的是( )
A. 苯的同系物都能使酸性高锰酸钾溶液褪色
B. 2-甲基-3-戊烯可使酸性高锰酸钾溶液褪色
C. 可用酸性高锰酸钾溶液除去乙烷中的乙烯
D. 聚乙炔可以使酸性高锰酸钾溶液和溴水褪色
查看答案和解析>>
科目: 来源: 题型:
【题目】高温下N2和O2发生反应N2(g)+O2(g)![]() 2NO(g),是导致汽车尾气中含有NO的原因之一。
2NO(g),是导致汽车尾气中含有NO的原因之一。
(1)下图是T1、T2两种不同温度下,一定量的NO发生分解过程中N2的体积分数随时间变化的图像,据此判断反应N2(g)+O2(g)![]() 2NO(g)为_______(填“吸热”或“放热”)反应。
2NO(g)为_______(填“吸热”或“放热”)反应。

(2)2000℃时向容积为2L的密闭容器中充入10molN2与5molO2,达到平衡后NO的物质的量为2mol,则此反应的平衡常数K=____。该温度下,若开始时向上述容器中充入N2和O2均为1mol,则达到平衡后N2的转化率为______。
(3)汽车净化装置里装有含Pd化合物的催化剂,气体在催化剂表面吸附与解吸作用的机理如图所示。写出其变化的总化学反应方程式:__________。
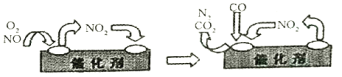
(4)为减少汽车尾气中NOx的排放,常采用CxHy(烃)催化还原NOx消除氢氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
若16gCH4还原NO2至N2共放出热量867kJ,则△H2=_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究小组发现一种化合物在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示。则反应10min时反应物的浓度和反应4min-8min间的平均反应速率,结果应是
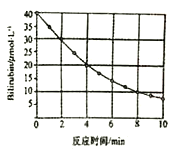
A. 7.5mol/L和2.5mol/(L·min) B. 7.5μmol/L和2.5umol/(L·min)
C. 0.75umol/L和3.0u(L·min) D. 0.75mol/L和5.0umol/(L·min)
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在实验报告中记录下列数据,其中正确的是( )
A.用500mL的容量瓶配制450mL溶液B.用托盘天平称量8.75g食盐
C.用25mL量筒量取12.36mL盐酸D.用广泛pH试纸测得某溶液的pH为3.5
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化铅(PbO)是黄色固体。实验室用草酸在浓硫酸作用下分解制备CO,其原理为:H2C2O4![]() CO↑+CO2↑+H2O。某课题组同学设计实验探究CO还原氧化铅并检验氧化产物(已知CO能使银氨溶液产生黑色沉锭)的装置如图所示。下列说法正确的是
CO↑+CO2↑+H2O。某课题组同学设计实验探究CO还原氧化铅并检验氧化产物(已知CO能使银氨溶液产生黑色沉锭)的装置如图所示。下列说法正确的是

A. 实验时,先点燃装置①处酒精灯,当装置⑤中产生连续气泡且有明显现象后再点燃装置③处酒精灯
B. 装置②④⑤中的试剂依次为碱石灰、银氨溶液、澄清石灰水
C. 实验完毕时,先熄灭装置①处酒精灯,再熄灭装置③处酒精灯
D. 尾气处理可选用点燃、气袋收集、NaOH溶液吸收等方法
查看答案和解析>>
科目: 来源: 题型:
【题目】SOCl2是一种重要氯化剂、锂电池的正极材料,还可作水合盐酸盐的脱水剂。
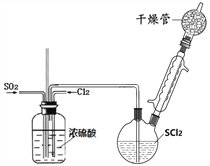
Ⅰ.一种模拟制备SOCl2装置如上图所示(夹持、加热装置略去),双颈瓶中加入25.4mL SCl2,通入纯净干燥Cl2、SO2混合气体,水浴条件下发生反应Cl2+SO2+SCl2=2SOCl2,几种物质的部分性质如下表所示:
密度/ g﹒mL-1 | 熔点/℃ | 沸点/℃ | 备注 | |
SCl2 | 1.62 | -122 | 59 | 40℃分解,遇水分解 |
SOCl2 | 1.64 | -104.5 | 76 | 76℃分解,遇水分解 |
(1)洗气瓶将气体混合并干燥,还有___________作用。
(2)干燥管中碱石灰作用__________。
(3)实验室制取SO2装置和药品应选择____。
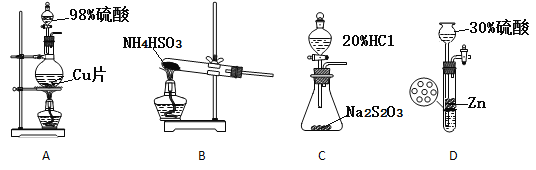
Ⅱ、双颈瓶换毛细玻璃管和蒸馏头,连接减压蒸馏装置,对粗产品减压初蒸,剩余液体继续减压蒸馏获得产品
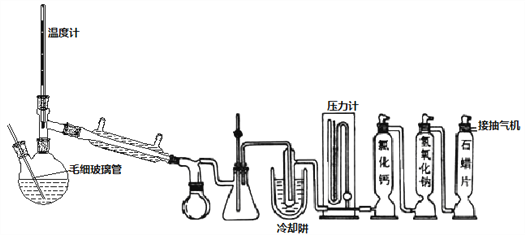
(4)不能用普通蒸馏方法分离混合物的原因是____。
(5)毛细玻璃管C作用是____________。初蒸水浴加热的温度应控制在____℃以下,再蒸馏获得产品25.4mL,则SOCl2产率为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )
A.加热
B.不用稀硫酸改用98%的浓硫酸
C.滴加少量硫酸铜溶液
D.不用铁片,改用铁粉
查看答案和解析>>
科目: 来源: 题型:
【题目】已知下列热化学方程式:
①H2O(l)=H2(g)+ ![]() O2(g)ΔH=+285.8 kJ/mol
O2(g)ΔH=+285.8 kJ/mol
②H2(g)+ ![]() O2(g)=H2O(g)ΔH=-241.8 kJ/mol
O2(g)=H2O(g)ΔH=-241.8 kJ/mol
③NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)ΔH=-57.3 kJ/mol
④C(s)+ ![]() O2(g)=CO(g)ΔH=-110.5 kJ/mol
O2(g)=CO(g)ΔH=-110.5 kJ/mol
⑤C(s)+O2(g)=CO2(g)ΔH=-393.5 kJ/mol
回答下列问题:
(1)如果反应物所具有的总能量大于生成物所具有的总能量,反应物转化为生成物时(填“吸收”或“放出”)热量,△H0(填“>”或“<”)
(2)上述反应中属于吸热反应的是
(3)C的燃烧热为;H2燃烧生成气态水的热值为 kJ。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于胶体的叙述不正确的是( )
A.胶体区别于其他分散系的本质特征是分散质的微粒直径在1~100nm之间
B.光线透过胶体时,胶体中可发生丁达尔效应
C.Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的
D.用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com