
科目: 来源: 题型:
【题目】某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)![]() 2C(g)测得平衡时A、B、C物质的量之比为n(A):n(B):n(C)=1:1:2,若保持温度不变,以1:1:2的物质的量之比再充入A、B和C,下列判断中正确的是
2C(g)测得平衡时A、B、C物质的量之比为n(A):n(B):n(C)=1:1:2,若保持温度不变,以1:1:2的物质的量之比再充入A、B和C,下列判断中正确的是
A. 平衡不移动
B. 平衡向逆反应方向移动
C. 新平衡时各物质的浓度都比原平衡时增大
D. C的质量分数减小
查看答案和解析>>
科目: 来源: 题型:
【题目】在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
A.K+、MnO4-、Na+、Cl-B.K+、Ca2+、NO3-、CO32-
C.Fe3+、Na+、Cl-、SO42-D.Na+、OH-、NO3-、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】某主族元素的原子最外层电子排布是5s1,下列描述正确的是
A. 其单质常温下跟水反应不如钠剧烈 B. 其原子半径比钾原子半径小
C. 其碳酸盐易溶于水 D. 其氢氧化物不能使氢氧化铝溶解
查看答案和解析>>
科目: 来源: 题型:
【题目】请参考题中图表,已知E1=134kJ/mol、E2=368kJ/mol,根据要求回答问题:
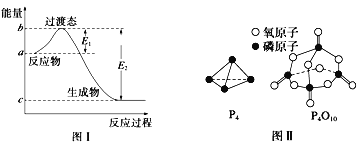
(1)图I是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能最变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是___(填“增大”、“减小”或“不变”下同),△H的变化是________。请写出NO2和CO反应的热化学方程式:__________。
(2)如表所示是部分化学键的键能参数:
化学键 | P-P | P-O | O=O | P=O |
键能/kJ/mol | a | b | c | x |
已知白磷的燃烧热为dkJ/mol,白磷及其完全燃烧的产物的结构如图II所示。1个P4O10分子中P-O的个数为_______,表中x=_____kJ/mol(用含a、b、c、d的代表数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验:
Ⅰ.以H2O2的分解反应为研究对象,实验方案与数据记录如下表,t表示收集a mL O2所需的时间。
序号 | 反应 温度/℃ | c(H2O2)/ mol·L-1 | V(H2O2) /mL | m(MnO2) /g | t/min |
1 | 20 | 2 | 10 | 0 | t1 |
2 | 20 | 2 | 10 | 0.1 | t2 |
3 | 20 | 4 | 10 | 0.1 | t3 |
4 | 40 | 2 | 10 | 0.1 | t4 |
(1)设计实验2和实验3的目的是研究____________对化学反应速率的影响。
(2)为研究温度对化学反应速率的影响,可以将实验________和实验________作对比(填序号)。
(3)将实验1和实验2作对比,t1________t2(填“>”、“<”或“=”)。
Ⅱ.以KI和FeCl3反应为例(2Fe3++2I-![]() 2Fe2++I2)设计实验,探究此反应存在一定的限度。可选试剂:
2Fe2++I2)设计实验,探究此反应存在一定的限度。可选试剂:
①0.1 mol·L-1 KI溶液 ②0.1 mol·L-1 FeCl3溶液 ③0.1 mol·L-1 FeCl2溶液 ④0.1 mol·L-1 盐酸 ⑤0.1 mol·L-1 KSCN溶液 ⑥CCl4
实验步骤:(1)取5 mL 0.1 mol·L-1 KI溶液,再滴加几滴0.1 mol·L-1 FeCl3溶液;
(2)充分反应后,将溶液分成三份;
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘;
(4)另取一份,加试剂________(填序号),现象______________,说明此反应存在一定的限度。
Ⅲ.N2O4可分解为NO2。在100 mL密闭容器中投入0.01 mol N2O4,利用现代化学实验技术跟踪测量c(NO2)。c(NO2)随时间变化的数据记录如下图所示。
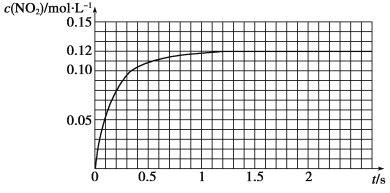
(1)反应容器中最后剩余的物质有______________,其中N2O4的物质的量为________mol。
(2)c(NO2)随时间变化的曲线表明,实验测得的化学反应速率在逐渐减小,最后________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积可变的密闭容器中,可逆反应2HI(g) ![]() H2(g)+I2(g)已达平衡,若将体积缩小,在缩小的过程中:
H2(g)+I2(g)已达平衡,若将体积缩小,在缩小的过程中:
(1)正反应速率;(填“变大”“变小”或“不变”)
(2)平衡;(填“移动”或“不移动”)
(3)混合气体的平均相对分子质量;(填“变大”“变小”或“不变”)
(4)混合气体的密度;(填“变大”“变小”或“不变”)
查看答案和解析>>
科目: 来源: 题型:
【题目】2017年9月我国科学家对于可充放电式锌一空气电池研究取得重大进展。电池装置如图所示,该电池的核心是驱动氧化还原反应(ORR)和析氧反应(OER),KOH溶液为电解质溶液,放电的总反应方程式为2Zn+O2+4OH-+2H2O=2Zn(OH)42-。下列有关说法正确的是

A. 可逆锌一空气电池实际上是二次电池,放电时电解质溶液中K+向负极移动
B. 在电池产生电力的过程中,空气无阻挡地进入电池,发生ORR反应,并释放电荷
C. 发生OER反应的电极反应式为2H2O-4e-=O2+4H+
D. 放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素a、b、c、d的原子序数依次增大,这四种元素形成的单质依次为m、n、p、q;x、y、z是由这些元素组成的二元化合物,其中z为形成酸雨的主要物质之一;25℃时,0.01mol·L-lw溶液中,![]() =1.0×10-10。上述物质的转化关系如图所示,下列说法正确的是
=1.0×10-10。上述物质的转化关系如图所示,下列说法正确的是
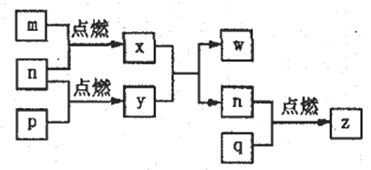
A. 原子半径的大小:a<b<c<d
B. 简单氢化物的沸点:b>d
C. y的电子式:![]()
D. y、w含有的化学键类型完全相同
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,参照元素①-⑧在表中的位置,请回答下列问题。
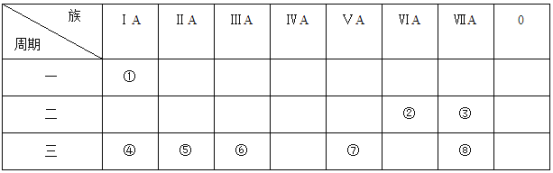
(1)元素③单质的化学式为___________,①和④两种元素形成化合物的电子式为_________。由①②组成且含有非极性键的物质的结构式为____________。
(2)④-⑧5种元素所形成的最高价氧化物的水化物中,碱性最强的是_________,酸性最强的是___________,属于中强酸的是_________(均填化学式)。
(3)④和⑥两种元素的最高价氧化物的水化物,在水中反应的离子方程式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com