
科目: 来源: 题型:
【题目】I.A~D是四种烃分子的球棍模型(如图)
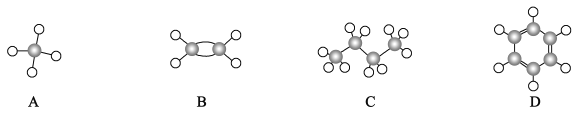
(1)所有原子一定共平面的是______(填序号)
(2)能使酸性高锰酸钾溶液褪色的物质是_____ (填序号)
(3)D与浓硝酸和浓硫酸共热的化学方程式______。
II.某些有机物的转化如下图所示。已知:A是营养物质之一,米饭、馒头中富含A,在酸性条件下水解的最终产物是B。C是白酒的主要成分,D的水溶液能使紫色石蕊试液变红。
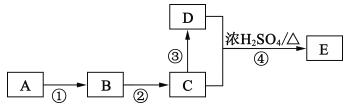
(4)C中官能团的名称为______;反应③的反应类型为______,反应④的化学方程式为______。
(5)反应④中,D断裂的化学键是_______ (填“C一H”、“O一H”或“C一O”)
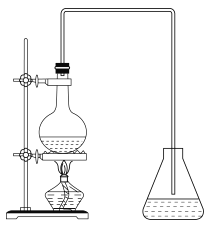
(6)实验室由反应④制备E的装置如图所示。烧瓶中依次加入C、浓硫酸、D和碎瓷片,锥形瓶中加入的是饱和碳酸钠溶液,实验结束后振荡锥形瓶内液体,看到有气泡产生,产生气泡的原因是__________(用离子方程式表示),将锥形瓶中的液体分离的方法是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验是学习化学的一个重要途径。
(1)图1是实验室常用的制气装置,其中b可用于制取O2和______(写化学式),其制取反应的化学方程式为_________。若用二氧化锰和浓盐酸制取氯气应选择的装置为_______,反应的离子方程式为__________。
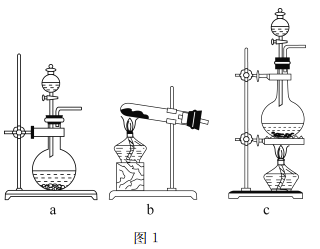
(2)图2是实验室制备氯气并进行一系列相关实验的装置。
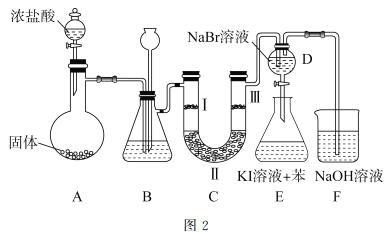
①A中盛放的固体药品是_________ (填化学式),装置B中盛装的液体试剂为_________。
②装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、II处依次放入的物质正确的是_________(填字母编号)。
编号 | I | II | III |
A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
③D中发生反应的离子方程式是_________。将装置D中的溶液加入装置E中,溶液分为两层,上层呈紫红色,要分离出紫红色溶液,需使用的玻璃仪器是玻璃棒、烧杯和________。
④报纸报道了多起因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。请用离子方程式表示其原因: ________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列科研成果不是由我国发明或创造的是( )
A.世界上第一个由人工合成的、具有生理活性的蛋白质﹣﹣结晶牛胰岛素
B.黑火药和造纸
C.发现元素周期律
D.青蒿素的合成
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚砜(SOCl2)是一种液态化合物,沸点为 77℃,在农药、制药行业中用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生.实验室合成原理:SO2+Cl2+SCl2═2SOCl2,部分装置如图所示,(已知 SCl2的沸点为 50℃).
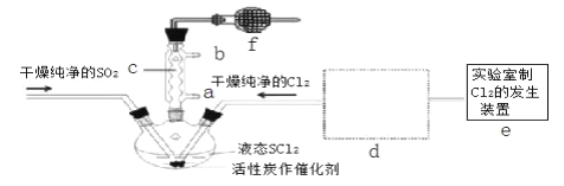
回答以下问题:
(1)下列四种制备 SO2的方案中最佳选择是____________________________
方案 | A | B | C | D |
发生装置 |
|
|
|
|
所选试剂 | 70%H2SO4+K2SO3 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO3 | NaHCO3固体 |
(2)以 MnO2和浓盐酸为原料制备 Cl2的离子方程式为___________________________
(3)仪器 f 的作用是_________________________________________________
(4)d 的虚线框内隐含两个装置,按气流方向顺序这两个装置的药品分别是_______________。
(5)实验结束后,将三颈烧瓶混合物中产品分离出来的方法是 _________________________
(6)若用 SOCl2作 FeCl36H2O 的脱水剂,设计实验证明脱水时发生了氧化还原反应。取少量 FeCl36H2O 于试管中,加入过量 SOCl2,振荡,往试管中加水溶解,滴加____________或________溶液,证明脱水过程发生了氧化还原反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨的热化学方程式为N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJ/mol.现将1molN2(g)、3molH2(g)充入一容积为2L的密闭容器中,在500℃下进行反应,10min时达到平衡,NH3的体积分数为φ,下列说法中正确的是( )
A.若达到平衡时,测得体系放出9.24kJ热量,则H2反应速率变化曲线如图甲所示
B.反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为p,三者关系如图乙
C.如图丙所示,容器I和II达到平衡时,NH3的体积分数为φ,则容器I放出热量与容器II吸收热量之和为92.4kJ
D.若起始加入物料为1 mol N2 , 3 mol H2 , 在不同条件下达到平衡时,NH3的体积分数变化如图丁所示
查看答案和解析>>
科目: 来源: 题型:
【题目】难挥发性二硫化钽(TaS2 )可采用如下装置提纯。将不纯的TaS2 粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下:
TaS2(g)+2I2(g)![]() TaI4(g)+S2(g)
TaI4(g)+S2(g)
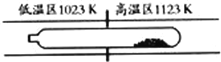
下列说法正确的是 ( )
A.在不同温度区域,TaI4 的量保持不变
B.在提纯过程中,I2 的量不断减少
C.在提纯过程中,I2的作用是将TaS2 从高温区转移到低温区
D.该正反应的平衡常数与TaI4 和S2 的浓度乘积成反比
查看答案和解析>>
科目: 来源: 题型:
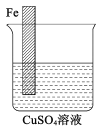
【题目】某兴趣小组为研究原电池原理,设计如图装置。
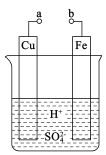
(1)a和b用导线连接,Fe电极的电极反应式为:________,Cu极发生_____反应,溶液中SO42-移向______(填“Cu”或“Fe”)极。
(2)无论a和b是否连接,Fe片均被腐蚀。若转移了0.4mol电子,则理论.上Fe片质量减轻____g。
(3)设计一个实验方案,使如图装置中的铁棒上析出铜,而铁不溶解(作图表示)。
 _____
_____
(4)依据Ba(OH)2·8H2O与NH4Cl晶体的反应原理设计原电池,你认为是否可行?理由是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】 Fe和Mg与H2SO4反应的实验如下:
实验 |
|
|
|
|
现象 | Fe表面产生大量无色气泡 | Fe表面产生气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是( )
A.I中产生气体的原因是:Fe + 2H+=Fe2++ H2↑
B.取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C.Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D.Ⅳ中现象说明Mg的金属性比Fe强
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中错误的是( )
A.质子数相同的原子,其核外电子排布也相同
B.质量数相同的原子,其化学性质一定相同
C.金属性越活泼,其原子在反应中越易失去电子
D.非金属性越活泼,其阴离子越难失去电子
查看答案和解析>>
科目: 来源: 题型:
【题目】 某无色溶液中加入氯化钡后有白色沉淀,再加稀硝酸沉淀不消失,则该溶液中
A.一定含有SO42-B.一定含有Ag+
C.可能含有SO42-或Ag+D.一定含有Ag+、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com