
科目: 来源: 题型:
【题目】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe2+的简化电子排布式为____________________。
(2)实验室可用KSCN、苯酚( )来检验Fe3+ 。N、O、S三种元素的第一电离能由大到小的顺序为 _______________(用元素符号表示),苯酚中碳原子的杂化轨道类型为_________。
)来检验Fe3+ 。N、O、S三种元素的第一电离能由大到小的顺序为 _______________(用元素符号表示),苯酚中碳原子的杂化轨道类型为_________。
(3)FeCl3的熔点为306 ℃,沸点为315 ℃。FeCl3的晶体类型是_____________ 。FeSO4常作净水剂和补铁剂,SO42- 的立体构型是___________________。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1 mol Fe(CO)5分子中含______molσ键,与CO互为等电子体的离子是 _________________(填化学式,写一种)。
(5)氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为________。
(6)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg/cm3 ,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为 ________ ;Fe2+与O2-最短核间距为 __________ pm。

查看答案和解析>>
科目: 来源: 题型:
【题目】工业合成氨的反应为:N2+3H2![]() 2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是( )
2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是( )
A. 达到平衡时,反应速率:v(正)=v(逆)=0
B. 使用催化剂可加快反应速率,提高生产效率
C. 为了提高H2的转化率,应适当增大H2的浓度
D. 若在密闭容器加入1molN2和过量的H2,最后能生成2molNH3
查看答案和解析>>
科目: 来源: 题型:
【题目】反应A(g)+4B(g)![]() C(g)+D(g),在四种不同情况下的反应速率如下,其中反应进行最快的是( )
C(g)+D(g),在四种不同情况下的反应速率如下,其中反应进行最快的是( )
A. vA=0.15mol/(L·min) B. vB=0.02mol/(L·s)
C. vC=0.2mol/(L·min) D. vD=0.01mol/(L·s)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知苯甲酸的酸性比碳酸强,苯酚的酸性比碳酸弱.可以将 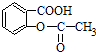 转变为
转变为 ![]() 的方法是( )
的方法是( )
①与足量的NaOH溶液共热,再通入CO2
②与稀硫酸共热后,加入足量的NaOH溶液
③加热溶液,通入足量的SO2
④与稀H2SO4共热后,加入足量的NaHCO3 .
A.①②
B.①④
C.②③
D.②④
查看答案和解析>>
科目: 来源: 题型:
【题目】硫是中学化学重要的非金属元素之一,请回答下列有关问题。
已知:2SO2(g)+O2(g)![]() 2SO3(g) △H=-196.6kJ/mol
2SO3(g) △H=-196.6kJ/mol
2NO(g)+O2(g)![]() 2NO2(g) △H=-113.0kJ/mol
2NO2(g) △H=-113.0kJ/mol
(1)反应NO2(g)+ SO2(g)![]() SO3(g)+NO(g)的ΔH= ______kJ/mol 。
SO3(g)+NO(g)的ΔH= ______kJ/mol 。
(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 _________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO2的同时消耗1 molNO
(3)S2Cl2和SCl2均为重要的工业化合物。已知:
a.S2(l)+Cl2(g)![]() S2Cl2(g) △H1
S2Cl2(g) △H1
b.S2Cl2(g)+ Cl2(g)![]() 2SCl2(g) △H2
2SCl2(g) △H2
—定压强下,向10 L密闭容器中充入1 molS2Cl2和1 mol Cl2,发生反应b。Cl2与SCl2的消耗速率(υ)与温度(T)的关系如图所示:
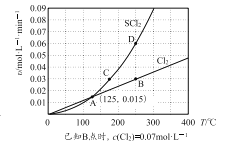
① A、B、C、D四点对应状态下,达到平衡状态的有______(填字母),理由是_______。
②—定温度下,在恒容密闭容器中发生反应a和反应b,达到平衡后缩小容器容积,重新达到平衡后,Cl2的平衡转化率_________(填“增大”或“减小”或“不变”),理由是________。
II.氮有不同价态的化合物,如氨、氮气、亚硝酸钠、乙二胺等。
图(I)和图(II)分别为二元酸H2A和乙二胺(H2NCH2CH2NH2)溶液中各微粒的百分含量δ(即物质的量百分数)随溶液pH的变化曲线(25℃)。
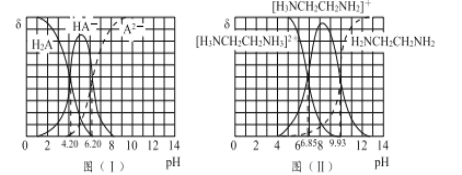
(1)H3NCH2CH2NH3A溶液显____(填“酸”或“碱”)性。
(2)乙二胺在水溶液中发生第二步电离的方程式:____________________,其平衡常数Kb2= _______________________ 。
(3)向20 mL 0.1 mol/L的H2A溶液加入10 mL 0.1 mol/L H2NCH2CH2NH2溶液后,溶液中各离子浓度大小的关系为 ____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】随着原子序数的递增,下列说法正确的是( )
A.最外层电子数逐渐增多
B.原子半径逐渐减小
C.元素的主要化合价逐渐增加
D.元素的化合价、原子半径、最外层电子数、得失电子能力、金属性与非金属性呈周期性变化
查看答案和解析>>
科目: 来源: 题型:
【题目】反应H2(g)+I2(g)![]() 2HI(g)在温度和容积不变的条件下进行。能说明反应达到平衡状态的叙述是( )
2HI(g)在温度和容积不变的条件下进行。能说明反应达到平衡状态的叙述是( )
A. c(H2)=c(I2) B. H2的消耗速率等于HI的分解速率
C. 容器内气体的颜色不再变化 D. 容器内压强不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com