
科目: 来源: 题型:
【题目】下列各组元素性质的递变情况错误的是 ( )
A. Li、Be、B原子最外层电子数依次增多
B. P、S、Cl元素最高正价依次升高
C. N、O、F电负性依次增大
D. Na、K、Rb第一电离能逐渐增大
查看答案和解析>>
科目: 来源: 题型:
【题目】已知二氧化碳和氢气在一定条件下可以合成甲醇,其制备反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),下列说法正确的是
CH3OH(g)+H2O(g),下列说法正确的是
A. 调控反应条件不能改变反应限度
B. 化学反应的限度决定了反应物在该条件下的最大转化率
C. 当CO2的消耗速率等于其生成速率时,该反应已停止
D. 投入1molCO2能得到1mol的CH3OH
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述不正确的是
A. 用电子式表示HCl的形成过程: ![]()
B. ![]() 中的原子核内的中子数与核外电子数之差是99
中的原子核内的中子数与核外电子数之差是99
C. 在空气中加热金属锂:4Li+O2![]() 2Li2O
2Li2O
D. (CH3)2CHC2H5和CH3CH2CH(CH3)2属于同种物质
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,由此可知 ( )
A. X的原子半径大于Y的原子半径
B. X的电负性小于Y的电负性
C. X的氧化性小于Y的氧化性
D. X的第一电离能大于Y的第一电离能
查看答案和解析>>
科目: 来源: 题型:
【题目】铬铁矿的成分主要为FeCr2O4,另含有少量Al2O3和SiO2。从铬铁矿中提取铁、铬的化合物,并获得副产物的工艺流程如下:
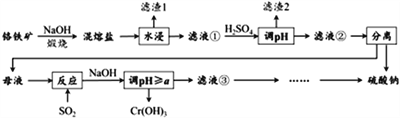
已知“混熔盐”中含有Na2CrO4和NaFeO2等成分,其中NaFeO2极易水解。试回答下列问题:
(1)“滤渣1”为红褐色沉淀,其化学式为_________________;通过水浸生成红褐色沉淀的化学方程式为_________________________________。
(2)向滤液①中加H2SO4“调“pH”的目的:一是使CrO42-转化为Cr2O72-,离子方程式为___________________________________;二是____________________________。
(3)“煅烧”铬铁矿时,主要成分反应的化学方程式为____________________________。
(4)根据下图溶解度(S)~温度(T)曲线判断,对滤液②进行的最佳“分离”方法为_____________(填序号)。
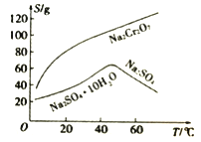
A.蒸发结晶 B.蒸发浓缩,趁热过滤 C.蒸发浓缩,冷却结晶,过滤
(5)“反应”的离子方程式为____________________________。
(6)Cr(OH)3溶于盐酸生成配离子[CrCln(H2O)6-n]x+。0.0015mol[CrCln(H2O)6-n]x+与氢离子交换树脂(HR)完全发生离子交换:[CrCln(H2O)6-n]x++xHR→Rx[CrCln(H2O)6-n] +xH+,生成的H+可与25.00mL 0.1200mol/L NaOH溶液恰好中和。则该配离子的化学式为__________________。
(7)已知25℃时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=1.0×10-32。则使Cr3+恰好完全沉淀,即溶液中c(Cr3+)=1.0×10-5mol/L时,应调节pH的最小值a为多少___________?(列式计算)
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下体积不变的密闭容器中:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H=-905.9k/mol,下列叙述正确的是
4NO(g)+6H2O(g) △H=-905.9k/mol,下列叙述正确的是
A. 4molNH3和5molO2反应,达到平衡时放出的热量为905.9kJ
B. 平衡时V正(O2)=4/5V逆(NO)
C. 适当增大氧气的浓度可以提高氨气的转化率
D. 降低压强,正反应速率减小,逆反应速率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】配制100mL 0.50 mol·L-1 NaOH溶液时,必须用到的仪器是
A.100mL容量瓶B.100mL集气瓶C.100mL烧瓶D.100mL滴瓶
查看答案和解析>>
科目: 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液。不正确的操作顺序是
A.⑤②④①③B.⑤④②①③C.②⑤④①③D.①④②⑤③
查看答案和解析>>
科目: 来源: 题型:
【题目】原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是

A. ①②中Mg作负极、③④中Fe作负极
B. ②中A1作负极,电极反应式为2A1-6e-=2Al3+
C. ③中Fe作负极,电极反应式为Fe-2e-=Fe2+
D. ④中Cu作正极,电极反应式为O2+4e-+2H2O=4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com