
科目: 来源: 题型:
【题目】根据下列化合物:①CH3COOH ②Na2C2O4③NaCl ④NaOH⑤NH4Cl.回答问题:
(1)H2C2O4是弱酸,则②溶液中盐水解的离子方程式为;
(2)浓度均为 0.1molL﹣1 的④、⑤溶液等体积混合后,c(Na+)+c(NH4+)+c(NH3H2O)=;
(3)常温下,pH都为4的①、⑤溶液中水电离出的c(OH﹣)的比为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】煤的主要组成元素是碳、氢、氧、硫、氮,燃煤产生CxHy、SO2等大气污染物,煤的气化是高效、清洁利用煤炭的重要途径之一。回答下列问题:
(1)利用煤的气化获得的水煤气( 主要成分为CO、CO2和H2 )在催化剂作用下可以合成绿色燃料甲醇。
已知: H2O(1) = H2O(g) ΔH1= +44 .0kJ/mol
CO2(g)+H2(g) = CO(g)+H2O(g) ΔH2=-3.0kJ/mol
CO2(g)+3H2(g) = CH3OH(g)+H2O(g) ΔH3=-58.7 kJ/mol
写出由CO与H2制备CH3OH 气体的热化学方程式____________。
(2)甲醇和CO2可直接合成碳酸二甲酯(CH3OCOOCH3简称DMC) ;
2CH3OH(g)+CO2(g) ![]() CH3OCOOCH3(g)+H2O(g) ΔH4<0
CH3OCOOCH3(g)+H2O(g) ΔH4<0
①该化学反应的平衡常数表达式为K=__________
②在恒温恒容密闭容器中发生上述反应,能说明反应达到平衡状态的是________(填编号)。
A.V正(CH3OH)= 2V逆(H2O)
B.容器内气体的密度不变
C.容器内压强不变
D.CH3OH与CO2的物质的量之比保持不变
③一定条件下分别向甲,乙、丙三个恒容密闭容器中加入一定量的初始物质发生该反应,各容器中温度、反应物的起始量如下表,反应过程中DMC的物质的量浓度随时间变化如图所示:
容器 | 甲 | 乙 | 丙 |
容积(L) | 0.5 | 0.5 | V |
温度(℃) | T1 | T2 | T3 |
起始量 | 1molCO2(g) 2molCH3OH(g) | 1molDMC(g) 1molH2O(g) | 2molCO2(g) 2molCH3OH(g) |
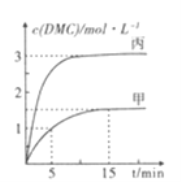
甲容器中,在5-15min时的平均反应速率v(CO2)=___________.乙容器中,若平衡时n(CO2)=0.2mol.则T1_____T2 (填“>”“<”或“=”)。两容器的反应达平衡时CO2的转化率: 甲________丙(填“>”“<."或”=”)。
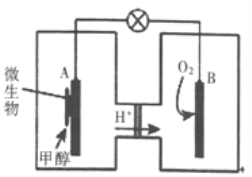
(3)利用甲醇可制成微生物燃料电池(利用微生物将化学能直接转化成电能的装置)。某微生物燃料电池装置如图所示: A极是_____极(填“正”或“负”),其电极反应式是_______。该电池不能在高温下工作的理由是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业废水中常含有一定量的Cr2O72﹣和CrO42﹣ , 它们会对人类及生态系统产生很大的伤害,必须进行处理;常用的处理方法之一为还原沉淀法生成Cr(OH)3而除去.
(1)Cr2O72﹣和CrO42﹣之间存在相互转化:2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O,能说明反应达平衡状态的是 . a.Cr2O72﹣和CrO42﹣的浓度相同 b.2v (Cr2O72﹣)=v (CrO42﹣) c.溶液的颜色不变
(2)常温下,Cr(OH)3的溶度积Ksp=1×10﹣32 , 要使c(Cr3+)降至1×10﹣5mol/L以下,溶液的pH应调至以上.
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,用0.10m/L的弱碱BOH滴定10.00 ml a mol/L的盐酸,溶液的pH与所加BOH溶液体积(V)的关系如图所示。已知N点溶液中存在关系式:c(C1—)=c(B+)+c(BOH)。下列说法正确的是
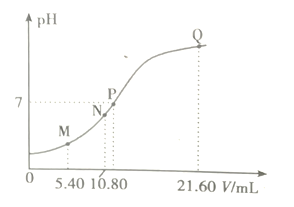
A. M点溶液中存在c(H+)=c(OH—)+2c(BOH)+c(B+)
B. N、Q两点溶液中BOH电离平衡常数:N<Q
C. P点BOH过量,此时溶液中c(B+)>c(Cl—)
D. a<0.108
查看答案和解析>>
科目: 来源: 题型:
【题目】研究NOx、SO2、CO等大气污染气体的处理具有重要意义.
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S.已知:1molCO(g)与适量的SO2(g)反应生成S(s)和CO2(g)时,放出135kJ的热量,则此反应的热化学方程式为.
(2)用CH4催化还原NOx也可以消除氮氧化物的污染.例如: ①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=﹣574kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2
若1molCH4(g)直接将NO2(g)还原至N2(g),整个过程中放出的热量为867kJ,则△H2= .
(3)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可转化为N2(g)和CO2(g)得到净化.已知 2NO(g)+2CO(g)N2(g)+2CO2(g)△H<0 在25℃、101kPa下,将2molNO、2.4molCO通入固定容积为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示.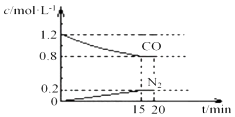
①0~15min 内,v(CO2)= , 25℃时该反应平衡常数为(该空保留2位小数);
②20min 时若改变反应条件,导致NO浓度下降,则改变的条件不可能是(填选项序号).
a.升高温度 b.增加CO的量 c.降低温度 d.扩大容积
(4)SO2尾气常用饱和Na2SO3溶液吸收,减少SO2气体污染并可得到重要的化工原料NaHSO3 . 已知NaHSO3溶液同时存在以下两种平衡: ①HSO3﹣SO32﹣+H+ , ②HSO3﹣+H2OH2SO3+OH﹣;常温下,0.1 mol/L NaHSO3溶液的pH<7,则该溶液中c(H2SO3)c(SO32﹣)(填“>”、“=”或“<”).
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物与人们的衣、食、住、行及健康等有非常密切的关系,认知和研究有机物具有十分重要的作用.
(1)有机物A是构成营养素的基础物质(含C、O、H、N等元素),A的球棍模型如图所示,图中“棍”代表单键或双键或三键,不同颜色的球代表不同元素的原子.回答下列问题: A的分子式是 , 含氧官能团的名称是;
(2)将含有C、H、O的有机物3.24g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过CaCl2管(A)和碱石灰(B),测得A管质量增加了2.16g,B管增加了9.24g,已知该有机物的相对分子质量为108. 该有机物的分子式为 , 该有机物1分子中有1个苯环,试写出它的同分异构体的结构简式中的任意一种 . 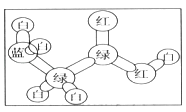
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,可用K2S沉淀Cu2+、Mn2+、Zn2+三种离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。下列说法正确的是

A. 三种离子对应的硫化物中Ksp(CuS)最小,约为1×10-20
B. 向MnS的悬浊液中加入少量水。沉淀溶解平衡向溶解的方向移动,c(S2-)增大
C. 可用MnS除去MnCl2溶液中混有的少量杂质ZnCl2
D. 向浓度均为1×10-5mol/L的Cu2+、 Zn2+、Mn2+混合溶液中逐滴加入1×10-4mol/的Na2S溶液,Mn2+最先沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒温恒容的密闭容器中,发生可逆反应2NO(g)+O2(g)![]() 2NO2(g),不能说明该反应已经达到平衡状态的是
2NO2(g),不能说明该反应已经达到平衡状态的是
A. 正反应生成NO2的速率和逆反应生成NO的速率相等
B. 反应容器中压强不随时间的延长而变化
C. 混合气体颜色深浅保持不变
D. 混合气体的密度不随时间延长而变化
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( ) 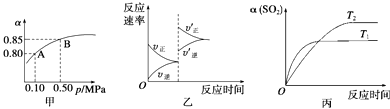
A.由图甲知,A点SO2的平衡浓度为0.4 mol/L
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com