
科目: 来源: 题型:
【题目】镁及其化合物是实验设计的热点载体,查阅资料。
ⅰ | 2NO2+2NaOH=NaNO2+NaNO3+H2O |
ⅱ | Mg3N2与水反应 |
ⅲ | 常温下,NH3·H2O、CH3COOH的电离常数都等于1.8×10-5 |
Ⅰ.探究镁的性质。
某学习小组设计实验探究镁与二氧化氮反应的产物,实验装置如图所示。
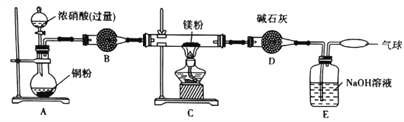
(1)B中试剂是_____________;D装置的作用是______________________________。
(2)实验时,先启动A中反应,当C装置中充满红棕色气体时点燃酒精灯,这样操作的目的是____________________________________________________________________________。
(3)确定有N2生成的实验现象是_______________________________________________________。
(4)实验完毕后,设计实验确认产物中有Mg3N2取少量C中残留固体于试管中,滴加蒸馏水,_____________________,则产物中有氮化镁。
(5)经测定,Mg与NO2反应生成MgO、Mg3N2和N2,其中Mg3N2和N2的物质的量相等。C中发生反应的化学方程式为_____________________________________________________。
Ⅱ.探究Mg(OH)2在氯化铵溶液中溶解的原因。供选试剂有:氢氧化镁、蒸馏水、硝酸氨溶液、盐酸、醋酸铵溶液。
取少量氢氧化镁粉末投入氯化氨溶液中,振荡、白色粉末全部溶解。为了探究其原因,他们提出两种假设。
假设1:氯化铵溶液呈酸性,H++OH-=H2O,促进Mg(OH)2溶解;
假设2:NH4++OH-=NH3·H2O,促进Mg(OH)2溶解。
(6)请你帮他们设计实验探究哪一种假设正确:____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素在元素周期表中的位置如图所示。
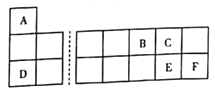
回答下列问题:
(1)在周期表中,E位于第_____________周期第_____________族。
(2)A、B能组成既含极性键又含非极性键的化合物,其电子式为_____________。
(3)在E、F的气态氢化物中,热稳定性较强的是_____________(填化学式,下同),还原性较强的是_______________。
(4)A、C、D、E组成两种酸式盐X、Y,将X、Y溶液混合发生复分解反应,写出离子方程式:________________________________________________________。
(5)常用(BA4)2E2C8检验废水中的Mn2+,若观察到无色溶液变紫红色,可判断废水中含Mn2+,还原产物与盐酸酸化的BaCl2溶液混合产生白色沉淀。写出无色溶液变紫红色溶液的离子方程式:_________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有一未知的无色溶液,只可能含有以下离子中的若干种:NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、SO42- , 现取两份100mL溶液进行如下实验: ①第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。②第二份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。以下推测不正确的是( )
A.原溶液一定不存在Cu2+
B.不能确定原溶液是否含有K+
C.实验所加的NaOH的浓度为2mol·L-1
D.原溶液确定含Mg2+、Al3+、NH4+ , 且n(Mg2+) ∶n(Al3+)∶n( NH4+)=1∶1∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个容积为2L的密闭容器中,加入0.8molA2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+ B2(g) ![]() 2AB(g)ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )
2AB(g)ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )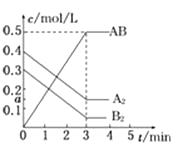
A.图中a点的值为0.15
B.该反应的平衡常数K=0.03
C.温度升高,平衡常数K值减小
D.平衡时A2的转化率为62.5%
查看答案和解析>>
科目: 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn (s、白)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH1
②Sn (s、灰)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH2
③Sn (s、灰) Sn (s、白);DH3=+2.1 kJ/mol
Sn (s、白);DH3=+2.1 kJ/mol
下列说法正确的是( )
A. DH1>DH2
B. 锡在常温下以灰锡状态存在
C. 灰锡转化为白锡的反应是放热反应
D. 锡制器皿长期处于低于13.2 ℃的环境中,会自行毁坏
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机合成中常用的试剂。
巳知:①2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g)△H1=akJ·mol-1
NaNO3(s)+ClNO(g)△H1=akJ·mol-1
②4NO2(8)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)△H2=bkJ·mol-1
2NaNO3(s)+2NO(g)+Cl2(g)△H2=bkJ·mol-1
③2NO(g)+Cl2(g)![]() 2ClNO(g)△H3=ckJ·mol-1
2ClNO(g)△H3=ckJ·mol-1
(1)上述反应中,a、b、c之间满足的关系为_____________________。
(2)某温度下,在密闭容器中发生反应:2NO(g)+Cl2(g)![]() 2ClNO(g),正反应速率表达式为v正=k·cn(NO)·cm(Cl2)(k是反应速率常数,只与温度有关;n、m为反应级数,只取正数)。测得正反应速率与浓度的关系如下表所示:
2ClNO(g),正反应速率表达式为v正=k·cn(NO)·cm(Cl2)(k是反应速率常数,只与温度有关;n、m为反应级数,只取正数)。测得正反应速率与浓度的关系如下表所示:
序号 | c(NO)/mol·L-1 | c(Cl2)/mol·L-1 | v正/mol·L-1·min-1 |
ⅰ | 0.100 | 0.100 | 0.144 |
ⅱ | 0.100 | 0.200 | 0.288 |
ⅲ | 0.200 | 0.100 | 0.576 |
①n=_____________,m=_____________。
②反应达到平衡后,其他条件不变时,缩小容器体积瞬间,v正_____________v逆(填“>"“<”或“=")。NO的平衡转化率_____________(填“增大”“减小”或“不变”)。
(3)在2L恒容密闭容器中充入0.8molClNO(g),发生反应:2ClNO(g)![]() Cl2(g)+2NO(g) △H,测得c(Cl2)与温度和时间的关系如图1所示。300℃时达到平衡后,温度与平衡常数负对数(-lgK)的关系如图2所示。
Cl2(g)+2NO(g) △H,测得c(Cl2)与温度和时间的关系如图1所示。300℃时达到平衡后,温度与平衡常数负对数(-lgK)的关系如图2所示。
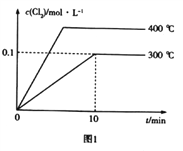
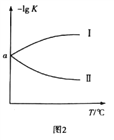
①a=_____________。
②图2中符合题意的曲线为_____________(填“Ⅰ”或“Ⅱ”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属铝分别和O2、O3发生反应生成Al2O3 , 反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。下列有关说法中不正确的是( )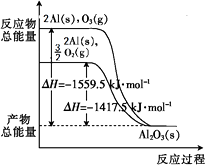
A.Al(s)与O3(g)反应的热化学方程式为2Al(s)+O3(g)=Al2O3(s) ΔH =-1559.5 kJ·mol-1
B.等质量的O2比O3的能量低
C.1 mol O2完全转化为O3 , 需吸收142 kJ的热量
D.给3O2(g) ![]() 2O3(g)的平衡体系加热,有利于O3的生成
2O3(g)的平衡体系加热,有利于O3的生成
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:C(s)+ ![]() O2(g)=CO(g) ΔH=-110.35kJ·mol-1
O2(g)=CO(g) ΔH=-110.35kJ·mol-1
CO(g)+ ![]() O2(g)=CO2(g) ΔH=-282.57kJ·mol-1
O2(g)=CO2(g) ΔH=-282.57kJ·mol-1
在6 g 碳不完全燃烧所得产物中,CO与CO2的体积比为2∶3, 与6 g碳完全燃烧相比,损失的热量为( )
A.282.57 kJ
B.110.35 kJ
C.196.46 kJ
D.56.51 kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】在反应2SO2+18O22SO3中,其中氧气用18O标记上,其中含有18O的物质有( )
A.SO2
B.O2 、SO3
C.SO2 、 O2 、 SO3
D.SO2 、SO3
查看答案和解析>>
科目: 来源: 题型:
【题目】铜及其化合物在生活、生产中有广泛应用。
(1)常用胆矾溶液对游泳池中的水消毒,它的水溶液呈酸性,用离子方程式表示其原因:________________________________________________________________________________。
(2)在Cu(OH)2悬浊液中滴加氨水,蓝色沉定变成蓝色溶液。已知:Ksp[Cu(OH)2]=2.2×10-20,Cu2+(aq)+4NH3(aq)![]() [Cu(NH3)4]2+(aq)K1=2.0×1013。则
[Cu(NH3)4]2+(aq)K1=2.0×1013。则
Cu(OH)2(s)+4NH3(aq)![]() [Cu(NH3)4]2+(aq)+2OH-(aq)K2=_____________。
[Cu(NH3)4]2+(aq)+2OH-(aq)K2=_____________。
(3)Cu(OH)2溶于浓烧碱溶液生成Na2CuO2,在Na2CuO2溶液中滴加CuCl2溶液,可能观察到的现象是______________________________________________________________________________。
(4)纳米级氧化亚铜(Cu2O)常作催化剂。工业上可用电解法制备,装置如图所示。
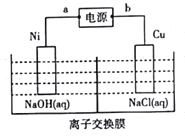
①a极名称是_________________;阳极的反应式为___________________。
②若电解过程中有1mol离子通过交换膜,则制备Cu2O的质量为_____________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com