
科目: 来源: 题型:
【题目】实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr ![]() C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g/cm3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g/mL);25 mL水。试回答下列问题:
(1)该实验应选择下图中的a装置还是b装置?。
(2)反应装置中的烧瓶应选择下列哪种规格最合适( )
A.50 mL
B.100 mL
C.150 mL
D.250 mL
(3)冷凝管中的冷凝水的流向应是( )
A.A进B出
B.B进A出
C.从A进或B进均可
(4)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是 ( )
A. 固体SiO2一定是晶体
B. 晶体有固定的组成,非晶体没有固定的组成
C. 晶体内部的微粒按一定规律呈周期性有序排列
D. 冰和固体碘晶体中相互作用力相同
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2既是温室气体,也是重要的化工原料,二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入足量的活性炭和一定量的NO,发生反应C(s)+ 2NO(g) ![]() N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
浓度/(mol/L)/\时间/min | 0 | 10 | 20 | 30 | 40 |
NO | 2.0 | 1.16 | 0.40 | 0.40 | 0.6 |
N2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 |
CO2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 |
①根据图表数据分析T1℃时,该反应在0~10min内的平均反应速率v(N2)=____________mol·L-1·min-1;计算该反应的平衡常数K=_____________。
②若30min后只改变某一条件,据上表中的数据判断改变的条件可能是____________(填字母编号)。
A.加入合适的催化剂 B.适当缩小容器的体积
C.通入一定量的NO D.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:3:3,则达到新平衡时NO的转化率___________(填“升高”或“降低”),△H______0(填“>”或“<”)。
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式_______________。
(3)二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池(电解质为KOH溶液)的负极反应式为:_________________________。
(4)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10 的溶液,则溶液中c(CO32-)∶c(HCO3-)=_______________。[常温下K1(H2CO3
②欲用2LNa2CO3溶液将4.66gBaSO4 固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为__________________________。[已知:常温下Ksp(BaSO4)=1×10-11,Ksp(BaCO3)=1×10-10]。(忽略溶液体积的变化)
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,根据表中给出的①—⑥六种元素,回答下列问题:
族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ |
(1)画出元素④的原子结构示意图__________;
(2)元素①形成的最简单有机物的化学式是__________;
(3)表中所列元素中非金属性最强的元素是__________(填元素符号)
(4)元素⑤形成的最高价氧化物对应的水化物的化学式是__________;
(5)元素③和元素⑥形成的化合物的电子式是__________。
(6)表中所列元素中金属性最强的元素是__________(填元素符号)
查看答案和解析>>
科目: 来源: 题型:
【题目】以锌片和铜片为电极,以稀硫酸为电解质溶液的原电池中,当导线中通过2mol电子时,下列说法正确的是( )
A.锌片溶解了1mol,铜片上析出1mol氢气
B.锌片发生还原反应
C.正极附近的SO42﹣离子浓度逐渐增大
D.电池工作时,电子由正极通过外电路流向负极
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应既属于氧化还原反应,又是吸热反应的是( )
A.生石灰与水作用制熟石灰
B.灼热的木炭与CO2反应
C.甲烷在氧气中的燃烧反应
D.Ba(OH)28H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目: 来源: 题型:
【题目】I.A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图a所示(部分产物已略去)。
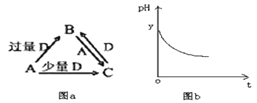
(1)若A为非金属单质,它的组成元素是形成物质种类最多的元素,D是空气的主要成分之一。请写出B的电子式_____________________________________________。
(2)若A为使用最广泛金属的单质,D是某强酸的稀溶液,则反应B+A![]() C的离子方程式为:__________________________________________________。
C的离子方程式为:__________________________________________________。
(3)若A为强碱,D为形成酸雨的气态氧化物。常温时将B的水溶液露置于空气中一段时间,其pH变化如图b所示,则其pH变化的原因是__________________。
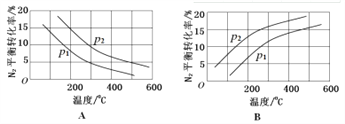
II.(1)对于合成氨反应:N2(g) +3H2(g) ![]() 2NH3(g) △H= -92.4kJ/mol。在其他条件相同时,分别测定N2的平衡转化率在不同压强(p1、p2)下随温度变化的曲线,下列图示正确的是_________(填“A”或“B”);比较p1、p2的大小关系:_____________。
2NH3(g) △H= -92.4kJ/mol。在其他条件相同时,分别测定N2的平衡转化率在不同压强(p1、p2)下随温度变化的曲线,下列图示正确的是_________(填“A”或“B”);比较p1、p2的大小关系:_____________。
(2)尿素是一种高效化肥,与水在一定条件下可以生成氨气:CO(NH2)2(s)+H2O(l)![]() 2NH3(g)+CO2(g) △H = +133.6kJ/mol。关于该反应,下列说法正确的是___________(填序号)。
2NH3(g)+CO2(g) △H = +133.6kJ/mol。关于该反应,下列说法正确的是___________(填序号)。
A.在平衡体系中再加入少量CO(NH2)2,平衡正向移动
B.降低温度使尿素的转化率减小
C.从反应开始到达到平衡时容器中混合气体的平均相对分子质量始终保持不变
D.恒温恒容时,向平衡体系中再充入少量氨气,平衡常数减小
(3)常温下向100mL0.2mo/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。

NH3·H2O的电离常数为_____________________________(已知lg1.8 = 0.26)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com