
科目: 来源: 题型:
【题目】X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是( )
A.原子序数:X<Y
B.原子半径:X<Y
C.离子半径:X>Y
D.最外层电子数:X<Y
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列有关说法不正确的是( )
A. 在元素周期表的金属和非金属分界线附近寻找半导体材料
B. 漂白粉失效是由于漂白粉中的Ca(ClO)2与空气中的CO2反应生成的HClO见光分解
C. 少量液溴要保存在棕色细口瓶中,并在液溴上面加水封
D. 向煤中加入适量CaCO3,可大大减少燃烧产物中温室气体的排放
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下图所示,下列说法不正确的是
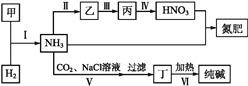
A. 甲、乙、丙三种物质中都含有氮元素
B. 反应Ⅰ、Ⅱ、Ⅲ中含氮元素的反应物都被氧化
C. Ⅴ中发生反应:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl
D. Ⅵ利用丁物质受热易分解的性质
查看答案和解析>>
科目: 来源: 题型:
【题目】能用H++OH-=H2O表示的化学方程式是( )
A.氢氧化钠溶液与醋酸反应
B.氢氧化铁与硫酸反应
C.氢氧化钡与硫酸反应
D.硫酸氢钠与氢氧化钠溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】把图2中的物质补充到图1中,可得到一个氧化还原反应的离子方程式。对该氧化还原反应的离子方程式,下列说法不正确的是( )
图1: Mn2+……→H+……
图2:![]()
A. Mn 元素从反应前的+2价升高到了反应后的+7价,Mn2+做还原剂
B. I![]() 作氧化剂,具有氧化性
作氧化剂,具有氧化性
C. 随着反应的进行,溶液酸性增强
D. 若有2 mol Mn2+参加反应,则转移5 mol电子
查看答案和解析>>
科目: 来源: 题型:
【题目】钯(Pd)元素的原子序数为46,下列叙述错误的是( )
A. ![]() Pd和
Pd和 ![]() Pd互为同位素 B. Pd核外有46个电子
Pd互为同位素 B. Pd核外有46个电子
C. Pd核内有46个质子 D. ![]() Pd的原子核内有46个中子
Pd的原子核内有46个中子
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nSnnPn |
B | 基态原子中的未成对电子数是同周期中最多的 |
C | 最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题(用对应元素的元素符号作答):
(1)写出D元素基态原子的价电子排布式 , E2+价电子的轨道表示式。
(2)这5种元素中电负性最大的元素是(填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为(填元素符号)
(3)B、C、D的简单离子的半径由大到小的顺序为(用离子符号表示)
(4)写出C的核外有18个电子的氢化物的电子式。
查看答案和解析>>
科目: 来源: 题型:
【题目】I、高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是____。
(2)放电时,正极发生____(填“氧化”或“还原”)反应;已知负极反应为Zn-2e-+2OH-====Zn(OH)2,则正极反应为_______________________。
(3)放电时,____(填“正”或“负”)极附近溶液的碱性增强。
II、在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,回答下列问题:
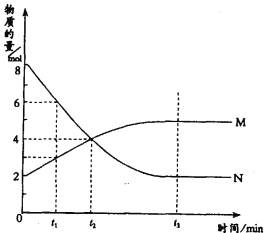
(4)反应的化学方程式为:______________。
(5)反应在_______时刻达到平衡状态。
(6)反应在_____时刻之前正反应速率大于逆反应速率。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g) ![]() 2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:下列说法不正确的是( )
2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:下列说法不正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 012 | 011 | 010 | 010 |
A.反应前2min的平均速率v(Z)=2.0×10-5mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前:v(逆)>v(正)
C.该温度下此反应的平衡常数:K=1.44
D.保持其他条件不变,起始时向容器充入0.32mol气体X和0.32mol气体Y,到达平衡时,n(Z)=0.024mol
查看答案和解析>>
科目: 来源: 题型:
【题目】能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的合理开发是当今社会面临的严峻课题,回答下列问题:
(1)我国是世界上少数以煤为主要燃料的国家,下列关于煤作燃料的论点正确的是 ___________________(填字母)。
A.煤是重要的化工原料,把煤作燃料简单燃烧掉太可惜,应该综合利用
B.煤是发热量很高的固体燃料,我国煤炭资源相对集中,开采成本低,用煤作燃料实惠
C.煤燃烧时产生大量二氧化硫和烟尘,对环境污染严重
D.通过洁净煤技术,如煤的气化和液化,以及烟气脱硫,不仅减轻了燃煤污染,还能提高煤燃烧的热利用率
(2)乙醇是未来内燃机的首选环保型液体燃料。2.0 g乙醇完全燃烧生成液态水放出59.43 kJ的热量,则乙醇燃烧的热化学方程式为____________________________________________________________。
(3)由于C3H8(g)=C3H6(g)+H2(g) ΔH=+b kJmol1(b>0)的反应中,反应物具有的总能量________(填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________(填“放出”或“吸收”)能量才能转化为生成物。
(4)关于用水制取二次能源氢气,以下研究方向不正确的是________________
A.组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(5)已知下列两个热化学方程式:
A、2H2(g)+O2(g) ===2H2O(l) △H=-571.6 kJmol-1 B、C3H8(g)+5O2(g) ===3CO2(g)+4 H2O(l) △H=-2 220 kJmol-1,其中,能表示燃烧热的热化学方程式为___________(A或B),其燃烧热为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com